En Chile el consumo de EPA y DHA es mucho menor a las recomendaciones internacionales. Para mejorar el aporte de omega-3 en el embarazo y lactancia desarrollamos una bebida láctea fortificada con 60 mg de DHA y 14 mg de EPA por 200/ml. El objetivo del estudio fue evaluar su efecto en embarazo, parto y recién nacido, composición lipídica de los glóbulos rojos y de la leche materna. Se estudió una cohorte de embarazadas que recibieron dos Kg/mes del nuevo producto (GE n = 175) o la misma cantidad de la leche en polvo que distribuye el Ministerio de Salud (GC n =177). Se analizó consumo de la bebida láctea y otros alimentos fuentes de EPA y DHA y las características del embarazo, parto y recién nacido. En una submuestra de cada grupo se analizó al ingreso y a los 60 días la composición de los ácidos grasos de membranas del glóbulo rojo de la madre y de la leche materna a los 2 meses post parto. El 16 y 53% de la muestra no consumía pescado o mariscos respectivamente y menos del 25% consumía pescado en forma semanal. La intervención aumentó el aporte diario de DHA de 48,8 mg (IC 38,7 – 57,5) a 147,8 mg (IC 128,4 – 167,9) (p < 0,001). El GE tuvo mayores niveles de DHA en los fosfolípidos de la membrana del glóbulo rojo materno: 17,9% (IC 12,9 – 23,0) versus 11,1% (IC10,2 – 13,0) p < 0,002 y aumentó en 50% la concentración de ácidos grasos omega-3 en la leche materna (p 0,06). Se observó menor prevalencia de partos pretérminos en el GE (2,8 vs 10,6%), aunque sin significación estadística. La bebida láctea logró un aumento significativo del consumo de DHA en el embarazo y lactancia y una mejoría de la composición de ácidos grasos en el glóbulo rojo y leche materna, sugiriendo que es una buena estrategia de intervención en esta población.
Palabras clave: Embarazo, lactancia, DHA, EPA, omega-3, fortificación.
EPA and DHA consumption in Chile is markedly below international daily intake recommendations. For improvement of such low intake level, we developed a fortified powdered dairy drink, containing 60 mg/serving of DHA and 14 mg/serving of EPA. Objectives: to evaluate the effects of DHA consumption during pregnancy, parturition, and in the newborn, on lipid composition of red blood cell membranes and levels of DHA and EPA on human milk during lactation. One hundred and seventy five (175) pregnant women received 2 kg/month of the fortified powdered dairy drink (GE), and 177 received the regular milk provided by the Ministry of Health (GC). We monitored daily intake of the dairy drink and all other sources of DHA and EPA in the diet, and measured general biological indicators during pregnancy, parturition, and in the new born. On a subsample of 14 women on each group (GE and GC), we measured fatty acid composition of red blood cell membranes after 0 and 60 days of consumption with the fortified dairy drink, and levels of DHA and EPA on human milk after 2 months of lactation. Of all women in the study, 16% had no consumption of fish, and 53% had no consumption of sea food. Less than 25 % of all women had fish on a weekly basis. Consumption of the fortified dairy drink tripled intake of DHA, from 48.8 mg/day (CI 38.7-57.5) to 147.8 mg/day (CI 128.4-167.9) (p<0.001). The GE group had a higher content of DHA on the phospholipids of red blood cell membranes: 11.1% (CI 10.2-13.0) versus 17.9% (CI 12.9-23.0) (p<0.002). Concentration of DHA and w-3 fatty acids increased 50% in milk of women consuming the fortified dairy drink (p<0.06). There was a lower incidence of preterm parturitions on the GE group (2.8 vs 10.6%), but without statistical significance. The consumption of the fortified dairy drink produced a significant increase of DHA consumption during pregnancy and lactation, and an improved composition of red blood cell membranes, as well as in human milk, proving to be an appropriate intervention strategy for the target population.
Key words: Pregnancy, lactation, DHA, EPA, fortification.
https://doi.org/10.37527/2009.59.3.007
Facultad Medicina, Universidad Chile, Gerencia Desarrollo & Calidad, Watt’s SA, Departamento de Alimentos y Nutrición, Ministerio de Salud. Santiago, Chile
Los ácidos grasos poliinsaturados de cadena larga de la familia omega-3 son esenciales a través de todo el ciclo vital, especialmente el ácido eicosapentanoico (EPA) y docosahexanoico (DHA). Un mayor consumo de estos ácidos grasos en el embarazo y lactancia se ha asociado a un mejor desarrollo cognitivo y visual del niño los primeros años de vida (1-4) y en menor grado a una mayor duración de la gestación (5). Estudios más recientemente han estado orientados a evaluar sus efectos en la salud cardiovascular (6-9) y mental del adulto y adulto mayor (10-13).
No hay consenso sobre los niveles de consumo óptimo de DHA en las distintas etapas de la vida, pero la mayor parte de los grupos técnicos lo sitúan entre 200 y 500 mg/día en la población adulta (5). En Chile, el consumo de pescado o de otros alimentos de origen marino es muy bajo, lo que determina un aporte de DHA del orden de sólo 50 mg/día, muy por debajo de las recomendaciones y de lo observado en otros países (14-16).
Las principales alternativas para mejorar el aporte de DHA son fomentar un mayor consumo de pescado, utilizar suplementos de aceites marinos o alimentos funcionales que contengan DHA, demostrándose en general la efectividad de estas medidas (17-21). Un estudio nacional mostró un aumento significativo de los ácidos grasos omega-3 de la leche materna con una suplementación de 160 gramos 2 veces por semana de un pescado graso en conserva (jurel), efecto que no se mantuvo al suspender la suplementación (22,23). Ello sugirió la necesidad de explorar otras formas de intervención que logren una mejor sustentabilidad, optándose por el desarrollo de un bebida láctea enriquecida con DHA para las embarazadas y nodrizas beneficiarias del Programa Nacional de Alimentación Complementaria del Ministerio de Salud, que representan al 65% de la población nacional.
El alimento se elaboró a partir de leche en polvo y cereales hidrolizados fortificados con vitaminas, minerales y con ácidos grasos omega-3 microencapsulados que aportan 60 mg de DHA y 14 de EPA por cada porción de 200 ml (24). El objetivo de este estudio fue evaluar el impacto de este producto en el aporte de DHA a través de la dieta, su efecto en el embarazo, parto, recién nacido y en la composición lipídica de los glóbulos rojos de la embarazada y de las grasas de la leche materna. El proyecto fue aprobado por el Comité de Ética de la Facultad de Medicina, Universidad de Chile y de los respectivos servicios de salud, donde se desarrolló.
Selección de la muestra. Diseño semiexperimental en una cohorte de embarazadas controladas en cinco centros de atención primaria de Santiago del sistema público de salud. En forma aleatoria las embarazadas fueron asignadas al grupo experimental (GE n = 175) que recibió dos kg mensuales de la bebida láctea con DHA o grupo control (GC n = 177), que recibió 2 kg. mensuales de la leche en polvo del programa del Ministerio de Salud (26% materia grasa, fortificada con hierro, zinc y vitamina C). la bebida láctea se diluye al 12%, lo que permitiría el consumo de tres raciones diarias de 200 ml. El alimento fue entregado gratuitamente en los dos grupos desde el primer control prenatal hasta los dos meses post parto.
Los criterios de inclusión fueron: firma del consentimiento informado por parte de la madre, primer control prenatal < de 14 semanas de embarazo, edad > 18 años, embarazo único y ausencia de patologías crónicas que afecten la evolución del embarazo o el crecimiento fetal (enfermedades hepáticas, renales, diabetes, etc.).
La estimación del tamaño de muestra se basó en el test de Wilcoxon para variables continuas: incremento de peso durante el embarazo, consumo de DHA o peso del recién nacido. Se consideró nivel de significación 0,05, valor de p1 = 0,4 (probabilidad de que un valor en el grupo experimental sea menor que en el grupo control), test de dos colas y poder 80, lo que determinó la necesidad de estudiar 131 mujeres en cada grupo. Considerando una pérdida del 25% la muestra se aumentó a 175 madres en cada grupo.
Encuesta de consumo. Las madres fueron entrevistadas en tres oportunidades durante el embarazo y a los dos meses post parto para obtener información sobre el consumo del alimento los dos días previos a la encuesta. En la última entrevista del embarazo se aplicó además una encuesta de tendencia de consumo para evaluar la frecuencia y cantidad de consumo habitual de distintas variedades de pescados y mariscos. No se consideraron alimentos fuentes de ácido alfa linolénico. A partir de esta información se calculó la mediana de consumo diario de estos alimentos y el consumo de EPA y DHA utilizando la tabla chilena de composición de ácidos grasos (25).
Información sobre la madre y recién nacido. De los registros del centro de salud y de la maternidad se obtuvo información sobre las patologías presentadas durante el embarazo, incremento de peso materno, edad gestacional al parto, peso y puntaje Apgar del recién nacido.
Obtención de muestras de sangre. Previo ayuno de 12 horas se obtuvo por punción venosa 5 ml. de sangre en 14 madres del GC y 11 en el GE, en un tubo con EDTA, y fue trasladada en cadena de frío antes de 2 horas y almacenada a – 80º C hasta su análisis. La muestra se tomó al momento de ingresar al estudio y en las mismas madres, 60 días después. El tamaño de muestra se estimó considerando un aumento del 50% del DHA en el grupo intervenido, desviación estándar común 5%, nivel de significación 0,05, poder del test 80 y test de una cola, para lo cual se requerían 14 madres en cada grupo.
Las membranas de los glóbulos rojos se separaron según Huertas et al (26), y los lípidos de las membranas se extrajeron según Bligh y Dyer (27) .Los ésteres metílicos de los ácidos grasos fueron cuantificados por cromatografía gaseosa empleando un Cromatógrafo Hewlett- Packard modelo 6890, equipado con una columna capilar apolar (50 m, x 0.22 mm; BPX 70).
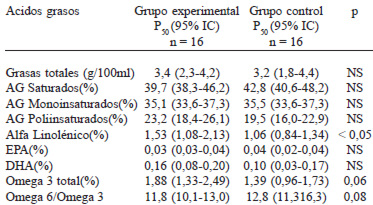
Obtención de muestras de leche materna. A los 60 ± 10 días postparto se obtuvo en condiciones estandarizadas en 16 mujeres de cada grupo una muestra de leche. En el Centro de Salud o su propio domicilio se solicitó a la madre que amamantara al hijo y extraer manualmente 5 ml de leche cuando estaba terminando el primer pecho. Las muestras fueron trasladadas en cadena de frío y almacenadas a – 80º C. Posteriormente fueron procesadas de acuerdo al método de Lepage-Roy 22, por transesterificación directa de los lípidos. El análisis de los ácidos grasos se realizó en un cromatógrafo gaslíquido Perkin Elmer Autosystem XL, con inyector automático y FID, utilizando una columna capilar BPX 70 x .25 mm DI, determinándose áreas bajo la curva por un programa computacional. Los ácidos grasos fueron identificados por los tiempos de retención, en relación a estándares de ácidos grasos y los valores obtenidos fueron expresados como porcentaje del total de ácidos grasos.
Análisis estadísticos. Los datos fueron procesados con el programa STATA 9.2. Se analizó la normalidad de cada variable a través del test de Shapiro-Wilk. Para la comparación entre grupos se usaron promedios y desviaciones estándar en variables continuas con distribución normal, el test de Wilcoxon y de Kruskall Wallis en variables sin distribución normal y chi2 en variables categóricas. En todos los casos se consideraron significativos valores de p < 0,05.
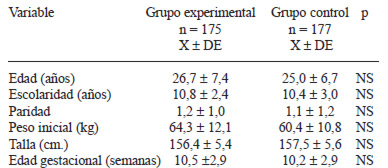
Ingresaron al estudio 352 embarazadas, 175 en el grupo intervenido y 177 en el grupo control, con características generales similares, que reflejan bien a las beneficiarias del sistema público de atención primaria en Chile (Tabla 1).
Durante el seguimiento hubo una pérdida importante de la cohorte inicial, ya sea por cambios de domicilio, inasistencias a control o por solicitud de las propias madres de retirarse del estudio. Se logró obtener información del parto sólo en 96 mujeres del grupo control (55% del grupo inicial) y 63 del grupo con Bebida Láctea (36% del grupo inicial). No hubo diferencias significativas en las principales variables analizadas en el grupo que abandonó el estudio respecto al que continuó en la cohorte.
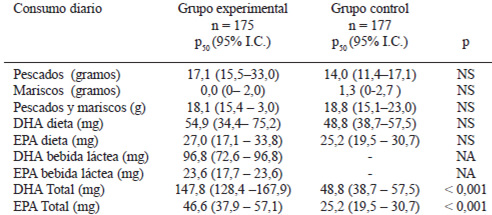
Menos del 25% de la muestra estudiada consumía pescado en forma semanal y sólo el 4% > 2 veces a la semana y el 16 y 53% no consumía pescado ni mariscos, respectivamente. Ello determinó una mediana de consumo de pescado del orden de 100 g. semanales y de DHA cercana a los 50 mg/día a partir de la alimentación habitual (Tabla 2). La intervención con la bebida láctea permitió un aporte adicional de DHA equivalente al doble del consumo de la dieta, con diferencias significativas respecto a los controles. A pesar de la bebida láctea fortificada sólo el 10% del grupo intervenido logró un consumo diario de DHA de 200 mg o más.
El consumo promedio de la bebida láctea fue 1,5 ± 1,0 tazas diarias durante el embarazo y 1,8 ± 1,0 en la lactancia, cifra inferior a las tres tazas programadas de acuerdo a la cantidad de producto que se entregó a cada beneficiaria (24).
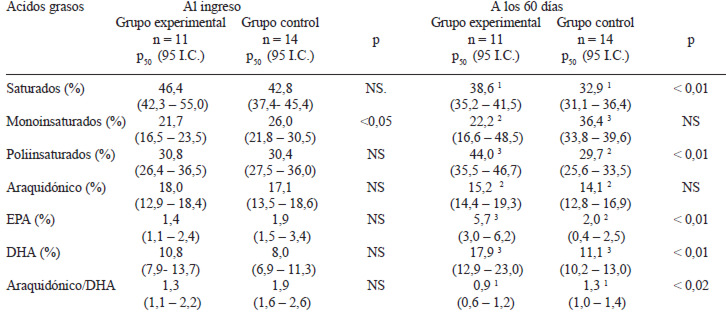
La composición de ácidos grasos en los fosfolípidos de la membrana del glóbulo rojo al ingresar al estudio y 60 días después, se presenta en la Tabla 3. Ambos grupos tenían características similares en el primer control prenatal, con predominio de ácidos grasos saturados, sin diferencias significativas entre ellos, a excepción de un mayor porcentaje de grasas monoinsaturadas en el grupo control. A los 2 meses se observó un aumento del porcentaje de EPA y DHA y un cambio favorable en la relación con el ácido araquidónico, en el grupo intervenido. El aumento fue especialmente importante en EPA, con niveles finales cuatros veces mayores respecto al valor inicial en el grupo experimental (p < 0,01). Al comparar la línea basal con los 60 días también se observaron algunos cambios positivos en el grupo control: disminución de los ácidos grasos saturados y aumento de los monoinsaturados y DHA.
El 18,8% de las madres presentó alguna patología durante el embarazo (datos no mostrados). Las patologías más frecuentes fueron hipertensión arterial y preeclampsia (6,7%), diabetes gestacional (6,0%), infecciones del tracto urinario (2,7%) y colestasia gravídica (1,3%). No se observaron diferencias entre los grupos, salvo una tendencia a una mayor frecuencia de hipertensión y preeclampsia en el grupo control (8,3% v/s 4,6% NS).
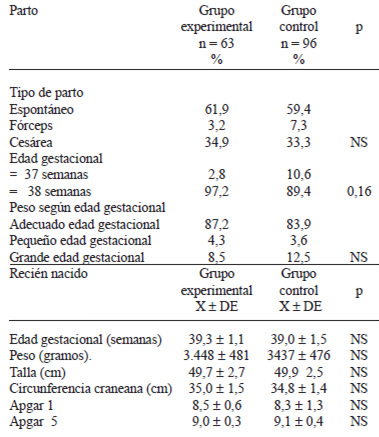
La mayor parte de los partos fueron espontáneos, de término y con recién nacidos adecuados para la edad gestacional, sin diferencias significativas entre los grupos (Tabla 4). La prevalencia de partos pretérminos fue 3,8 veces mayor en el grupo control, valor que no alcanza significación estadística, pero que sigue la tendencia descrita en algunos estudios. La edad gestacional al parto y las características antropométricas de los recién nacidos fueron similares en ambos grupos, destacando un alto peso promedio al nacer y el resto de los valores en el rango normal.
En ambos grupos la concentración de DHA en leche materna fue bastante baja en relación a lo observado en países con mayor consumo de pescado. El grupo intervenido tuvo un 60% más de DHA en la leche materna, no estadísticamente significativo por la amplia variabilidad de esta variable y el reducido tamaño de muestra. También aumentó la concentración de omega-3 y mejoró la relación omega 6/omega 3, en el límite de la significación estadística (Tabla 5).
Los múltiples beneficios del DHA en el embarazo y lactancia se encuentran ampliamente documentados en la literatura. La principal fuente de DHA en la dieta son los pescados, cuyo nivel de consumo es muy bajo en muchos países. Las guías de alimentación de la población chilena recomiendan el consumo de al menos dos porciones semanales de pescado durante el embarazo y lactancia, cifra que cumple menos del 5% de la población nacional a pesar de la extensa costa del país. Según los estudios de consumo aparente o hojas de balance que realiza FAO en cada país, en los últimos 20 años se ha triplicado en Chile el consumo de carnes (vacuno, cerdo, pollo) mientras que el consumo de pescado se mantiene estable y en niveles muy bajo, representando menos del 7% del consumo total de este grupo de alimentos.
Diversas estrategias de intervención pueden contribuir a mejorar esta situación, incluyendo campañas educativas, modificación de los programas de alimentación institucional, subsidios específicos para mejorar el acceso a la población de menores recursos, etc. Sin embargo su efecto necesariamente se verá en el mediano o largo plazo y su sostenibilidad es variable, como fue la experiencia en un estudio previo, donde la educación nutricional no fue suficiente para mantener los niveles de consumo después de suspender la entrega gratuita de una ración de pescado en conserva (23).
Otra estrategia está orientada al uso de suplementos de aceite de pescado, ya que una dosis diaria puede aportar la misma cantidad de DHA que 100g de pescado graso y bastante más que una porción de pescado de carne blanca. Muchas de las intervenciones de la literatura se han basado en el uso de suplementos y han sido exitosas (17-21, 28). Un gran problema es como llevar los resultados de un estudio clínico controlado a una intervención a gran escala, donde la adhesividad al tratamiento probablemente puede ser baja en un segmento de la población.
Finalmente está la posibilidad de utilizar un alimento de consumo habitual que sea fortificado con DHA, tal como se ha hecho con otros micronutrientes (hierro, ácido fólico, vitamina A, yodo, etc.). Para lograr éxito a nivel de salud pública el alimento debe ser de consumo masivo en el grupo objetivo. Chile tiene la ventaja de que el Ministerio de Salud realiza desde hace varias décadas un programa de alimentación materno infantil, que beneficia regularmente al 65% de la población nacional, con especial énfasis en la población más vulnerable. Ello dio la oportunidad de desarrollar un producto fortificado especialmente orientado a las madres embarazadas y en lactancia, que tuvo una adecuada aceptabilidad en un estudio piloto.
El objetivo de este estudio fue evaluar su consumo y el aporte de DHA a la dieta habitual. En forma complementaria se evaluaron potenciales efectos beneficios en el embarazo, parto y recién nacido, aunque ellos son más difíciles de demostrar en una muestra relativamente pequeña de un estudio cuasi experimental. Una debilidad del estudio es la importante pérdida de la cohorte durante el seguimiento, llegándose a encuestar solo al 70% de la muestra al final del embarazo y obtener datos sobre el parto y recién nacido en solo el 45% de ellas. La perdida fue algo mayor en el grupo experimental, fundamentalmente por la propia solicitud de las madres de retirarse del estudio. Este hecho en parte fue interpretado por una menor aceptabilidad del producto, aunque también puede haber influido la limitada información que se entregó a las madres sobres sus potenciales beneficios nutricionales. Estudios posteriores han demostrado que se mantiene una mejor aceptabilidad para la leche entera 26% de materia grasa que han estado recibiendo por varios años y que tiene la ventaja de poder ser compartido con el resto del grupo familiar. Para poder evaluar un posible sesgo por la perdida muestral se analizaron las principales características del grupo que se mantuvo en el seguimiento respecto de aquellos que se retiraron, sin encontrase diferencias entre ellos, lo que reduce esa posibilidad.
Los resultados demuestran que se logró triplicar el nivel de consumo de DHA respecto al grupo control, aunque no se lograron los niveles óptimos recomendados, ya que la ingesta real de la bebida láctea fue la mitad de lo esperado. El menor consumo podría ser explicado por algún grado de rechazo al producto, aunque también por que cerca del 40% de las mujeres no consumen leche en forma habitual (24). Ello sugiere la necesidad de reforzar la consejería nutricional orientada a incentivar un mayor consumo de lácteos y pescado. Otra posibilidad es aumentar la concentración de DHA en la bebida láctea, aunque debieran hacerse estudios de estabilidad para evaluar la vida útil del producto y nuevos estudios de aceptabilidad y consumo. También es importante reevaluar las características organolépticas del producto, lo que ya se está haciendo.
De acuerdo a lo esperado la intervención modificó favorablemente la composición de los ácidos grasos de la membrana de los glóbulos rojos, aunque no se evidenciaron efectos positivos en la evolución del embarazo, parto y recién nacido. Sin embargo debe tenerse en cuenta que la población estudiada es de bajo riesgo, con buen estado nutricional inicial, adecuadamente controlada, con un incremento promedio de peso durante la gestación de 13,2 ± 5,0 kg y con peso promedio al nacer de 3.440 ± 480 gramos, donde es difícil modificar los resultados. Se observó una reducción importante de los partos pretérminos, aunque no significativa, lo que requiere ser estudiado en una muestra de mayor tamaño.
Se logró un aumento de 50% en la concentración de ácidos grasos omega-3 en la leche materna, que no fue estadísticamente significativa, probablemente por el reducido tamaño de muestra y el insuficiente nivel de consumo total de DHA alcanzado. Sin embargo, aún después de la suplementación la concentración de DHA en la leche materna fue menos de la mitad observada a nivel mundial y menos del 15% de los valores se ubicaron en el intervalo superior, lo que refuerza la necesidad de utilizar otras medidas complementarias para mejorar el consumo de estos ácidos grasos (29).
A pesar de estas limitaciones, el estudio permitió demostrar que la intervención era factible, lo que contribuyó a que el Ministerio de Salud incorporara este alimento a nivel nacional. Desde agosto del 2008 cerca de 200 mil embarazadas y nodrizas del país están recibiendo regularmente este producto, lo que permitirá poder realizar una nueva evaluación de impacto a mayor escala.
Recibido: 14-04-2009
Aceptado: 07-07-2009