As características nutricionais, funcionais e agrícolas do amaranto são responsáveis pelo aumento do interesse por este alimento nas últimas décadas. O grão pode ser cozido, estourado, torrado, extrusado ou moído para ser consumido. Foi avaliado o efeito destes processamentos na atividade antioxidante do grão de amaranto, através das determinações do teor de fenólicos totais e da atividade antioxidante in vitro por dois métodos: inibição da oxidação lipídica pelo sistema β-caroteno/ácido linoléico e índice de atividade antioxidante pelo aparelho Rancimat®. Os processamentos reduziram em média o teor de fenólicos totais do grão de amaranto de 31,7 para 22,0 mg de equivalentes de ácido gálico/g de resíduo seco. Observouse que o extrato obtido por etanol do grão torrado foi o único a apresentar menor índice de atividade antioxidante (IAA) em relação ao grão cru (1,3 v 1,7). Os processos de extrusão, torração e explosão não alteraram a capacidade de inibição da oxidação lipídica (IOL) do amaranto (55%). Já o cozimento aumentou o IOL (79%), o que pode ter ocorrido devido ao maior tempo de processamento sob alta temperatura (100ºC/10min). Os métodos mais comuns de processamento do grão de amaranto ocasionaram redução do teor de fenólicos totais, no entanto a atividade antioxidante do estourado e do extrusado, avaliada pelos dois métodos, foi semelhante ao do grão cru. O grão de amaranto tanto cru como processado apresenta potencial antioxidante. Polifenóis, antocianinas, flavonóides, tocoferóis, vitamina C e compostos gerados na reação de Maillard podem estar relacionados à atividade antioxidante deste grão.
Palavras chave: Amaranthus cruentus, fenólicos totais, atividade antioxidante, processamento.
Amaranth has attracted increasing interest over recent decades because of its nutritional, functional and agricultural characteristics. Amaranth grain can be cooked, popped, toasted, extruded or milled for consumption. This study investigated the effect of these processes on the antioxidant activity of amaranth grain. Total phenolic content and in vitro antioxidant activity were determined according to two methods: inhibition of lipid oxidation using the β-carotene/linoleic acid system and the antioxidant activity index using the Rancimat® apparatus. The processing reduced the mean total phenolics content in amaranth grain from 31.7 to 22.0 mg of gallic acid equivalent/g of dry residue. It was observed that the ethanol extract from toasted grain was the only one that presented a lower antioxidant activity index compared with the raw grain (1.3 versus 1.7). The extrusion, toasting and popping processes did not change the capacity to inhibit amaranth lipid oxidation (55%). However, cooking increased the inhibition of lipid oxidation (79%), perhaps because of the longer time at high temperatures in this process (100°C/10 min). The most common methods for processing amaranth grain caused reductions in the total phenolics content, although the antioxidant activity of popped and extruded grain, evaluated by the two methods, was similar to that of the raw grain. Both raw and processed amaranth grain presents antioxidant potential. Polyphenols, anthocyanins, flavonoids, tocopherols, vitamin C levels and Maillard reaction products may be related to the antioxidant activity of this grain.
Key words: Amaranthus cruentus, total phenolics, antioxidant activity, processing.
Departamento de Nutrição. Faculdade de Saúde Pública Universidade de São Paulo (USP). Brasil
Agência financiadora: Fundação de Amparo a Pesquisa do Estado de São Paulo.
O grão de amaranto, (Amaranthus sp.), apresenta características nutricionais, funcionais e agrícolas responsáveis pelo aumento do interesse por este alimento nas últimas décadas (1).
O Amaranthus cruentus L. possui cerca de 4% de cinzas, 8% de lipídios, 15% de proteína, 13% de fibra alimentar e 60% de amido (2-4). O teor protéico e o seu perfil de aminoácidos fazem com que seja uma atrativa fonte protéica, apresentando conteúdo expressivo de aminoácidos essenciais, especialmente lisina (5%) e aminoácidos sulfurados (4%), que são limitantes na maioria dos grãos utilizados para a alimentação humana (5-8). Também, destacam-se na sua composição os teores de vitaminas e minerais (3). E por ser isento de glúten o seu consumo vem sendo recomendado para celíacos (9). Outros compostos estão presentes em sua composição, como o esqualeno, a fibra alimentar, os tocoferóis, os tocotrienóis, os flavonóides e os compostos fenólicos (10-17), os quais podem apresentar ação antioxidante.
A capacidade antioxidante dos alimentos depende da forma como este é consumido, seja na forma in natura ou processado. Kaur e Kappor (18) consideram que o tratamento térmico é aprincipal causa da alteração do teor de antioxidantes naturais em alimentos. O processamento e os procedimentos para a preservação dos alimentos podem ser responsáveis tanto pelo aumento quanto pelo decréscimo da ação antioxidante, dependendo de muitos fatores, tais como: estrutura química, potencial de oxiredução, sua localização na matriz e possíveis interações com outros componentes do alimento (19).
O grão de amaranto pode ser submetido a vários processamentos para ser consumido (4,20). Assim, o objetivo deste trabalho foi avaliar os efeitos dos processos de cocção, explosão, torração e extrusão na atividade antioxidante in vitro do grão de amaranto.
Grãos de amaranto (Amaranthus cruentus) foram adquiridos da Embrapa Cerrados (Planaltina-DF). Estes foram processados de quatro formas distintas, de acordo com Bressani (20) com adaptações de Capriles e col. (4). Cocção: foi realizada pela imersão do grão em água em ebulição (100°C) por 10 minutos. Explosão: para estourar, o grão foi submetido ao contato com superfície aquecida a 90ºC por 10 a 15 segundos. Torração: foi realizada através de contato com superfície aquecida a 120ºC por cerca de 1 minuto. Extrusão: utilizou-se farinha desengordurada (1% de lipídeos base seca) com umidade ajustada para 15%. Foi necessário o desengorduramento prévio para possibilitar a obtenção de um produto aceito sensorialmente, uma vez que os lipídeos presentes no grão de amaranto (7,6%) prejudicam a expansão, a textura e o sabor do extrusado. O processo foi realizado em extrusora de parafuso único com razão de comprimento/diâmetro de 20 e quatro zonas de aquecimento (Inbra 200 – INBRAMAQ, Indústria de Máquinas Ltda, São Paulo, Brazil). As condições foram: velocidade de rotação da rosca em 404 rpm e taxa de compressão de 1:1. As zonas de alimentação e de transição foram mantidas em 25oC e a zona de alta pressão e o orifício de saída em 90oC.
O processo de extração das substâncias presentes nos alimentos pode ocorrer de diversas maneiras, variando tanto o tipo de solvente, quanto a metodologia. No presente estudo, optou-se por trabalhar com o método de extração seqüencial utilizado por Nuutila e col. (21), com modificações, utilizando os solventes hexano e etanol, a fim de se obter a extração de compostos de polaridades diversas.
Foram pesados 3 g do grão de amaranto e de seus produtos e adicionados 20 mL de hexano P.A, em seguida, foi realizada agitação por 1 hora (agitador magnético marca Quimis, modelo Q.261.2) e ultrassonificação (marca Elma, modelo Transsonic digital S) por 20 minutos, sendo a amostra posteriormente filtrada (papel filtro qualitativo marca Nalgon, diâmetro 12,5 cm e porosidade 3 μ). O sobrenadante foi armazenado em balão volumétrico. O resíduo retido no filtro sofreu nova extração com hexano, sendo que o seu sobrenadante foi direcionado para o mesmo balão do anterior. Foram utilizados 10 mL de hexano para lavagem final do resíduo. Os sobrenadantes foram completados para o volume de 50 mL com hexano. O resíduo final da extração com hexano foi ressuspendido em etanol pelo mesmo processo descrito acima, sendo este descartado posteriormente.
Os extratos foram transferidos para frascos âmbar, sob atmosfera de nitrogênio e armazenados à -20oC até o momento das análises.
A quantificação do resíduo seco dos extratos foi determinada pelo método gravimétrico. Para isso, 2 mL do extrato foram transferidos para vidro relógio, previamente tarado, e este foi colocado em estufa à 105oC, por 16 horas, seguido de resfriamento em dessecador e pesagem, sendo a operação repetida até peso constante, obtendo então o resíduo seco em mg/mL de extrato (22).
A determinação do teor de compostos fenólicos presentes nos extratos de amaranto e nos seus produtos foi realizada pelo método desenvolvido por Genovese e col. (23), com reagente Folin-Ciocalteu. Foram adicionados a cada tubo de ensaio 0,25 mL do extrato, 2 mL de água destilada e 0,25 mL de solução de Folin-Ciocalteau 1:10. Os tubos foram agitados e deixados em repouso por 3 minutos. Foi então adicionado 0,25 mL de solução saturada de carbonato de sódio e o tubo agitado. Os tubos de ensaio foram deixados em repouso em banho-maria a 37oC durante 30 minutos. A absorbância foi lida a 750 nm em espectrofotômetro (marca Shimadzu, modelo TCC-24OA).
O ácido gálico foi utilizado como padrão. Os resultados obtidos foram expressos em mg de equivalentes de ácido gálico por grama de resíduo seco (mg EAG/g).
A inibição da oxidação lipídica utilizando o aparelho Rancimat® requer equipamento simples e pode ser utilizado como um método para determinar a atividade antioxidante, através de diversos substratos como a gordura vegetal hidrogenada e os óleos comestíveis. O lipídio é exposto a uma corrente de ar seco ou de oxigênio, a uma temperatura de 100 a 140oC, e o progresso das curvas de oxidação decorrente pode ser seguido pela determinação periódica do índice de peróxido. Estas curvas compreendem uma fase de indução, onde não se forma praticamente nenhum dos produtos secundários da oxidação, e uma fase de oxidação, durante a qual há uma grande elevação no índice de peróxido e detecção de produtos voláteis (principalmente ácido fórmico). A adição de um antioxidante resulta na inibição da oxidação (24).
Para avaliar a capacidade protetora das amostras de amaranto utilizou-se o aparelho Rancimat® 743, marca Metrohm, conectado ao programa PC: 743 Rancimat 1.0, onde foi medido o período de indução da oxidação lipídica da gordura vegetal hidrogenada contendo o extrato obtido por hexano e o obtido por etanol (24). Os extratos (2 mg de resíduo seco/mL) foram colocados nos tubos do Rancimat® e evaporados sob atmosfera de nitrogênio. Em seguida 3 g de gordura vegetal hidrogenada sem antioxidante foram adicionados em cada tubo e a mistura homogeneizada por 15 minutos em ultrasonificador. Depois, com a programação de temperatura de 110oC, ΔT = 1,5oC, fluxo de ar de 20 L/h, os tubos foram acoplados ao aparelho Rancimat®, até que a curva de condutividade em relação ao tempo de indução (TI) fosse finalizada para se calcular o Índice de Atividade Antioxidante (IAA). Um controle foi também preparado com a gordura vegetal hidrogenada sem antioxidante. Os resultados foram expressos como Índice de Atividade Antioxidante (IAA), calculado pela fórmula:

Donde: TI amostra = tempo de indução (h) da gordura vegetal hidrogenada + extrato contendo a amostra. TI controle = tempo de indução (h) da gordura vegetal hidrogenada.
A determinação da atividade antioxidante pelo sistema β-caroteno/ácido linoléico foi realizada de acordo com a metodologia descrita por Marco (25) e modificada por Miller (26). Como substrato, foi utilizado a emulsão de β-caroteno/ácido linoléico. Em 28 μL da solução de β-caroteno (concentração de 20 mg de β-caroteno/mL de clorofórmio) foram adicionados 28 μL de ácido linoléico e 200 mg de Tween 40 (emulsificante). Em seguida, o clorofórmio foi evaporado sob atmosfera de nitrogênio e acrescentados 140 mL de água oxigenada (água destilada tratada com oxigênio por 30 minutos).
No tubo de ensaio, 5 mL desta solução foi adicionada a 1 mL dos extratos diluídos (2 mg de resíduo seco/mL). Após homogeneização, a leitura foi feita em espectrofotômetro a 470 nm, sendo esta a leitura do tempo zero. Os tubos foram colocados em banho-maria (50oC) e a cada 15 minutos foi realizada leitura, até atingir o tempo de 2 horas. O controle foi preparado da mesma forma, porém para este no lugar da amostra foi adicionado 1 mL de etanol.
A oxidação do β-caroteno, obtida pelas medidas espectrofotométricas, indica a velocidade de transformação desse composto sob condições oxidantes (oxigênio e temperatura). Para o cálculo da porcentagem da inibição da oxidação lipídica (%IOL) foi utilizada a seguinte fórmula:

Resultados foram expressos como média e desvio padrão de três determinações. Os dados obtidos foram submetidos à análise de variância de um fator (ANOVA one-way). Diferenças entre as médias foram determinadas pelo teste de Tukey. A análise estatística foi realizada com o auxílio do software SPSS 13.0 (SPSS Institute Inc., Cary, NC), adotandose o nível de significância de p < 0,05.
Apenas os extratos obtidos por etanol foram utilizados para a análise de fenólicos totais, uma vez que soluções de polaridade intermediária – avançada são mais efetivas para extração destes compostos (27) (Tabela 1).
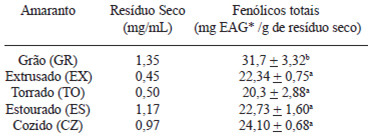
Os valores de fenólicos totais em relação ao resíduo seco constam na tabela 1. Observa-se que o grão (GR) apresenta maior quantidade destas substâncias em relação aos seus produtos (p < 0,05). Não foram observadas diferenças entre extrusado (EX), torrado (TO), estourado (ES) e cozido (CZ). No produto estourado, pode-se observar que o solvente etanol extraiu 1,17 mg de substâncias em cada mL de extrato e apresentou 22,73 mg EAG/g de resíduo seco. Este mesmo solvente extraiu apenas 0,54 mg de substâncias/mL no produto extrusado, no entanto, apresentou o mesmo teor de fenólicos totais do produto estourado. Foi verificado que nem todas as substâncias extraídas dos produtos de amaranto são compostos fenólicos. (Tabela 2).

Observa-se na Tabela 2 que os extratos obtidos por hexano não apresentaram atividade antioxidante, uma vez que valores de IAA destas amostras foram iguais ou inferiores a 1,0. Já os extratos obtidos por etanol foram capazes de inibir a oxidação lipídica dos substratos. GR, ES, EX, CZ não apresentaram entre si valores estatisticamente diferentes de IAA. (Tabela 3).

A inibição da oxidação lipídica (IOL) foi determinada apenas para o extrato obtido por etanol, uma vez que as amostras apresentaram um alto teor de lipídios, impossibilitando a realização desta análise no extrato obtido por hexano.
De acordo com a tabela 3 verifica-se que a cocção ocasionou aumento da IOL. Os processos de extrusão, explosão e torração não ocasionaram alteração destes valores.
Os resultados de fenólicos totais representados na Tabela 1 indicam que os processamentos térmicos utilizados na obtenção destes produtos alteraram a estrutura do grão de amaranto, o que acarretou em maior susceptibilidade destes compostos à oxidação (28). É possível que alguns produtos de oxidação, mesmo permanecendo como compostos fenólicos, não possam ser detectados por esta metodologia (28).
Embora este método seja o mais utilizado para quantificação de compostos fenólicos em alimentos, o reagente Folin-Ciocalteau é capaz de interagir com outros compostos não fenólicos, o que pode resultar em valores superestimados de fenólicos totais (29). O ácido ascórbico presente no grão de amaranto (cerca de 69 mg/100 g) assim como os fenólicos, também reage com Folin-Ciocalteau (30), e pode da mesma forma ter sua estrutura modificada pelo tratamento térmico (31). Outro composto que pode reagir com o Folin-Ciocalteau é a proteína (32), que representa 15% do grão de amaranto.
Klimczak e col. (33) encontraram 39,17 mg de fenólicos totais/100 g no Amaranthus caudatus, enquanto neste estudo foram encontrados 65,93 mg de fenólicos totais/100 g no Amaranthus cruentus. Provavelmente a divergência observada se deve as diferenças entre as espécies e as condições ambientais. Gamel (34) em estudo sobre a influência do tratamento térmico verificou que o conteúdo de fenólicos do A. caudatus e do A. cruentus foi reduzido quando comparado ao grão cru, dados que condizem com este estudo. Porém encontrou menores valores no cozido comparado ao estourado, sendo que o mesmo não ocorreu no presente estudo. Isso provavelmente se deve ao tempo de cozimento do estudo de Gamel (34), mais de quinze minutos.
O teor de fenólicos totais presentes no grão de amaranto é superior ao descrito para aveia, trigo e ervilha (35).
Os valores de IAA dos extratos de hexano indicam que provavelmente os compostos antioxidantes não foram extraídos por este solvente ou, ainda, estes compostos não agiram de forma eficiente a ponto de evitar a oxidação dos lipídios do substrato (gordura vegetal hidrogenada) somados aos lipídios presentes na amostra.
Apesar do IAA do extrato de etanol para as amostras GR, ES, EX, CZ não diferirem entre si, o teor de fenólicos totais (Tabela 1) destas amostras é diferente. Sugere-se que outras substâncias presentes no grão de amaranto, além dos compostos fenólicos, contribuiram para a atividade antioxidante observada (13, 14, 33). A redução dos valores de IAA no TO se deve provavelmente à perda de compostos termolábeis, uma vez que este processamento a seco expõe a amostra a temperaturas elevadas por um período mais prolongado que o ES e EX.
Em relação ao IOL observado após a cocção, supõe-se que o aumento tenha ocorrido devido a uma maior concentração dos compostos com atividade antioxidante, com a solubilização em água de compostos com baixa atuação antioxidante; ou ainda, pode ter ocorrido a formação ou a liberação de compostos não fenólicos que atuam na inibição da oxidação lipídica.
Encontram-se na literatura valores de atividade antioxidante pelo sistema β-caroteno/ácido linoléico para o A. hypocondriacus de 26% (13), para o A. cruentus e A. hybridus de 26 e 25%, respectivamente (33). Nsimba e col. (14) observaram proteção de 66% e 70% da oxidação do β-caroteno ocasionada pelas substâncias presentes nos extratos obtidos por etanol de duas variedades de A. cruentus. Estes valores são mais próximos aos encontrados no presente estudo. A diferença entre os valores reportados pode ser decorrente dos diferentes métodos de extração utilizados, bem como a variedade do grão e as condições climáticas. O critério utilizado para escolher o melhor método e solvente foi aquele que apresentou o maior teor de fenólicos totais e o melhor resultado de atividade antioxidante (21). Foi constatado neste estudo que a maioria dos compostos que apresentam atividade antioxidante são mais solúveis em solventes polares, como o etanol, que em solventes apolares, como o hexano. No trabalho de Ozsoy e col (11) foi constatado que os solventes mais polares (metanol e água) extrairam mais compostos fenólicos e consequentemente apresentaram melhor atividade antioxidante quando comparado com o extrato menos polar (acetato de etila) de Amaranthus lividus.
Apesar da redução do teor de fenólicos ocasionada pelos diferentes processamentos, a atividade antioxidante (IOL) do grão de amaranto praticamente se manteve, assim como ocorreu no IAA. Nsimba e col. (14) observaram que o teor de fenólicos e atividade antioxidante do grão de amaranto tiveram diferentes valores e foram fracamente correlacionados. Outros constituintes poderiam ser responsáveis pela atividade antioxidante deste grão. Polifenóis, antocianinas, flavonóides, tocoferóis, tocotrienóis e vitamina C têm sido associados à atividade antioxidante deste grão (13-17); assim como os compostos gerados na reação de Maillard. Novas investigações visando à identificação e a quantificação destes componentes, bem como a sua estabilidade frente aos processos utilizados para viabilizar o consumo do grão de amaranto devem ser realizadas.
Verifica-se que no teste utilizando o aparelho Rancimat® a atividade antioxidante dos extratos do CZ e do GR foram semelhantes. Estes dois produtos apresentaram os maiores IAA, porém todos os extratos etanólicos demonstraram potencial antioxidante.
O produto CZ apresentou os melhores resultados de atividade antioxidante, tanto para o teste Rancimat®, quanto para o sistema β-caroteno/ácido linoléico. Porém, a ordem de grandeza da atividade antioxidante dos demais produtos não foi semelhante comparando-se estes dois testes. Vale ressaltar a importância de se utilizar vários métodos para avaliar a capacidade antioxidante de um alimento, pois cada teste avalia um mecanismo diferente de proteção. A atividade antioxidante do grão de amaranto também foi constadada através do uso de outros métodos, como por exemplo, o DPPH (1,1-difenil-2-picrilhidrazil) e o FRAP (poder antioxidante de redução do ferro) (14,17).
Os resultados obtidos neste trabalho em ambos os testes indicam a elevada atividade antioxidante do extrato obtido por etanol do grão de amaranto cru e de seus produtos.
Todos os processamentos reduziram o teor de fenólicos totais. Porém, os processos de explosão, torração e extrusão do grão de amaranto não reduziram a atividade inibitória da oxidação quando comparados ao grão cru através do ensaio do β-caroteno/ácido linoléico. No ensaio com aparelho Rancimat® observou-se que apenas a torração ocasionou menor inibição da oxidação em relação à matéria-prima.
O grão de amaranto tanto cru como processado apresenta potencial antioxidante. Polifenóis, antocianinas, flavonóides, tocoferóis, vitamina C, assim como os compostos gerados na reação de Maillard podem estar associados à atividade antioxidante deste grão.
Recibido: 26-08-2008
Aceptado: 11-08-2009