Con la finalidad de evaluar la variabilidad en la concentración de algunos metabolitos secundarios en el grano de diferentes híbridos de sorgo (Sorghum bicolor (L) Moench), y aportar información para su uso más racional en alimentos para animales, se colectaron muestras representativas de 12 híbridos (Criollo 1, Criollo 27, Chaguaramas III, Chaguaramas VII, Cristiani Burkard H-8046-2, Guanipa 95, Himeca 101, Himeca 400, Pioneer 81-G67, Pioneer 83-G88, Pioneer 86-P42 y Tecsem 120) sembrados durante el ciclo 2008 en el área de influencia del municipio Turén, edo. Portuguesa-Venezuela. Aplicando métodos analíticos normalizados, los materiales mostraron contenidos de compuestos fenólicos (0,92 ±0,37% Eat), taninos totales (0,61 ±0,29% Eat) y condensados (0,95± 0,65% ELeu), fósforo fítico (0,17 ± 0,03%) y actividad de fitasas intrínseca (12,3 ± 6,74 U/kg) ubicados dentro de los valores promedio citados en la literatura, resaltando una importante variación que debe ser considerada al determinar los niveles de inclusión de este cereal en la formulación de raciones balanceadas para especies de interés zootécnico, así como tomarse en cuenta en los programas de mejoramiento genético de este cultivo.
Palabras clave: Taninos, fósforo fítico, fitasas, Sorghum bicolor.
In order to evaluate the variability in concentration of secondary metabolites among grains from different sorghum hybrids (Sorghum bicolor (L) Moench) and provide some information for rational use in animal feeds, grain samples were collected from 12 hybrids (Criollo 1, Criollo 27, Chaguaramas III, Chaguaramas VII, Cristiani Burkard H-8046-2, Guanipa 95, Himeca 101, Himeca 400, Pioneer 81-G67, Pioneer 83-G88, Pioneer 86-P42 y Tecsem 120) sowed on 2008 in the Turén municipality, Portuguesa State-Venezuela. Using standardized analytical methods, hybrids showed polyphenolics compounds contents (0.92 ± 0.37% TaE), total (0.61 ± 0.29% TaE) and condensed tannins (0.95 ± 0.65% LeuE), phytic phosphorus (0.17 ± 0.03%) and intrinsic phytase activity (12.3 ± 6.74 U/kg) in the ranges described in the literature, with an important variation among hybrids that must be considered for their inclusion levels in the formulation of balanced feeds, as well as plant breeding programs.
Key words: Tannins, phytic phosphorus, phytase activity, Sorghum bicolor.
Facultad de Agronomía, Universidad Central de Venezuela. Maracay, INIA-Araure Edo. Portuguesa, INIA- CENIAP, Edo. Aragua, Universidad Rómulo Gallegos, Area Agronomía, Edo. Guárico, Venezuela
Para el año 2007, en Venezuela se sembraron unas 267000 ha de sorgo granífero (Sorghum bicolor (L) Moench), las cuales generaron 563350 t de cereal, equivalentes a 2110 kg/ha (1). A nivel nacional, esto representa el 30,8% de la superficie dedicada a la siembra de cereales, lo cual resalta la importancia relativa de este cultivo para la seguridad agroalimentaria del país.
El grano de sorgo producido a nivel nacional, con la particularidad de ser mayoritariamente de testa de color pardo, se emplea exclusivamente en la industria de alimentos balanceados para animales, fundamentalmente a la formulación de raciones para aves y cerdos, aunque no se descarta su uso potencial en la alimentación humana, tal como ocurre en comunidades de África y Asia, y en menor grado, en América Latina. Como materia prima, aunque su perfil nutricional puede ser equivalente al de otros cereales de uso tradicional y mostrar la ventaja de resistencia a condiciones agroclimáticas adversas, presenta como limitantes nutricionales un bajo contenido de pigmentos carotenoides y la presencia de metabolitos secundarios, donde destacan los taninos condensados y fitatos; entre otros (2,3).
Los taninos condensados (polímeros de catequina o proantocianidinas) se asocian a efectos detrimentales sobre el consumo, digestibilidad de la proteína, materia seca y fracciones minerales, entre otros (4-8); mientras que la presencia de complejos insolubles en ácido fítico ó fitatos (ácido myo-inositol hexafosfórico), si bien constituyen un mecanismo de garantía de almacén de fósforo a la planta, se señalan como responsables de la pobre utilización del 50 a 80 % del fósforo total presente en los granos de cereales (3). Si bien la actividad enzimática de fosfatasas ácidas, como las fitasas, puede potencialmente liberar el fósforo insoluble a partir de estos complejos, para la mayoría de los cereales se reportan valores marginales en la actividad intrínseca de estas enzimas, con la consecuente baja biodisponibilidad de fósforo y otros elementos minerales (cationes), reducción en la digestibilidad de la proteína a consecuencia de la formación de complejos con la molécula de fitato y un negativo impacto ambiental derivado de una elevada concentración de este mineral en las heces; entre otros (3, 9-12).
Con la finalidad de estudiar la variabilidad en la concentración de algunos metabolitos secundarios en el grano de sorgo, y aportar así información para un uso más racional de este cereal en la alimentación animal y humana, el presente trabajo evaluó el contenido de compuestos fenólicos, taninos totales y condensados, fitatos y actividad intrínseca de fitasas en 12 híbridos de sorgo de amplia difusión a nivel nacional.
Para la realización del presente estudio se consideraron siembras comerciales ubicadas en cinco unidades de producción localizadas en el área de influencia del municipio Turén (09º 20’ 03’’ latitud norte y 69º 07’ 21’’ longitud oeste) del edo. Portuguesa, Venezuela. Este municipio se ubica a una altura de 275 m.s.n.m, con una media anual de 27ºC, 1395 mm de precipitación, 1975 mm de evaporación y 4,3 meses secos (13,14).
Se evaluaron los híbridos Criollo 1, Criollo 27, Chaguaramas III, Chaguaramas VII, Cristiani Burkard H-8046-2, Guanipa 95, Himeca 101, Himeca 400, Pioneer 81-G67, Pioneer 83-G88, Pioneer 86-P42 y Tecsem 120. Éstos fueron sembrados en el ciclo 2008 en condiciones de norte-verano en suelos predominantemente franco-arenosos, con un área de siembra para cada híbrido de 10-40 ha, densidad de 166000 a 222000 plantas/ha, fertilización al momento de la siembra con 150-200 kg/ha de 20-10-20 (N-P-K) y reabono 25 días después con 100-150 kg urea/ha. Este manejo agronómico permitió un rendimiento de 2885 ± 787,9 kg/ha, en híbridos con un ciclo de 90-110 días.
Al momento de la cosecha se tomaron muestras representativas del grano (4 kg/híbrido), las cuales fueron deshidratadas a temperatura ambiente, en un local ventilado y oscuro, hasta la obtención de peso constante, siendo posteriormente molidas en criba de 1mm de diámetro. Para la evaluación de compuestos fenólicos, una fracción de las muestras deshidratadas fue molida en criba 0,25 mm de diámetro, para luego ser conservadas en envases de color ámbar a los fines evitar el deterioro de dichos compuestos por efecto de la incidencia de la luz.
Los contenidos de materia seca a 105ºC, cenizas, proteína cruda y extracto etéreo, se evaluaron según lo descrito por la AOAC (15). La determinación de fibra insoluble en detergente neutro (FDN) se efectuó de acuerdo a la metodología descrita por Van Soest et al. (16), con la adición de sulfito de sodio a la solución de detergente neutro para remover parcialmente los complejos taninos-proteína (17). Las fracciones de calcio y fósforo fueron evaluadas por espectrofotometría de absorción atómica de acuerdo a metodología reportada por Fick et al. (18) y Fiske y Subbarow (19); respectivamente.
Para difundir los compuestos fenólicos a una fase líquida (20), 200 mg de la muestra molida se colocaron en un frasco y se les adicionó 10 ml de una solución solvente de acetona/agua destilada (70% v/v), para luego de ser tratada con ultrasonido durante 20 min, determinar el contenido total de fenoles y taninos extractables presentes en la solución por el Método de Folin-Ciocalteu (21), expresando el resultado como equivalentes de ácido tánico (Eat). Los taninos condensados extractables ó proantocianidinas extractables se cuantificaron por el método de Butanol-HCL -36%- en relación 95:5 v/v (22), reportando los resultados como equivalentes de leucocianidinas (ELeu).
Paralelamente, se tomaron 2 g de cada muestra molida con criba de 1mm y se colocaron en un frasco al que se adicionó 100 ml de una solución extractora (1,2% HCl + 10% Na2SO4). Luego de 2 h de agitación mecánica, el extracto se filtró al vacío empleando papel Whatman Nº 54 y 10 ml del filtrado fueron procesados para determinar la concentración de fósforo fítico de acuerdo a la metodología descrita por Early y Turk (23), considerando las modificaciones propuestas por Thompson y Erdman (24). La actividad de fitasas intrínseca fue medida de acuerdo al procedimiento descrito por Bitar y Reinhold (25), tomando como base la solución obtenida por centrifugación (20G x 30 min) del extracto generado por la dilución de 1 g de muestra en tampón tris-HCL, 0,02M a pH 7,5. Bajo estas condiciones, una unidad de fitasa (U) fue descrita como la cantidad de fósforo inorgánico liberado por minuto, a partir de 5 mM de una solución de fitato de sodio a 37 ºC y pH de 5,5.
Las variables químicas estudiadas se analizaron mediante estadística descriptiva, calculándose la desviación estándar para cada valor promedio. El grado de asociación entre variables se caracterizó a través de correlaciones lineales simples - Pearson- y regresiones lineales múltiples. Por medio de estadística multivariada, se formaron cluster considerando como criterio de agregación las coordenadas factoriales, obteniendo así grupos homogéneos en cuanto a la participación relativa de los metabolitos secundarios en estudio (26,27).
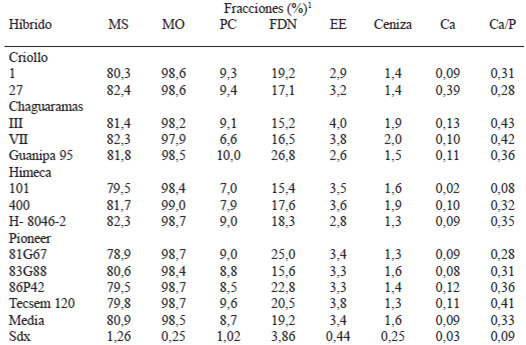
En la Tabla 1 se presenta la composición bromatológica y FDN de los granos de los diferentes híbridos de sorgo considerados en este estudio. La proteína cruda (8,7 ± 1,02%) presentó valores en un rango de 6,6 a 10,0%, donde los granos de los híbridos Criollo (1 y 27), Chaguaramas III, Guanipa 95, Himeca (8046-2), Pioneer (81G67) y Tecsem 120 se mostraron superiores, con un registro promedio de 9,34 ± 0,36%. En lo referente al contenido de carbohidratos estructurales, la FDN presentó un valor medio de 19,2 ± 3,86%, resaltando con los mayores valores Guanipa 95 y Pioneer (81G67 y 86P42), quienes en su conjunto presentaron un registro de 24,9 ± 2,00%.
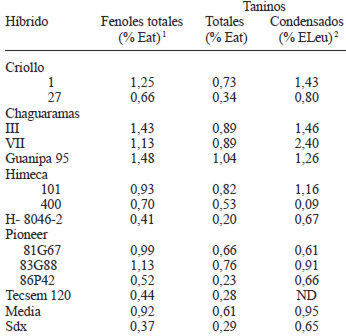
Tal como se observa en la Tabla 2, los híbridos considerados presentaron un contenido de fenoles totales de 0,92 ±0,37 % Eat. Dentro de este grupo químico, se hallan compuestos de variable nivel de toxicidad como los ácidos benzoicos y cinámicos, cumarinas, quinonas, benzofenonas, flavonoides y taninos; entre otros. En los híbridos bajo estudio, los taninos totales extractables (hidrosolubes y condensados) presentaron una concentración de 0,61 ±0,29% Eat, representando el 65,6 ±12,8 % de los compuestos fenólicos presentes. Los taninos condensados mostraron una media de 0,95 ±0,65 % ELeu, con valores que en promedio ascendieron a 1,54 ± 0,49 % ELeu en los híbridos Chaguaramas (III y VII), Guanipa 95, Criollo 1 y Himeca 101; destacando la ausencia de estos compuestos polifenólicos en el híbrido Tecsem 120.
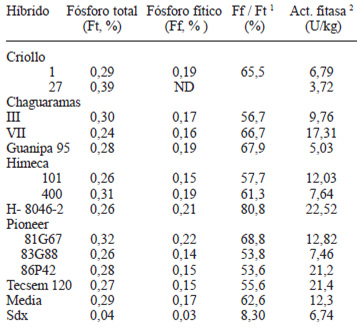
Los contenidos de fósforo total, fósforo fítico y actividad intrínseca de fitasa se presentan en la Tabla 3. La concentración de fósforo fítico (0,17 ±0,03%) muestra poca variación relativa entre híbridos, destacando la ausencia de este metabolito secundario en el híbrido Criollo 27. Para los restantes híbridos evaluados, un 62,6 ±8,3 % del fósforo total se halla indisponible por estar en forma de sales de ácido fítico, o como se conoce comúnmente, en la forma de fósforo fítico. De acuerdo al criterio empleado en la literatura (28), los híbridos evaluados no muestran actividad significativa de fitasa intrínseca por presentar un valor inferior a 100 U/kg.
Los valores promedio para la composición bromatológica de los granos de sorgo de los híbridos evaluados son similares a los reportados para este cereal por tablas internacionales de composición química de alimentos (29-31). Sin embargo, resalta la variabilidad mostrada entre híbridos para las fracciones de de proteína cruda, FDN y extracto etéreo, lo que sugiere un amplio margen para la selección genética en función a estos parámetros.
En el caso particular del FDN, la variación en su contenido se puede asociar a una mayor participación relativa de la testa en la estructura del grano de algunos híbridos; mientras que a pesar de la relativa uniformidad en la concentración de fracciones grasas (3,35 ± 0,43 %), es bueno acotar que los híbridos Criollo 1, Guanipa 95 e Himeca (8046-2) presentaron como media un 20,9 % menos de extracto etéreo, lo cual debe considerarse a la hora de valorar su aporte energético y como fuente de ácidos grasos.
Si bien los valores promedio de calcio y fósforo se ajustan a lo reportado para este cereal, presentan un rango para la relación Ca:P (0,08 a 0,41) distante del valor de 2:1 señalado como deseable en virtud de ser similar a lo encontrado en el tejido óseo (29), por lo que este indicador debe ser considerado por su impacto nutricional y económico en el diseño de raciones balanceadas.
Los taninos totales extractables (hidrosolubes y condensados) presentaron valores superiores al 0,3% considerado por la Comunidad Europea como máximo tolerable para incorporación de este cereal en raciones para aves y cerdos (31). A pesar de la ventaja agronómica de la presencia de taninos en el sorgo (resistencia al ataque de insectos, pájaros y enfermedades de origen fúngico), actualmente está suficientemente documentado en animales y seres humanos, que niveles de ácido tánico dietario superiores a 2,0% se asocian con reducción del consumo voluntario y retención de nitrógeno, disminución en la absorción de minerales (fundamentalmente P, Fe, Ca, Mg, Na y K), baja eficiencia de uso de metionina, marcado incremento de la actividad proteolítica del hígado, alteración de la respuesta inmune y trastornos locomotores; entre otros (32,33,34,38).
Aunque en términos relativos el contenido de fósforo fítico se ubica dentro del rango de 61 a 76 % del fósforo total reportado en la literatura para este cereal (3,10,35), es relevante destacar que en el caso del híbrido Criollo 27 la biodisponibilidad de fósforo en su grano no se halla limitada por la presencia de estos metabolitos secundarios, mientras que el elevado contenido de fósforo fítico en H-8046-2 (80,8%) debe considerarse al momento de la formulación de raciones que incluyan granos procedentes de este híbrido.
Aun considerando la nula actividad de fitasa intrínseca, el valor promedio obtenido (12,3 ± 6,74 U/kg) representa aproximadamente el 50% de lo reportado por varios autores (3,10,28), lo que sugiere la existencia de diversidad asociada a los genotipos en consideración. La suplementación con fósforo disponible y otros nutrientes (vitamina D y ácidos orgánicos), incorporación de materias primas con elevada actividad intrínseca de fitasas (como trigo y sus subproductos), el granulado de la dieta, fraccionamiento físico del grano y la adición de fuentes exógenas de fitasas, son estrategias que han sido empleadas con variable éxito en la reducción del efecto antinutricional de las sales de ácido fítico (10,36,37). Aunque comúnmente se reconoce el efecto antinutricional del fósforo fítico, no obstante es bueno acotar que se han demostrado sus propiedades antiinflamatoria y antitumoral debido a su capacidad para inhibir la proliferación celular y la angiogénesis, inducir la apoptosis o muerte celular programada, así como su capacidad para regular la expresión de determinados oncogenes in vitro (37).
El contenido promedio de fenoles totales mostró correlación con el de taninos totales (P<0,001; r2= 0,94) y taninos condensados (P<0,05; r2= 0,67), indicando para este cereal la importancia de la fracción taninos dentro de los compuestos fenólicos presentes. Así mismo, llama la atención la correlación entre la actividad de fitasa intrínseca y el contenido de fenoles totales (P<0,05; r2= -0,61), lo cual puede ser un factor a tomar en cuenta en programas de mejoramiento genético del cultivo. Considerando la actividad de fitasas, se obtiene una ecuación de regresión que permite demostrar la asociación de esta variable con el contenido de fósforo total (P) y fenoles totales (FenT) de acuerdo a:
Activ. Fitasa= 53,2 – 103,05P – 12,16FenT (P<0,01; r2= 0,74)
El contenido de metabolitos secundarios en los híbridos evaluados permitió la formación de tres clúster homogéneos, identificados como A (Criollo 1, Chaguaramas III, Chaguaramas VII, Guanipa 95, Himeca 101 y Pioner 83G88), B (Criollo 27) y C (Himeca 400, H- 8046-2, Pioneer 81G67, Pioneer 86P42 y Tecsem 120). Los híbridos del grupo A presentan mayor contenido de fenoles totales (1,23 ± 0,19% Eat), taninos totales (0,86 ± 0,1% Eat) y taninos condensados (1,44 ± 0,47% ELeu). Al comparar los híbridos del grupo A con los del grupo C, los primeros presentan una menor concentración de fósforo fítico (0,17 ± 0,02%), actividad intrínseca de fitasa (9,73 ± 4,1 U/kg) y fósforo total en forma de fósforo fítico (61,4 ±5,5%); mientras que en B se evidencian registros marginales en dichas variables.
Se concluye que los híbridos de sorgo evaluados muestran contenidos de compuestos fenólicos (0,92 ± 0,37%), taninos totales (0,61 ± 0,29%) y condensados (0,95 ± 0,65%), fitatos (0,17 ± 0,03%) y actividad de fitasas (12,3 ± 6,74 U/kg) ubicados dentro de los rangos citados en la literatura. El potencial impacto antinutricional de los metabolitos secundarios evaluados, unido a la variación exhibida entre los híbridos considerados y los niveles de tolerancia diferencial entre especies animales, deben ser factores a considerar al momento de determinar los niveles de inclusión de este cereal en la formulación de raciones, configurando de este modo una variable de interés en los programas de mejoramiento genético de este cultivo.
Los autores agradecen al Consejo de Desarrollo Científico y Humanístico de la Universidad Central de Venezuela por el respaldo financiero para la realización de este estudio (CDCH PI 01-10-5471-2004), así como al Laboratorio de Nutrición Animal del INIA-Maracay por su apoyo en la determinación de fósforo fítico y actividad de fitasas intrínseca.
Recibido: 13-08-2009
Aceptado: 21-11-2009