O presente trabalho tem como objetivo avaliar a excreção urinária de iodo e relacionar com a sua quantidade presente no sal de consumo humano. Participaram do estudo 145 crianças de duas escolas: uma de zona rural e outra de urbana. Foram realizadas avaliação antropométrica e coleta de amostra de urina e do sal de cozinha cada uma das crianças voluntárias. Na escola rural, 3,8% das crianças apresentaram deficiência de iodo. Entretanto, a maioria dos valores de iodúria ficou acima de 300μg/L (62,03%) com 59,49% das amostras do sal de cozinha entre 20 e 60mg de iodo por quilo de sal. Para a escola urbana, 3,03% das crianças apresentaram iodúria inferior à 100μg/L, sendo que, 90,91% das crianças apresentaram valores de iodúria superior a 300μg/L. Desse total, 84,85% das amostras do sal de cozinha encontrava-se entre 20 e 60mg de iodo por quilo de sal. A deficiência de iodo na população estudada está controlada, destacando-se agora uma nova realidade de alta prevalência de excesso de iodo urinário.
Palavras chave: Iodúria, sal e crianças.
The objective of the present study was to evaluate the urinary excretion of iodine and relate it to the amount present in salt for human consumption. The study involved 145 children from two schools: a rural one and an urban one. We performed anthropometric measurements and collected a urine sample and a kitchen salt sample from each child. In the rural school, 3.38% of children had iodine deficiency. However, most of the values of urinary iodine were above 300 μg/L (62.03%) and 59.49% of the kitchen salt samples contained 20 to 60 mg iodine per kilo of salt. In the urban school, 3.03% of the children had urinary iodine excretion of less than 100 μg/L and 90.91% of the children had urinary iodine values exceeding 300 μg/L. Of this total, 84.85% of the kitchen salt samples contained 20 to 60 mg iodine per kilo of salt. Iodine deficiency is controlled in this population, with the current reality showing a high prevalence of excess urinary iodine.
Key words: Urinary iodine, salt, children.
Departamento de Clínica Médica, Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo, Ribeirão Preto -São Paulo. Brasil
O iodo é um nutriente essencial, amplamente encontrado na natureza, especialmente na água dos oceanos (1), entretanto, se distribui de forma irregular sobre a superfície terrestre. Sua principal função no corpo humano é a participação na síntese dos hormônios da tiróide. Desta maneira, o iodo tem influência importante no organismo como um todo através de sua participação nos processos metabólicos (2).
Geralmente a ingestão inadequada de iodo está associada à ocorrência de um grupo de situações clínicas denominadas Desordens por Deficiência de Iodo ou, em inglês, Iodine Deficiency Disorders – IDD. A forma de correção dessas carências é a fortificação de alimentos de uso massivo. Atualmente, a estratégia usual para garantir a suficiência de iodo no Brasil é a fortificação do sal de cozinha, já que os alimentos naturais não garantem uma ingestão adequada de iodo.
A forma mais utilizada para verificar e monitorar a adequação da ingestão desse nutriente é a iodúria, pois a sua ingestão de iodo correlaciona-se diretamente com a sua excreção urinária (3). Portanto, a iodúria é um importante marcador para avaliação da suficiência de iodo. Desta forma, o presente trabalho tem como objetivo avaliar a excreção urinária de iodo e relacionar com a sua quantidade presente no sal de consumo humano.
O trabalho foi realizado em duas escolas de Botucatu-SP (Rural e Urbana), selecionadas pela facilidade de acesso e consentimento de participação. Foram incluídas crianças e adolescentes, saudáveis, sem diagnóstico de distúrbios renais ou qualquer alteração patológica de ambos os gêneros, com idades entre 6 e 12 anos. Participaram 79 estudantes da escola rural e 66 estudantes de uma escola urbana, totalizando 145 crianças e adolescentes. Para a participação voluntária foram incluídas apenas as crianças que os pais autorizaram depois de assinarem um termo de consentimento livre e esclarecido aprovado pelo comitê de ética em pesquisa do HCFMRP - USP e FMRP-USP (processo número 12466/2004).
Com o objetivo de caracterizar o estado nutricional das crianças voluntárias foi realizada uma avaliação antropométrica. Todas as medidas foram realizadas pelo mesmo pesquisador, após padronização dos equipamentos e procedimentos a serem utilizados de acordo com as técnicas descritas por Gordon et al (4). As medidas foram realizadas nas próprias escolas, de acordo com a disponibilidade de cada uma delas, e após consentimento anteriormente informado autorizado pelo responsável do escolar.
As variáveis do estado nutricional utilizadas foram: peso, estatura, idade e sexo. Os indicadores do estado nutricional foram: peso para idade (PI), estatura para idade (E/I) e índice de massa corporal para idade (IMC/I). Os pontos de corte adotados foram os definidos pela WHO (5). Para os cálculos dos valores de escore z, utilizou-se o software Epiinfo, versão 3.2, 2004, segundo os valores de referência do CDC/NCHS (6).
Foram coletadas uma amostra casual de urina e uma de sal de cozinha utilizada no domicílio de cada criança voluntária.
Para a dosagem de iodo na urina foi utilizada a reação Sandell & Kalthoff (7,8), substituindo o ácido clórico por persulfato de amônia (9).
A amostra foi tratada com persulfato de amônia sob condições médias de aquecimento e o iodeto foi determinado pelo seu papel catalítico na redução do íon cérico (Ce4+) para íon cério (Ce3+), acoplada à oxidação do íon arsenioso (As3+) para íon arsênico (As5+). O íon cérico (Ce4+) tem cor amarela, enquanto o íon cério (Ce3+) é incolor. Assim, o curso da reação pode ser seguido pelo desaparecimento da cor amarelada à medida que o íon cérico é reduzido. Mantidos os demais reagentes estáveis, a velocidade do desaparecimento da cor na reação é diretamente proporcional à quantidade de iodo que está catalisando.
A análise de iodo no sal de consumo humano foi realizada de acordo com a técnica recomendada pelo Ministério da Saúde (10). Em presença de iodeto de potássio (KI) e em meio ácido, o iodato de potássio (KIO3) reage liberando iodo, que é imediatamente titulado com tiosulfato de sódio, usandose solução de amido como indicador.
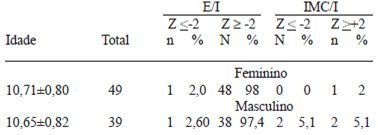
Os dados antropométricos estão apresentadas nas Tabelas 1, 2 e 3 sendo separados por escola, faixa etária, sexo, medida antropométrica e valores de escore Z para os diferentes indicadores antropométricos.
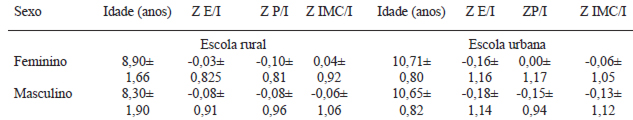

A Tabela 4 representa a associação entre iodúria e iodo adicionado ao sal de uso doméstico para as crianças que estudavam na Escola Rural.
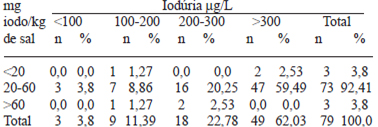
Pôde ser observado que 3,8% das amostras de iodúria e iodo no sal se encontravam abaixo de 100μg/L e 3,8% entre 20 a 60mg de iodo/kg de sal de cozinha. Para iodúria de 100 a 200μg/L, a porcentagem encontrada foi de 11,39%, sendo que 1,27% apresentou menos de 20mg de iodo/kg de sal, 8,86% entre 20 e 60mg de iodo/kg e 1,27% acima de 60mg/kg. Para as concentrações de 200 a 300μg/L, obteve-se 22,78% do total, sendo que 20,25% com valores de iodo no sal de cozinha entre 20 e 60mg/kg de sal e 2,53% acima de 60mg/kg. A maioria das amostras (62,03%) apresentava iodúria acima de 300μg/L. Do total dessa maioria, 2,53% estavam com valores de iodo no sal de cozinha inferior a 20mg/kg e 59,49% entre 20 e 60mg/kg de sal.
A Tabela 5 representa a associação entre os valores de iodúria e iodo adicionado ao sal de uso doméstico, para as crianças que estudavam na Escola Urbana.

Foi observado que 3,03% das amostras de iodúria e iodo no sal se encontravam abaixo de 100μg/L e de 20mg de iodo/kg de sal de cozinha; para iodúria de 100 a 200μg/L não foram encontrados resultados. Para as amostras com concentrações de 200 a 300μg/L, 6,06% apresentou valores entre 20 e 60mg de iodo/kg de sal. A grande maioria das amostras de iodúria, 90,91%, teve concentrações acima de 300μg/L, sendo que 6,06% delas com valores de iodo no sal de cozinha abaixo de 20mg/kg de sal e 84,85% entre 20 e 60mg de iodo/kg.
Assim como encontrado em outros países em desenvolvimento, como por exemplo mostra Ovelar e colaboradores em estudo realizado em 2006 no Paraguai (11), o Brasil também tem apresentado profundas modificações no perfil nutricional de sua população, fruto de um processo conhecido como transição nutricional (12-14).
Tal situação pôde ser documentada por inquéritos domiciliares nacionais ou regionais realizados entre os períodos de 1975-1997 e outro realizado mais recentemente entre 2002 e 2003, cujos dados evidenciam uma clara tendência de diminuição da desnutrição em todo o país, mas em intensidades diferentes dependendo da região e do estrato social (15).
Em relação a estes dados antropométricos encontrou-se em geral situações diferentes entre as duas escolas (rural e urbana), mas que em conjunto colaboram para estas estatísticas. Para os escolares rurais, considerando o sexo masculino, pôde ser evidenciado uma prevalência de 7,7% de crianças com baixo peso e 2,6% com obesidade. Na escola urbana 5,1% apresentavam baixo peso, 7,1% obesidade. Estes dados comprovam os achados do IBGE (15) onde o baixo peso é maior em zonas rurais em relação às urbanas.
A prevalência de sobrepeso e obesidade vem aumentando também nos países em desenvolvimento, onde as deficiências nutricionais e doenças infecciosas desempenhavam um papel central nesse quadro e, hoje predominam as doenças cardiovasculares e outras doenças crônico-não transmissíveis, em função das mudanças no estilo de vida acompanhadas de alteração na estrutura da dieta e na composição corporal dos indivíduos (15, 14,16). Entre menores de cinco anos, além da tendência declinante de subnutrição, destacam-se prevalências relativamente baixas e estáveis de sobrepeso e obesidade, situando-se em torno de 5% (16). Em contraposição, em crianças de 6 a 10 anos e nos adolescentes pode-se considerar que o sobrepeso é a alteração nutricional em ascensão. De acordo com Wang et al. (17), a prevalência de sobrepeso aumentou de 4,9 para 17,4% entre crianças de 6 a 9 anos e de 3,7 para 12,6% nos jovens entre 10-18 anos nas ultimas décadas (18, 5). Resultados semelhantes foram evidenciados nesse estudo que também estão em concordância com os dados do IBGE (15).
Considerando a suficiência ou não de iodo, o quarto inquérito nacional da excreção urinária de iodo, realizado de Norte a Sul do Brasil, revelou que 86,5% dos escolares apresentavam excreção urinária acima de 300μg/L (19, 20), mostrando que a prevalência de deficiência de iodo e bócio no Brasil se encontram dentro das metas recomendadas pela Organização Mundial da Saúde.
Duarte et al. (21), avaliando o estado nutricional de escolares no estado de São Paulo, encontrou 53% das crianças com excreção urinária de iodo acima de 300 μg/L. Em nosso trabalho encontramos 62,03% das crianças da escola rural e 90,91% da escola urbana com valores de iodúria acima de 300 μg/L, valores estes acima da média do estado como demonstrado por Duarte (21).
Silva e Munasinghe (22), avaliando excreção urinária de iodo em adolescentes do sexo feminino e gestantes encontrou, respectivamente, uma variação de 51,9 a 1395,6 μg/L e 13,6 a 785,6μg/L e, 56% das adolescentes e 39% das gestantes apresentavam valores superiores a 300 μg/L, sugerindo o risco aumentado principalmente para as adolescentes de hipertiroidismo induzido por iodo e a necessidade de avaliação do programa de fortificação do sal. O sal como veículo de iodo é o principal recurso utilizado no mundo para a erradicação das DDI, devendo ser utilizado de forma adequada e cautelosa (23).
No presente estudo as quantidades de iodo utilizadas na fortificação do sal estava adequada na maioria das amostras não havendo, portanto evidência de adulteração da legislação, que preconizava a adição de 20 a 60 mg de iodo/kg de sal. Estudos recentes tem discutido a necessidade de alteração desta legislação para maior controle da suficiência de iodo, evitando assim sua insuficiência ou excesso (24).
Apesar de encontrarmos vários estudos indicando o excesso de excreção urinária de iodo (25,26,23,27), sua deficiência ainda persiste em várias regiões do mundo (28,23,29,30-34), ou em alguns grupos populacionais como, por exemplo, em vegetarianos e gestantes (35,36).
Portanto, a prevalência da deficiência de iodo na população estudada encontra-se em conformidade com a estabelecida pela Organização Mundial de Saúde. Destacando-se ainda uma nova realidade de alta prevalência de excesso de iodo urinário.
Recibido: 09-08-2010
Aceptado: 27-10-2010