Se evaluó la bioaccesibilidad de diversos minerales en infusiones de yerba mate y en preparaciones con leche fortificada con Fe para determinar la influencia de las infusiones en la biodisponibilidad potencial de minerales intrínsecos y del Fe de fortificación. Se evaluó la dializabilidad (D) de hierro, calcio, magnesio y zinc, como indicador de la bioaccesibilidad, en muestras de leche fortificada con sulfato ferroso (SF), bisglicinato férrico (BGF) y EDTANaFe. También se evaluó en mezclas de leche con mate cocido y en infusiones-cocciones con leches fortificadas. En cada caso se estudió la acción del ácido ascórbico (AA) en una relación Fe:AA 1:4. En el mate cocido la DFe fue nula y aumentó a 15% con el agregado de AA. La DFe en leche con SF, BGF y EDTANaFe (1.2; 1.0 y 27.4 respectivamente), se incrementó con el agregado de AA a 2.9; 3.5 y 24.8. La DFe en la mezcla leche:mate cocido resultó 4.7%; 5.7% y 31.2% para SF, BGF y EDTANaFe respectivamente. Con el agregado de AA resultó de 13.5%; 13.7% y 25.7% En infusionescocciones en leche fortificada con SF, los valores resultaron menores a los de la mezcla. La DCa no presentó variaciones importantes en las leches fortificadas y sus preparaciones con yerba mate, mientras que la DMg y la DZn solo mostraron una disminución significativa en la infusión-cocción. El consumo de infusiones de yerba mate no aporta cantidades significativas de minerales. Sin embargo, su consumo en mezclas con leche no afectaría negativamente la disponibilidad de Fe en dicha matriz.
Palabras clave: Yerba mate, dializabilidad de minerales, fortificación
The bioaccesibility of various minerals in infusions of yerba mate (mate cocido) and preparations with Fe-fortified milk was assessed to determine the influence of the infusions on the potential bioavailability of intrinsic minerals and fortified Fe. The dialyzability (D) of iron, calcium, magnesium and zinc was evaluated, as indicator of bioaccesibility in milk samples fortified with ferrous sulfate (FS), ferric bisglicinate GF) and EDTANaFe. Dialyzability was also evaluated in mixtures of milk with mate cocido and in infusions cooked with Fe-fortified milk. In each case the effect of ascorbic acid (AA) in a ratio Fe: AA 1:4 was studied. In the mate cocido FeD was zero and increased to 15% with the addition of AA. The FeD in milk with SF, BGF and EDTANaFe (1.2, 1.0 and 27.4 respectively), increased with the addition of AA to 2.9, 3.5 and 24.8. The FeD in the mixture milk: mate cocido was 4.7%, 5.7% and 31.2% for SF, BGF and EDTANaFe respectively. With the addition of AA was 13.5%, 13.7% and 25.7%. In infusions cooked with SF fortified milk, the values were lower than those of the mixture. The CaD did not show significant changes in Fe fortified milk and its preparations with yerba mate, while the MgD and ZnD only showed a significant reduction in infusion cooked with Fe-fortified milk. The use of infusions of yerba mate does not provide significant amounts of minerals. However, its use in mixtures with milk will not adversely affect the availability of Fe in that matrix.
Key words: Mineral dializabilitaty, fortification, mate infusions.
Cátedra de Bromatología. Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires, Argentina
La yerba mate (Ilex paraguariensis St) es una planta importante que crece naturalmente en Sud América y es cultivada en el NE de Argentina, SE de Brasil y E de Paraguay. Sus hojas son utilizadas para un tipo de infusión llamada mate, muy similar a un té. Tal infusión recibe el nombre de mate cocido. Además de su consumo como tal, es muy habitual tomarla en un recipiente con una bombilla metálica. En este caso se colocan aproximadamente 50 g de yerba mate en dicho recipiente y se sirven sobre ella porciones de agua caliente (1).
Esta infusión está ingresando rápidamente en el mercado de Estados Unidos y en la Comunidad Europea aumentando paulatinamente su consumo (2). Por tal motivo diversos investigadores han estudiado su composición, los efectos fisiológicos y sus potenciales usos en la salud (3).
Ya desde 1990 científicos españoles comenzaron a estudiar la composición mineral de esta hierba y encontraron que era capaz de aportar cantidades apreciables de varios minerales, entre ellos Mg, Fe, Zn y K (4). También existen estudios sobre la cantidad de estos minerales que era extraída con el agua. Según tales resultados se podía inferir que las infusiones realizadas con yerba mate aportaban una buena cantidad de minerales (5).
Sin embargo, no se han realizado estudios sobre la biodisponibilidad de los minerales que contiene. Tal evaluación resulta de interés ya que si bien la yerba mate es rica en ácido ascórbico, conocido promotor de la biodisponibilidad de Fe, durante el procesado de las hojas la mayoría de éste se pierde (6). Además contiene valores altos de polifenoles, importantes inhibidores de la absorción de Fe y Zn. (1). Es común que esta infusión se ingiera mezclada con leche y además existe en nuestro país una importante variedad de leches fortificadas con Fe.
El objetivo del presente trabajo fue evaluar la influencia sobre la bioaccesibilidad de minerales del consumo conjunto de infusiones de yerba mate y leche fortificada
Se eligieron tres fuentes de Fe de fortificación diferentes. El sulfato ferroso, que es una de las fuentes mas comúnmente usadas en la fortificación de alimentos, por su buena biodisponibilidad en ausencia de inhibidores de la absorción. El bisglicinato ferroso que es un quelato de aminoácidos con Fe, que posee buena biodisponibilidad y no posee las cualidades prooxidantes del sulfato ferroso (7). El NaFeEDTA que es un quelato de alta biodisponibilidad, especialmente útil en el caso de dietas con importantes cantidades de inhibidores de la absorción del hierro.
Además, en la actualidad existen empresas elaboradoras de productos como mate cocido en polvo soluble que añaden ácido ascórbico como parte de una pre-mezcla vitamínica. Por este motivo se le agregó ácido ascórbico a las muestras estudiadas para poder observar el efecto beneficioso de la misma sobre la biodisponibilidad del Fe.
Las muestras analizadas fueron preparadas de la siguiente manera:
La dializabilidad de los minerales (D) como un indicador de la bioaccesibilidad fue determinada por un método in vitro (8), modificado (9). El procedimiento involucra una digestión enzimática en condiciones que simulan las fisiológicas. Cada muestra fue homogeneizada para facilitar su posterior análisis. Alícuotas de 50 g de los homogeneizados fueron incubadas con 5 ml de una solución acuosa al 3% de α-amilasa, durante 30 min a 37º C con agitación. Luego, el pH se ajustó a 2 con solución valorada de HCl 6N y se agregaron 1,6 ml de una solución de pepsina / HCl (16 g/100 mL en HCl 0,1N) (Sigma-Aldrich, P7000), incubándose la mezcla a 37º C durante 2 h, con agitación (proceso que simula la digestión estomacal). Dos alícuotas de 15g del digerido se colocaron en Erlenmeyers (capacidad 120 ml y de boca ancha) con bolsas de diálisis Spectrapore Molecular Weight cut-off 6000-8000) conteniendo 18,75 mL de buffer PIPES 0,15 M y pH variable. Después de una hora de incubación, cuando el pH alcanzó un valor mínimo de 4,5, se agregaron 3,75 ml de una mezcla de bilis-pancreatina [2,5% bilis (Sigma-Aldrich B8631) y 0,4% pancreatina (Sigma-Aldrich P1750) en NaHCO3 0,1N] prosiguiéndose la incubación durante 2 h a 37ºC para simular la digestión intestinal. Las bolsas de diálisis fueron removidas y enjuagadas con agua ultrapura y los dializados se transfirieron a tubos tarados y se pesaron. Los minerales dializados se cuantificaron por espectroscopía de absorción atómica (10).
El contenido total de minerales de las muestras fue cuantificado en el digerido obtenido luego de la digestión con pepsina por espectroscopía de absorción atómica previa mineralización con una mezcla HNO3 -HClO4 (50:50) (11).
Para las determinaciones de Ca y Mg las muestras se diluyeron con 0,65% de lantano para suprimir la interferencia causada por los fosfatos (12).
La dializabilidad mineral fue calculada como el porcentaje del mineral dializado con respecto a la concentración total de mineral presente en cada muestra.
Dializabilidad % del mineral = (mg de mineral en el dializado / mg de mineral en el digerido) x 100
El análisis estadístico se realizó utilizando ANOVA y Test de Dunnet a posteriori con p< 0,05.
Las concentraciones medias de minerales en yerba mate fueron: Fe: 48,9 mg/100g, Ca: 858,0 mg/100g, Mg: 499,0 mg/100g y Zn 5,6 mg/100, lo cual hacía suponer que este producto sería un importante aportador de minerales en la dieta.
Sin embargo, la DFe fue nula en el mate cocido (Tabla 1). Por otra parte la DFe fue muy baja en las leches fortificadas con SF y BGF obteniéndose un valor elevado cuando la fuente de fortificación fue el EDTANaFe (Tabla 1). En las mezclas de leche fortificada con mate cocido, los valores fueron intermedios a los de la leche y el mate cocido. Sólo en las infusiones cocciones de leche fortificada con sulfato ferroso con yerba mate (ICSF) la DFe fue menor a la de la mezcla, no encontrándose diferencias significativas en las muestras que contenían BGF y EDTANaFe como fuentes de fortificación (p>0,05) (Tabla 1).
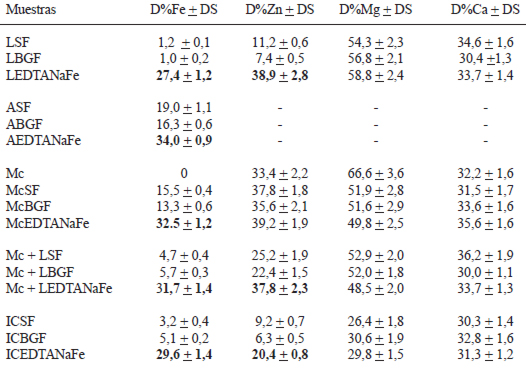
La DCa no presentó variaciones importantes en las leches fortificadas y sus preparaciones con yerba mate (Tabla 1).
En el caso de la DZn, de modo semejante a lo ocurrido con la DFe, los valores obtenidos en las mezclas mate cocido:leche fueron intermedios a los hallados en leche y en mate cocido para las muestras fortificadas con SF y con BG. Sin embargo, en el caso del EDTANaFe no se encontró diferencia significativa para la DZn en ninguna de las tres matrices estudiadas (Tabla 1). En el caso de la infusión:cocción los valores de la DZn fueron menores a los de la leche fortificada con SF y BGF, sólo existiendo diferencia significativa en el caso de la leche fortificada con EDTANaFe (Tabla 1).
La DMg presentó valores altos tanto en la leche, como en el mate cocido y en la mezcla mate:leche, independientemente de la fuente de fortificación empleada, no existiendo diferencia significativa entre estas muestras ni en comparación con los valores obtenidos en las muestras de agua empleadas como control (Tabla 1). Sólo se pudo observar una disminución significativa en los valores obtenidos en la infusión cocción (Tabla 1).
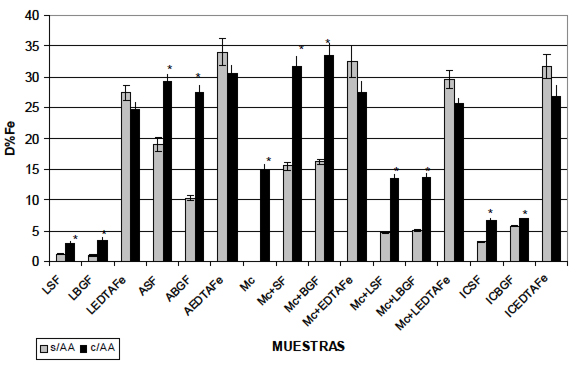
Al analizar los valores de DFe de todas las muestras con y sin agregado de AA se puede observar que, salvo en el caso de las muestras en donde la fuente de fortificación es el EDTAFe, la DFe mostró un aumento muy significativo, (p<0,01) (Figura1). Para el caso de las muestras fortificadas con EDTANaFe (Figura 1) el efecto fue negativo.
La biodisponibilidad de los minerales se mide con gran precisión en los estudios in vivo, sobre todo en humanos. También existen estudios con cultivos celulares que se han aplicado con éxito, sobre todo para estimar la biodisponibilidad del Fe. Sin embargo tales técnicas son laboriosas y costosas por lo que pueden aplicarse en pocos laboratorios en el mundo. Entre los métodos in vitro, la dializabilidad del Fe ha mostrado ser un buen predictor de la biodisponibilidad (13). Los resultados de los ensayos in vitro evalúan sólo la capacidad para la absorción, es decir que los minerales no están formando complejos insolubles y/o de elevado peso molecular, concepto al que actualmente se lo denomina bioaccesibilidad. Algunos autores han demostrado que la dializabilidad del Zn también tiene buena correlación con los estudios in vivo y puede ser útil para predecir su biodisponibilidad (14-16). Tanto para el Fe como para el Zn las condiciones presentes en el tracto intestinal son los principales determinantes de la absorción. La determinación de la dializabilidad de Ca ha sido propuesta para predecir la biodisponibilidad (14,15,17). Para elementos traza como el Ca donde mecanismos homeostáticos complejos regulan no sólo la absorción sino también la retención, las condiciones en el lumen intestinal no serían los principales factores para regular la biodisponibilidad. Sin embargo, la evaluación de la dializabilidad del Ca es útil para determinar la proporción de Ca soluble y potencialmente absorbible. En el presente trabajo se ha utilizado una modificación del método de diálisis que ha demostrado, en trabajos anteriores, ser de gran utilidad para determinar la bioaccesibilidad mineral.
La dializabilidad del Fe fue nula en las infusiones de yerba mate lo que podría explicarse dado que estudios en ratas demostraron que los polifenoles son ligandos inhibidores del hierro no hemínico (18). Estos forman complejos insolubles con el hierro y también con el zinc que precipitan y por lo tanto no pueden dializar. Estos complejos también pueden ser de un alto peso molecular (mayor a 8000 Daltons) lo que impediría tanto su diálisis como su absorción in vivo (19). Esto se ve reflejado en los valores bajos tanto para la DFe como para la DZn en las infusiones de yerba mate y las mezclas con leche.
Respecto a los valores bajos para la DFe obtenidos con las muestras de leche fortificada con las diferentes fuentes de Fe, esto se justifica dado que en diversos estudios previos se ha demostrado que tanto las caseínas como el Ca de la leche son importantes inhibidores de la absorción del Fe y del Zn (20-22).
Si bien los valores de la dializabilidad mineral en las IC fueron los más bajos de todas las muestras estudiadas, se hubiera esperado un efecto depresor más marcado dado que la cantidad de inhibidores presentes en la IC es mayor que la presente en las mezclas.
La DZn fue baja en las leches fortificadas con SF y BGF presentando un valor elevado cuando la fuente de fortificación fue EDTANaFe. Estudios previos han demostrado que la absorción del NaFeEDTA puede ser 2,5 veces mayor que la del sulfato ferroso, según la matriz alimentaria (23).
Los valores de la DZn de las muestras de mate cocido con agregado de Fe fueron elevados y no presentaron diferencia significativa entre las tres fuentes de Fe estudiadas. Esto estaría demostrando que el efecto inhibidor del calcio y la caseína de la leche (21, 24) es mucho mayor que el de los polifenoles de la yerba mate (25).
El aumento marcado de la DFe en las muestras con agregado de ácido ascórbico se debería a que la acción de este último involucra la reducción del ion férrico a su forma ferrosa, mejor absorbida, la formación de quelatos solubles y estables con el hierro en el estómago y por ende el mantenimiento de su solubilidad cuando el alimento ingresa en el ambiente más alcalino del duodeno. Este último efecto se puede explicar por el hecho de que el ácido ascórbico forma complejos solubles con el hierro de los alimentos a pHs más bajos que los ligandos inhibitorios, es decir que actuaría a nivel estomacal donde las condiciones de pH son desfavorables para la formación de complejos con otros ligandos (26). Sin embargo, cuando se empleó EDTANaFe como fortificante, el efecto del AA resultó levemente negativo. Esto ya se había encontrado en trabajos previos donde se observó que en matrices alimentarias que contienen inhibidores de la absorción no se observa el efecto promotor del AA sobre la biodisponibilidad del EDTANaFe (27).
El consumo de infusiones de yerba mate no aportaría Fe. Sin embargo, el consumo de tales infusiones en mezcla con leche fortificada con Fe no afectaría negativamente la disponibilidad de Fe en dicha matriz, aunque la preparación de infusiones-cocciones con leche puede disminuir la bioaccesibilidad de Fe, Zn y Mg. El agregado de AA promueve un importante aumento en la dializabilidad de Fe tanto en las infusiones como en sus preparaciones con leche.
Este trabajo fue parcialmente financiado por el proyecto UBACyT B081.
Recibido: 09-01-2011
Aceptado: 10-04-2011