Introducción
La Organización Mundial de la Salud (1) recomienda la incorporación de alimentos complementarios a partir del sexto mes de vida, momento en que la mayoría de los lactantes comienzan a consumir papillas semisólidas, como parte de su alimentación. Estos alimentos complementarios juegan un rol muy importante en la nutrición infantil. En Argentina, las dietas caseras se encuentran entre las variantes más usadas y más recomendadas por los pediatras.
Un aspecto muy importante de los alimentos complementarios se refiere a su digestibilidad, su aporte de proteínas de alta calidad y de minerales esenciales (2, 3). Es habitual que el hierro, calcio y zinc se encuadren entre los nutrientes críticos por encontrarse en niveles sustancialmente inferiores a los recomendados (1, 4).
Por otra parte, la fortificación de alimentos de consumo masivo es una de las estrategias costo-beneficio más utilizada para prevenir las deficiencias poblacionales de minerales. En Argentina, desde el año 2003, la harina de trigo se enriquece con sulfato ferroso, con el objetivo de disminuir la prevalencia de anemia en la población.
La disponibilidad de los micronutrientes, especialmente de los minerales, es particularmente importante ya que muchos componentes presentes en los alimentos / dietas, afectan su absorción y utilización, al igual que la forma química de los minerales de fortificación (5). Una opción adicional para mejorar la absorción del mineral propio de la matriz así como la del mineral de fortificación consiste en el agregado a los alimentos de promotores de la absorción mineral.
Las distintas fuentes de hierro usadas como fortificantes presentan ventajas y desventajas para su aplicación (6). Los compuestos de hierro utilizados comprenden a algunos que son solubles en agua, en ácidos diluidos, o insolubles en agua. Los compuestos de hierro solubles en agua o en ácidos diluidos tienen buena biodisponibilidad pero son también los más reactivos. Catalizan reacciones oxidativas que producen cambios en las características organolépticas de los alimentos (7). También se utilizan complejos de aminoácidos como el bisglicinato ferroso o el glicinato férrico, que además de poseer buena biodisponibilidad, no poseen las cualidades prooxidantes del sulfato ferroso (8).
En el caso de las dietas con importantes cantidades de inhibidores de la absorción del hierro, sería conveniente utilizar promotores de la absorción y/o fortificantes cuya biodisponibilidad sea superior a la del sulfato ferroso. En la actualidad existen tres fuentes que poseen este potencial, el NaFeEDTA, la hemoglobina y complejos de aminoácidos como el bisglicinato ferroso ya mencionado (9). La absorción del NaFeEDTA puede ser 2,5 veces mayor que la del sulfato ferroso, según la matriz alimentaria (10). Esto se debería a que los fitatos de los cereales tienen poco efecto inhibitorio sobre esta fuente (11). Sin embargo, en nuestro país el uso del NaFeEDTA como fuente de fortificación no está permitido. Por ello, sería una buena estrategia recurrir al agregado de diferentes promotores de la absorción para permitir que el hierro del sulfato ferroso estuviera más disponible para ser asimilado.
Para el caso del zinc la situación es muy similar a la del hierro. Si bien no es habitual que los alimentos de consumo masivo estén fortificados con zinc, sí lo están los destinados a lactantes o niños de la primera infancia, debido a que la deficiencia de este mineral provoca la detención del crecimiento, alteraciones del desarrollo cognitivo y problemas en el sistema inmune (1). Por otra parte, otros alimentos o bebidas habitualmente presentes en la dieta podrían afectar la absorción de estos minerales (12).
El objetivo del presente trabajo es el estudio de la disponibilidad de hierro y zinc en una dieta complementaria de consumo habitual conteniendo pan fortificado con diferentes fuentes de hierro: sulfato ferroso, bisglicinato férrico, NaFeEDTA, o bien pan sin fortificar con agregado de ácido ascórbico, citrato de sodio o Na2EDTA como promotores de la absorción, combinada con diversas bebidas.
Materiales y métodos
Se elaboró una dieta infantil de consumo habitual (13) con los componentes y proporciones indicados en la Tabla 1. Los componentes utilizados en la dieta estaban cocidos, tal como se consumen. El pan empleado fue elaborado en el laboratorio. Se realizó una primera mezcla con procesadora doméstica, de los componentes sólidos: zapallo (Cucurbita moschata), papa (Solanum tuberosum L.), sémola de trigo (Triticum vulgare) preparada con caldo de verduras y manzana (Pirus malus L.), a excepción del pan. Posteriormente se tomaron 132g de esta mezcla y se le adicionaron 11g de pan y 68g de alguna de las bebidas. Con estos componentes se realizó la mezcla final que luego fue sometida al análisis.
TABLA 1
Composición de la dieta.

Las bebidas ensayadas fueron: agua, leche, té, bebida cola (BC) y bebida artificial a base de naranja (BAN). Las condiciones de preparación para estas bebidas fueron: té (1 saquito/250 ml de agua ultrapura a ebullición), bebida artificial a base de naranja (24 g de polvo para preparar bebidas/300 ml de agua ultrapura).
El pan se fortificó con tres fuentes distintas de hierro: sulfato ferroso (SO4Fe), bisglicinato férrico y Na-FeEDTA. En todos los casos se obtuvo una concentración de 30 ppm de Fe en el pan que es el nivel de enriquecimiento obligatorio en Argentina.
La concentración de los promotores de la absorción en los panes fue de 300 ppm de ácido ascórbico (AA), 1,2% de citrato de sodio y 30 mg% de Na2EDTA.
Las relaciones finales Fe:promotor en cada uno de los panes fueron de 1:2 en el caso del pan con AA; 1:50 en el que tenía agregado de citrato y 1:1 en el pan con EDTA.
En el caso del AA, una relación 1:2 sería suficiente para ejercer el efecto promotor. En trabajos realizados previamente se pudo observar que esta relación incrementaba de manera significativa la DFe (14).
En estudios realizados en humanos se observó que la acción promotora del citrato no se evidenciaba a bajas relaciones molares Fe:promotor (1:10) pero sí lo hacía a elevadas concentraciones de citrato (1:50), siendo además dosis-dependiente (15, 16).
Para el EDTA se trabajó con una relación Fe:EDTA 1:1 que es suficiente para incrementar la biodisponibilidad de Fe en dietas ricas en fitatos (17). La ventaja del EDTA es su elevada constante de afinidad por el hierro, mayor que la que poseen este tipo de inhibidores. Esto asegura una buena competencia entre inhibidor y promotor. Por otra parte, cuando la relación EDTA:Fe es mayor a 1 hay una marcada disminución de la absorción de hierro (18).
Dializabilidad
La dializabilidad de los minerales (D) como un indicador de la biodisponibilidad potencial fue determinada por medio de un método in vitro (19), modificado por Wolfgor et al (20). El procedimiento involucra una digestión enzimática en condiciones que simulan las fisiológicas. Cada muestra fue homogeneizada para facilitar su posterior análisis. Alícuotas de 50 g de los homogeneizados fueron incubadas con 5 ml de una solución acuosa al 3% de α-amilasa, durante 30 minutos a 37º C con agitación. Luego, el pH se ajustó a 2 con solución valorada de HCl 6N, y se agregaron 1,6 ml de pepsina-HCl (16 g/100 ml en HCl 0,1N), incubándose la mezcla a 37º C durante dos horas, con agitación (digestión estomacal). Dos alícuotas de 15 g del digerido se colocaron en erlenmeyers con bolsas de diálisis (Spectrapore Molecular Weight cut-off 6000-8000) conteniendo 18,75 ml de buffer PIPES 0,15 M y pH variable. El pH del buffer a utilizar fue establecido luego de hacer ensayos previos en base a la matriz alimentaria en estudio (21), para obtener un pH final uniforme de 6,5 0,2, al final de la segunda incubación a 37º C. Después de una hora de incubación, cuando el pH alcanzó un valor mínimo de 4,5, se agregaron 3,75 ml de una mezcla de bilis-pancreatina (2,5% bilis y 0,4% pancreatina en NaHCO3 0,1N) prosiguiéndose la incubación durante dos horas a 37º C (digestión intestinal). Las bolsas de diálisis fueron removidas y enjuagadas con agua ultrapura y los dializados se transfirieron a tubos tarados y se pesaron. Los minerales dializados se determinaron por espectroscopía de absorción atómica (22, 23).
El contenido total de minerales de las muestras fue determinado en el digerido de pepsina por espectroscopía de absorción atómica previa mineralización con una mezcla HNO3 -HClO4 (50:50).
La dializabilidad mineral fue calculada como el porcentaje del mineral dializado con respecto a la concentración total de mineral presente en cada muestra.
Dializabilidad % del mineral =

Estadística
El análisis estadístico se realizó utilizando ANOVA y Test de Tukey a posteriori (p< 0,05).
Resultados
Dializabilidad de hierro
La concentración de hierro era de 0,20 mg% cuando la dieta contenía pan sin fortificar. Las dietas con pan fortificado con sulfato ferroso, bisglicinato férrico y NaFeEDTA contenían 0,45 mg%, 0,53 mg% y 0,44 mg%, respectivamente.
No hubo diferencias significativas entre las dietas del pan fortificado con sulfato ferroso o bisglicinato férrico, pero sí con el NaFeEDTA, donde el aumento fue muy significativo en todas las combinaciones estudiadas (p<0,05) (Fig.1).
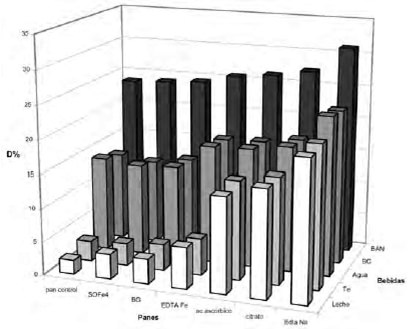
FIGURA 1
DFe en una dieta con pan fortificado con diferentes fuentes de hierro o agregado de promotores de absorción mineral, combinada con distintas bebidas.
Al comparar los tres promotores se pudo observar que la mayor DFe se obtuvo en las dietas que contenían el pan con agregado de EDTA sódico (p<0,05). Entre las dietas que contenían ácido ascórbico o citrato de sodio no se observó ninguna diferencia significativa (Fig 1).
Por otra parte, el aumento de la D fue mucho más elevado en las dietas que tenían panes con agregado de promotores de la absorción que las que tenían panes fortificados (Fig 1).
Cuando se combinó la dieta con las diferentes bebidas se pudo observar que la bebida artificial a base de naranja era la que más aumentaba la DFe (Fig 1).
La bebida cola no produjo variación en la DFe con respecto al control con agua. En cambio, tanto el té como la leche la disminuyeron significativamente (Fig 1).
Dializabilidad de zinc
La concentración de zinc en las dietas estudiadas fue de 0,25 mg%.
Al analizar los valores de la DZn se observó (Fig 2) que no existía diferencia significativa entre las dietas con agregado de ácido ascórbico y citrato pero sí con la dieta que tenía agregado de Na2EDTA (p<0,05).
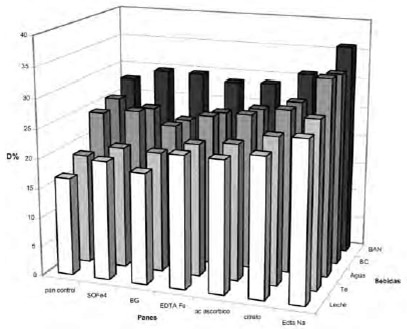
FIGURA 2
DZn en una dieta con pan fortificado con diferentes fuentes de hierro o agregado de promotores de absorción mineral, combinada con distintas bebidas.
Sin embargo, en los panes fortificados con las distintas fuentes de hierro la DZn varió dependiendo de la bebida utilizada. (Fig 2). Si bien cuando la bebida empleada fue agua no existió diferencia significativa entre el control y las tres fuentes de hierro estudiadas, si comparamos las tres fuentes de hierro entre sí, se observó que al utilizar bisglicinato la DZn tendía a ser menor que cuando las fuentes eran sulfato ferroso y Na-FeEDTA (Fig 2).
Tampoco se pudo observar diferencia significativa en las dietas que tenían panes con ácido ascórbico o citrato de sodio y las dietas con panes con sulfato ferroso o EDTA Fe (Fig 2).
Cuando la dieta se combinó con las diferentes bebidas se observó que la inclusión de té o leche provocó una disminución de la DZn. Al agregar la bebida a base de naranja se observó un aumento significativo de la DZn (p<0,05). No se observó una variación significativa con el uso de bebida cola. (Fig 2)
Discusión
Dializabilidad de hierro
En las dietas en las que la fuente de hierro era Na-FeEDTA, o el promotor utilizado era EDTA sódico, la DFe aumentaba de manera muy marcada.
La alta disponibilidad potencial del NaFeEDTA se puede atribuir a que el hierro en este quelato está más fuertemente ligado, que en el bisglicinato o sulfato ferroso, y también posee una constante de afinidad por el hierro mayor que los inhibidores presentes. De la misma manera, cuando el EDTA es utilizado como promotor, formaría complejos más estables que los que forma el Fe con los fitatos, que son los principales inhibidores en esta dieta. Estos resultados son concordantes con los observados en otros estudios (24, 25).
Sin embargo, hay que tener en cuenta que el EDTA posee una Ingesta Diaria Admisible (IDA) de 0-2,5 mg/kg/día (26). Por lo tanto debe considerarse la Ingesta Diaria Potencial (IDP) de este aditivo no sólo para controlar los niveles de adición aprobados por la legislación, sino también frente a la posibilidad de utilizar FeNaEDTA como fortificante de alimentos.
En un estudio realizado en Argentina en 2007, en un grupo de 199 niños de entre 3 y 18 años, la IDP obtenida fue de 0,04mg/Kg (27). En Argentina, los alimentos en los que se autoriza el agregado de EDTA son las bebidas sin alcohol y las mayonesas. Los resultados indican que la IDP está muy lejos del valor de la IDA, lo cual sería un buen comienzo para profundizar estudios y plantear la posibilidad de utilizar este compuesto ya sea como fortificante o como promotor.
El aumento de la DFe con la bebida artificial a base de naranja se atribuye a la presencia de los ácidos cítrico y ascórbico que son importantes promotores de la absorción del hierro. Cabe destacar que la acción del ácido ascórbico involucra la reducción del ion férrico a su forma ferrosa, mejor absorbida, la formación de quelatos solubles y estables con el hierro en el estómago y por ende el mantenimiento de su solubilidad cuando el alimento ingresa en el ambiente más alcalino del duodeno. Este último efecto se puede explicar por el hecho de que el ácido ascórbico forma complejos solubles con el hierro de los alimentos a pHs más bajos que los ligandos inhibitorios, es decir que actuaría a nivel estomacal donde las condiciones de pH son desfavorables para la formación de complejos con otros ligandos. Estos efectos, que ocurren en el tracto gastrointestinal, serían los mismos que explican el marcado incremento de la dializabilidad observada in vitro, en condiciones que simulan las fisiológicas (12, 28).
Por otra parte, la absorción de hierro en las dietas que contienen leche es afectada adversamente por la presencia de proteínas lácteas y calcio (29-30-31). La presencia de grupos fosfoserina en las subunidades de caseína, puede explicar la unión del hierro a péptidos de caseína insolubles y, por lo tanto, la disminución de la DFe y su biodisponibilidad.
En el caso del té, el efecto depresor sería causado por los polifenoles presentes, que son ligandos inhibidores de la absorción del hierro no hemínico. Estudios en ratas demostraron que los polifenoles forman complejos insolubles con el hierro y el zinc que precipitan y por lo tanto no pueden dializar. Estos complejos también pueden ser de un alto peso molecular lo que impediría tanto su diálisis como su absorción in vivo (32).
Existen evidencias de una alta correlación entre los estudios de dializabilidad de hierro in vitro y los estudios realizados en humanos (33).
Dializabilidad de zinc
El hecho de que no se observaron diferencias significativas en la dializabilidad de zinc en las dietas que tenían panes con ácido ascórbico o citrato de sodio y las dietas con panes con sulfato ferroso o FeEDTA, se debería a una competencia en la dializabilidad del hierro y del zinc, de tal manera que al haber mayor cantidad de hierro en el medio, la dializabilidad del zinc se vería afectada (34).
Tal como se indicó para el hierro, la inclusión de té o leche provocó una disminución de la DZn. Los polifenoles presentes en el té ejercerían un efecto inhibitorio sobre la absorción del Zn (35). En el caso de la leche el efecto inhibitorio se debería al calcio presente que, junto con los fitatos de la dieta, formarían complejos insolubles que impiden la absorción del Zn (36).
En la combinación con la bebida a base de naranja, el aumento significativo de la DZn se debería a que el ácido cítrico presente en esta bebida, es uno de los promotores de la absorción de zinc. Este forma de complejos con el ácido cítrico que lo mantendría soluble a pHs fisiológicos y así ejercería un efecto positivo sobre su absorción (37).
Conclusiones
Los resultados permiten concluir que varios factores influyen sobre la biodisponibilidad potencial de hierro y zinc. La bebida utilizada en la dieta, la fuente de hierro empleada como fortificante o el promotor de la absorción mineral agregado en el pan son determinantes de la disponibilidad mineral.
Las dietas que contenían sales de EDTA como fortificante o promotor fueron las que presentaron mayores valores de DFe y Zn, por lo que su utilización parece promisoria. Si bien los resultados en este estudio fueron obtenidos utilizando métodos in vitro permiten tener una idea de la bioaccesibilidad de los minerales en las dietas evaluadas.
Agradecimientos
Proyectos PICTR0110 y UBACYTB063.
Referencias
- World Health Organization. Complementary feeding of young children in developing countries; a review of current scientific knowledge. Geneva, 1998.
- Glinsmann WH, Bartholmey SJ, Coletta F. Dietary guidelines for infants: a timely reminder. Nutr Rev 1996; 54:50-57.
- Dewey KG, Cohen RJ, Landa Rivera L, Brown KH. Effects of age of introduction of complementary foods on iron status of breast-fed infants in Honduras. Am J Clin Nutr 1998; 67:878-884.
- Gibson RS, Hotz C. The adequacy of micronutrients in complementary foods. Pediatrics 2000; 106: 1298-1299.
- Olivares A.B, Martinez C., López G., Ros GInfluence of the design of a product on in vitro mineral availability of homogenized weaning foods. Innovative Food Science & Emerging Technologies. 2001; 2 181-187.
- Hurrell RFImproving the iron fortification of foods. En: Nutritional Anemias. Nestle Nutrition Workshop Series No. 30. Ed. By S.R. Fomon and S. Zlotkin. New York: Vervey/Raven Press Ltd. 1992; 193-208.
- Hurrell RF. Nonelemental Sources. En: Iron Fortification of Foods. Ed. Clydesdale FM and Wiemer KL. New York: Academic Press 1985; 147-178.
- Galdi M, Carbone N, Valencia ME. Comparison of ferric glycinate to ferrous sulphate in model infant formulas: kinetic of T.B.A., lysine and methionine changes. J Food Sci 1989; 54 (5): 1230-1233.
- Allen LH, Ahluwalia N. Improving Iron Status Through Diet. The application of knowledge concerning dietary iron bioavailability in human populations. 1997; Arlington, Va: OMNI. Technical paper, 8.
- Ballot DE, MacPhail AP, Bothwell TH, Gillooly M and Mayet FG. Fortification of curry powder with NaFe(III)EDTA in an iron-deficient population: report of a controlled iron-fortification trial. Am J Clin Nutr. 1989; 49: 162-169.
- INACG. Iron EDTA for Food Fortification. A report of the International Nutritional Anemia Consultative Group. Lynch SR, Hurrell RF, Bothwell TH, and MacPhail AP. Washington. USA. 1993.
- Binaghi MJ, Lopez LB, Ronayne de Ferrer PA, Valencia ME. Evaluación de la influencia de distintos componentes de la dieta sobre la biodisponibilidad potencial de minerales en alimentos complementarios. Rev Chil Nutr 2007; 34-1, 56-60.
- Macías SM. Evaluación de nutrientes en leche materna y en alimentos complementarios usados durante el primer año de vida. Tesis doctoral. Universidad Nacional de Santiago del Estero, Argentina. 2005.
- Pizarro F A, Olivares M G, Kain J B. Hierro y zinc en la dieta de la población de Santiago. Rev Chil Nutr 2005; 32: 1-8.
- Derman, D. P., Ballot, D., Bothwell, T. H., MacFarlane, B. J., Baynes, R. D., MacPhail, A. P et al. Factors influencing the absorption of iron from soya-bean protein products. Br. J. Nutr. 1987; 57: 345–353.
- Gillooly, M., Bothwell, T. H., Torrance, J. D., Mac-Phail, A. P., Derman, D. P., Bezwoda, W. R. The effects of organic acids, phytates and polyphenols on the absorption of iron from vegetables. Br. J. Nutr. 1983; 49: 331–342.
- Hurrell R, Reddy M, Burri J, Cook JD. An evaluation of EDTA compounds for iron fortification ofcerealbased foods. Br. J. Nutr. 2000; 84: 903-910.
- Hurrel FR. Fortification: Overcoming technical and practical barriers. J Nutr 2002; 132: 806-812.
- Miller D., Schrinken B.R., Rassmussen R.R.. An in vitro method for estimation of iron availability from meals. Am J Clin Nutr 1981; 34:248-56.
- Wolfgor R., Drago S.R., Rodriguez V., Pellegrino N., Valencia M.E. In Vitro measurement of iron availability in fortified foods. Food Res Int. 2002; 35: 85-90.
- Drago Silvina R., Binaghi Maria J., Valencia Mirta E. Effect of gastric digestion pH on iron, zinc, and calcium dializability from preterm and term starting infant formulas. J Food Sci 2005; 70:(2) 107-112.
- Official Method of Analysis of AOAC International. 17th Edition. Washington DC, USA. Association of Official Analytical Chemists. 2000
- Perkin-Elmer Corp. Calcio, Hierro y Zinc. Analytical Method for Atomic Absorption Spectrophotometry. Norwolk Cl. 1971
- Pabón ML, Lönnerdal B. Distribution of iron and its bioavailability from iron fortified milk and formula. Nutr Res 1992; 12:975-984.
- Drago SR, Valencia ME. Mineral dialyzability in milk and fermented dairy products fortified with Fe-NaEDTA. J Agric Food Chem. 2008; 56(8):2553-7.
- JECFA. Annex 4: Acceptable daily intakes [Ethylenediaminetetraacetate, disodium and calcium disodium salts]. In: Toxicological Evaluation of Certain Food Additives With a Review of General Principles and of Specifications. Prepared by the 17th Meeting of the Joint FAO/WHO Expert Committee on Food Additives (JECFA). Geneva (Switz.): World Health Organization (WHO); 1974, WHO Technical Report Series No. 539, pp. 35-38.
- Cagnasso Carolina E., López L B., Rodríguez V G., Valencia M E. Estimación de la ingesta potencial de ácido etilendiaminotetraacético en niños y adolescentes argentinos, influencia de la fortificación de cereales para desayuno con sal férrica de este ácido. Rev Chil Nutr. 2007; 34 (2):143-149.
- Troesch B, Egli I, Zeder C, Hurrell RF, Zimmermann MB. Fortification iron as ferrous sulfate plus ascorbic Acid is more rapidly absorbed than as sodium iron EDTA but neither increases serum nontransferrinbound iron in women. J Nutr. 2011;141(5):822-7.
- Jackson LS. The effect of dairy products on iron availability. CRC Crit Rev Food Sci Nutr. 1992; 31:259-70.
- Hurrell RF. Bioavailability of iron. In: Assessment of the bioavailability of micronutrients. Proceedings of an ILSI Europe Workshop. Eur J Clin Nutr. 1997;51:54-8.
- Drago SR and Valencia ME. Influence of components of infant formulas on in vitro iron, zinc and calcium availability. J Agric Food Chem. 2004; 52: 3202-3207.
- Brown R.C., Klein A., Simmons W., Hurrell R. The Influence of Jamaican herb teas and other polyphenol-containing beverages on iron absorption in the rat. Nutr Res. 1990; 10: 343-53.
- Walter T, Pizarro F, Olivares M. Iron bioavailability in corn-masa tortillas is improved by the addition of disodium EDTA. J Nutr. 2003; 133(10):3158-61.
- Binaghi MJ, Cagnasso C, Pellegrino N, Ronayne P, Valencia M Dializabilidad y aporte potencial de hierro y zinc en una dieta para niños, con pan con agregado de diferentes promotores de la absorción con o sin agregado de sulfato ferroso. Trabajos del XII Congreso Argentino de Ciencia y Tecnología de Alimentos. 2009. (editado en CD). ISBN: 978-987-22165-3-5.
- Aggett PJ, Comererford JG. Zinc and human health. Nutr Rev. 1995; 2: 16-22.
- O´Dell BL. Mineral interactions relevant to nutrient requirements. J Nutr. 1989; 119 ,12:1832-1838.
- Pabón ML, Lönnerdal B Effect of citrate on zinc bioavailability from milk fractions and infant formulas. Nutr Res. 1993; 13:103-111.