El síndrome de déficit de atención e hiperactividad (ADHD) es un trastorno neurológico /conductual que se inicia en la infancia. Se ha propuesto que el zinc tendría un potencial rol como terapia adjunta para el ADHD. Nuestro objetivo fue evaluar el efecto de la suplementación con zinc sobre la conducta, como terapia complementaria al metilfenidato, en niños con ADHD. En un estudio controlado, doble ciego, se seleccionaron 40 pacientes con criterios clínicos y psicométricos de ADHD, (31 niños, 9 niñas, 7-14 años de edad). Ellos fueron seleccionados aleatoriamente para recibir ya sea metilfenidato 0,3 mg/kg/d + placebo (sacarosa) (grupo placebo, GPL), o metilfenidato 0,3 mg/kg/d + zinc (sulfato) 10 mg/d (grupo Zn, GZN) por 6 semanas; se excluyeron 4 niños. Se tomó una muestra de 3 mL de sangre en el tiempo 0 y a las 6 semanas para el análisis de Zn plasmático; se aplicó en ambos tiempos a padres y profesores la escala abreviada de Conners para ADHD. Entre los resultados, El Zn plasmático fue normal en el tiempo 0 en ambos grupos, disminuyendo después de 6 sem., especialmente en el grupo GPL (GPL: 95,9 ± 21,5 a 77,9 ± 15,5; GZN: 90.3 ± 9.1 a 85,0 ± 12,0 μg/dl, NS). El test de Conners aplicado por los profesores mostró una aparente mejoría en GZN: GPL: 18 (9-28) a 16 puntos (2-26); GZN: 19 (6-24) a 11 puntos (3-23) (p= 0,07), sin mejoría en el Conners aplicado por los padres: GPL: 19 (7-25) a 13 (3-22); GZN: 19 (7-25) a 11 (2-19). Se concluye que se observa una disminución en las concentraciones plasmáticas de Zn en ambos grupos, pero mayor en el grupo placebo. Con el suplemento de zinc se observa una aparente mejoría en los síntomas de ADHD, de acuerdo con la evaluación de Conners aplicada por profesores. Se requiere avanzar en el estudio de esta probable interacción entre zinc y metilfenidato.
Palabras clave: Zinc, déficit de atención, hiperactividad, metilfenidato, Conners
The attention-deficit/hyperactivity disorder (ADHD) is a neurological/behavioral disorder which begins in childhood. Zinc has a potential role as an adjuvant therapy for ADHD. The objective was to evaluate the effect of Zn supplementation on behavior, as a complementary therapy to metylphenidate, in pediatrics patients with ADHD. In a controlled, double blind design, 40 patients with clinical criteria of ADHD (DSMIV) and psychometric evaluation (WISC-R), were selected (31 boys and 9 girls, 7-14 years of age). They were randomized to receive methylphenidate 0.3 mg/kg/d + placebo (sucrose) (group placebo, GPL) or methylphenidate 0.3 mg/kg/d + zinc (sulfate) 10 mg/d (group Zn, GZN) for 6 weeks. A blood sample was drawn at time 0 and 6 weeks, for plasma Zn analysis. The teacher and parent ADHD rating scale (Conners` global index, CGI) was applied at both times. Among the results, plasma Zn was normal at time 0, decreasing especially in the GPL after 6 weeks (GPL: 95.9 ± 21.5 to 77.9 ± 15.5; GZN: 90.3 ± 9.1 to 85.0± 12.0 μg/dL; NS). The CGI by teachers showed a non-significant improvement with Zn: GPL: 18 (9-28) to 16 points (2-26); GZN: 19 (6-24) to 11 points (3-23) (p=0.07); no significant difference in the CGI by parents by groups was found: GPL: 19 (7-25) to 13 (3-22); GZN: 19(7-25) to 11(2-19). We conclude that a decrease in plasma Zn levels in both groups was found, greater in the placebo group. An apparent improvement in ADHD signs in children was observed with the Zn supplementation, according to the Conners global index by teachers.
Key words: Zinc, attention deficit, hyperactivity, methylphenidate, Conners
Departamento de Pediatría, Facultad de Medicina Campus Centro, Universidad de Chile. Servicio de Neuropsiquiatría Infantil, Hospital San Boja-Arriarán. Chile.
El síndrome de déficit de atención e hiperactividad (ADHD) es un trastorno heterogéneo neurológico conductual que comienza habitualmente en la infancia y continúa hasta la edad adulta. El metilfenidato ha sido usado como terapia para el ADHD durante los últimos 50 años, con efectos positivos sobre la conducta, pero también con potenciales efectos adversos, incluyendo un retraso leve en el crecimiento, atribuible según algunos autores a una posible interferencia en el metabolismo de zinc (1,2). Se han ensayado nuevas drogas tratando de incrementar la eficacia sobre el ADHD y disminuir los efectos adversos. En la pasada década, se han publicado algunos estudios que analizaban el rol de algunos micronutrientes como una terapia complementaria potencial para el ADHD, incluyendo el zinc (3, 4,6-8). Algunos de estos estudios fueron efectuados en niños de comunidades de Turquía con una alta prevalencia de deficiencia nutricional de zinc; no conocemos de estudios al respecto en Latinoamérica. El objetivo de esta investigación fue evaluar el efecto de la suplementación de zinc oral por 6 semanas, adicionado a metilfenidato, en niños con síndrome de déficit de atención e hiperactividad.
En un estudio controlado, doble ciego, se seleccionaron aleatoriamente 40 niños (29 niños y 7 niñas, 7-14 años de edad ), de entre 120 pacientes que reunían los criterios clínicos (DSM IV) y psicométricos (WISC –R) para ADHD. Los criterios de inclusión fueron: niños de uno u otro sexo, nacidos a término (≥ 37 semanas de edad gestacional), con un peso al nacer >2500 g, no gemelares y ausencia de enfermedades crónicas o retardo mental; se excluyeron 4 niños por pérdida durante el seguimiento. A los padres de los pacientes se les solicitó un consentimiento informado, el cual fue previamente aprobado por el Comité de Ética e Investigaciones del Departamento de Pediatría, Facultad de Medicina y Servicio de Pediatría Hospital Clínico San Borja-Arriarán.
Todos los niños fueron medidos y pesados en ropa interior, en ayunas; el peso fue medido usando una balanza mecánica con ± 10 g de precisión (SECA Corp., Columbia, MD). La talla fue medida con una precisión de ± 0.1 cm con un estadiómetro (SECA Corp., Columbia, MD). La talla para la edad y el índice de masa corporal fueron calculados y comparados con los estándares de referencia de crecimiento OMSNCHS 2007 (9). Los sujetos fueron asignados en forma aleatoria (bolsa negra con números asignados a cada grupo) para recibir ya sea metilfenidato 0,3 mg/Kg/d más una dosis de una solución que contenía el placebo (sacarosa) (grupo placebo, GPL), o metilfenidato 0,3 mg/Kg/d más una dosis de sulfato de zinc (10 mg Zn + sacarosa) (grupo zinc, GZN), que fueron administradas por la madre en las mañanas, de lunes a viernes durante 6 semanas. El sulfato de zinc fue preparado en una solución al 2 ‰ de Zn elemental. Los códigos fueron mantenidos secretos por el químicofarmacéutico de la unidad de farmacia del hospital hasta completar el análisis de los datos. La adherencia al tratamiento fue evaluada mediante la medición al control siguiente de las dosis remanentes de zinc y metilfenidato en los envases entregados cada 2 semanas. Una muestra de 3 mL de sangre fue extraída al tiempo 0 y otra igual a las 6 semanas (8:30-9:00 h AM), para el análisis de zinc plasmático. La sangre fue inmediatamente transferida a un tubo plástico libre de elementos traza con heparina (100 U). Las muestras de sangre fueron centrifugadas (2500 G) por 10 min, dentro de las primeras 2 horas de extraída y el plasma extraído fue guardado congelado a -20 ºC. Todas las muestras fueron analizadas para Zn en una misma serie, por espectrofotometría de absorción atómica (Perkin Elmer, model 2280, Norwalk, CT).
Se solicitó aplicar la escala abreviada de Conners constituida por 10 puntos (Conners`global index), al inicio y al término del estudio, por el profesor jefe del niño y por los padres (10,11). Para el análisis se utilizó el software estadístico SPSS (Statistical Package for Social Sciences) v. 12.0. Como primer paso, se comprobó que los datos tuvieran una distribución normal, (Kolmogorov-Smirnov), que contrasta la hipótesis de existencia de normalidad. Al comprobar que los datos son normales, se pudo realizar el estudio de diferencia de medias con un análisis de simetría. La prueba t-student para dos muestras relacionadas permitió contrastar hipótesis referidas a la diferencia entre dos medias relacionadas. En este caso obtenemos los estadísticos para muestras relacionadas, su correlación y por ultimo la prueba en si de 2 colas. Se consideró un error alfa de 0,05.
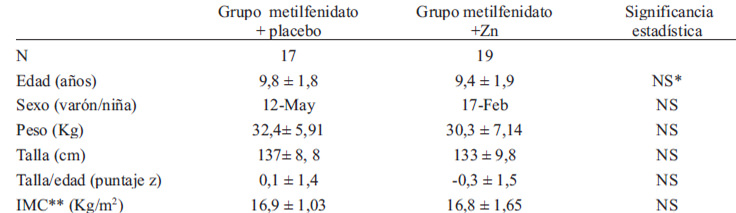
Tanto los varones como las niñas se encontraban dentro de los límites de normalidad para IMC y talla/edad; sin diferencias entre los grupos en el indicador talla/edad ni en IMC.
Las concentraciones plasmáticas de zinc al tiempo 0 estuvieron dentro de límites normales en ambos grupos; después de 6 semanas de seguimiento, en el GPL hubo un descenso de 95,9 ± 21,5 a 77,9 ± 15,5 μg/dL (p< 0,01) y en el GZn hubo un descenso de 90,3 ± 9,1 a 85,0 ± 12,0 μg/dL. Sin embargo la diferencia en la variación 0-6 semanas entre ambos grupos no fue estadísticamente significativa. En el grupo GPL, 5 de los 17 niños presentaron al inicio un Zn plasmático bajo el límite de normalidad (80 μg/dL) y 8 niños lo presentaron a las 6 semanas; en el grupo GZN, 3 de los 19 niños presentaron concentraciones plasmáticas de Zn < 80 μg/dL al inicio y 3 niños a las 6 semanas (NS).
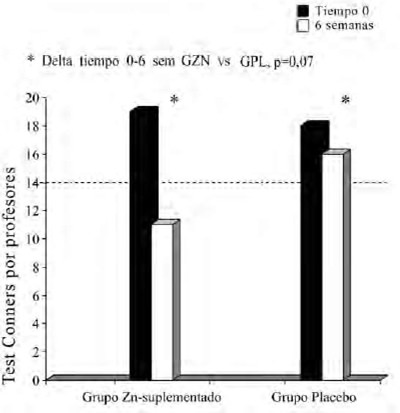
No se observó diferencias en la variación de las encuestas abreviadas de Conners realizadas por los padres; en las realizadas por los profesores se observó una tendencia a un mejor desempeño en el grupo suplementado con Zn en comparación al que recibió placebo: grupo GZn: mediana de 19 puntos al inicio (límites: 6-24) disminuyó a 11 puntos a las 6 semanas (3-23); grupo GPL: mediana de 18 puntos al inicio (9-28) disminuyó a 16 puntos a las 6 semanas (2– 26) (test de simetría; p=0,07) (Fig. 1). En esta misma encuesta completada por los profesores, 16/19 niños del grupo GZn tenían al inicio más de 14 puntos (considerado como sugerente de ADHD) y 5 /19 a las 6 semanas; en el GPL 13/17 al inicio y 7/17 a las 6 semanas (NS).
Nuestros resultados muestran una disminución en las concentraciones plasmáticas de zinc después de 6 semanas de terapia con metilfenidato más placebo, con un descenso no significativo en el grupo que recibió Zn. Este resultado sugiere un efecto de la terapia con metilfenidato sobre el metabolismo del zinc.
Desde las primeras décadas de terapias con metilfenidato, hubo estudios que mostraron un posible efecto negativo del medicamento sobre el peso y la estatura, proponiéndose un efecto sobre el metabolismo del zinc como un mecanismo potencial (1, 2, 12, 13). Mattes et al (1), habían observado un descenso significativo en los percentiles de peso, descenso que fue evidente después de 2, 3 y 4 años de tratamiento con metilfenidato, pero no durante el primer año. Sin embargo, en otros estudios no se encontró diferencias significativas en el peso final, entre aquellos pacientes tratados con metilfenidato y los controles (2). Se ha sugerido que el descenso en el peso pudiera ser parte del mismo síndrome de déficit de atención y no consecuencia de la terapia con metilfenidato (14).
Aún no se conoce bien el mecanismo de acción del metilfenidato sobre el ADHD; tal vez produce un efecto estimulante sobre el sistema de alerta del tronco cerebral y la corteza. El metilfenidato incrementa la dopamina extracelular en el cerebro bloqueando transportadores de dopamina, los cuales han sido asociados con sus efectos terapéuticos (15). Después de una dosis oral, el efecto máximo sobre la conducta ocurre cuando la concentración sérica alcanza su máximo para luego declinar, con un 50% del máximo a las 2-3 horas. En escolares se pueden requerir de 2-3 dosis diarias (16); esto exige más adecuadamente una formulación de liberación prolongada que pueda ser administrada una vez al día, con un mejor perfil de farmacocinética. La dosis óptima de metilfenidato para niños con ADHD está entre 5 y 20 mg por administración. Algunos niños pequeños pueden requerir mayores dosis y algunos niños grandes pueden requerir dosis pequeñas, el ajuste por peso no cuenta en este campo. No hay diferencias en la absorción y metabolismo, los niños que responden a bajas dosis (5 mg por administración) tienen bajas concentraciones séricas de metilfenidato (4-5 ng/mL al T max) y aquellos que responden a altas dosis (20 mg por administración) tienen altas concentraciones séricas (12-15 ng/mL) (17).
No se conocen los mecanismos por los cuales el Zn puede contribuir a aumentar los efectos terapéuticos del metilfenidato. Se conoce que el Zn juega un rol significativo en la modulación de la neurotransmisión tanto en los receptores de membrana como en los canales; dentro de estos mecanismos, el Zn interactúa inhibiendo al transportador de dopamina (18-22). Por otra parte, el zinc modula algunas áreas específicas del cerebro relacionadas con el movimiento. Estudios experimentales en ratas muestran que el Zn se encuentra en altas concentraciones en el globus pallidus en el sistema nervioso central y participa en la modulación de la neurotransmisión a nivel de los receptores del ácido gama aminobutírico (GABA) (19). Finalmente algunos estudios preclínicos han demostrado la relevancia de receptores adrenérgicos alfa 2A en los procesos de atención y en los mecanismos de activación provocados por el metilfenidato (20).
Se han observado algunas diferencias en el efecto del metilfenidato de acuerdo a género. Las mujeres tienen una respuesta estadísticamente superior 1,5 horas post dosis y una respuesta inferior a las 12 horas del inicio en relación, con los varones; no hay estudios que hayan evaluado el eventual efecto de la formulación farmacológica del metilfenidato en la respuesta diferencial por género (21).
En resumen, parece haber una interacción entre metilfenidato y zinc en niños con síndrome con déficit de atención e hiperactividad, donde las dosis habituales de metilfenidato influyen en una disminución de las concentraciones plasmáticas de Zn y a su vez la suplementación con Zn aumenta el efecto favorable del metilfenidato sobre el comportamiento asociado al síndrome de déficit de atención e hiperactividad. Se justifica avanzar en nuevos estudios controlados, doble ciego de suplementación con Zn y que analicen componentes específicos del síndrome de déficit de atención e hiperactividad.
Nuestros sinceros agradecimientos a Angélica Letelier (TM) por los análisis de Zn plasmático y a Alejandra Ávila (enfermera universitaria) quien con una excelente disposición realizó la obtención y almacenamiento de las muestras de sangre para el análisis de Zn de nuestros pacientes.
Recibido 12-11-2010
Aceptado: 10-06-2011