Debido a la complejidad de la enfermedad renal, su tratamiento nutrimental es complicado y muchos alimentos se encuentran restringidos, entre ellos el pescado, por su contenido de fósforo. El objetivo del presente estudio fue cuantificar en el filete de diez especies de pescado, de consumo cotidiano en México: (Cyprinus carpio carpio, Ophichthus rex, Symphurus elongatus, Eucinostomus entomelas, Chirostoma patzcuaro, Bairdiella chrysoura, Salmo salar, Oreochromis urolepis hornorum, Sphyraena guachancho, Istiophorus albicans), el contenido de fósforo (P), proteína (Pr), colesterol, sodio, potasio, vitaminas D3 y E y ácidos grasos n-3 (EPA+DHA); para identificar, aquellos pescados que podrían ser incluidos en la dieta renal. Los análisis se realizaron de acuerdo a las técnicas del AOAC. Con los resultados se calcularon las relaciones entre los nutrimentos benéficos (EPA+DHA, vitaminas) y limitantes (Pr, P, colesterol). Los valores de proteína variaron entre 16.5 y 33.5g/100g de filete; el pescado con mayor contenido de fósforo fue Salmo salar y con menor Symphurus elongatus. La cantidad de EPA+DHA varió desde 79.64mg/100g hasta 1,381.53mg/100g. Tomando en cuenta la relación P/g de Pr recomendada para pacientes renales, todas las especies analizadas exceptuando Salmo salar, Ophichthus rex y Istiophorus albicans pueden ser incluidas en la dieta dependiendo de la etapa de la enfermedad. Considerando la relación entre P/EPA+DHA, las especies recomendadas para el paciente renal son Symphurus elongatus, Bairdiella chrysoura, y Sphyraena guachancho.
Palabras clave: Pescado, dieta renal, ácidos grasos n-3 EPA+DHA, proteína, fósforo.
Because renal disease is highly complex, its nutritional treatment is complicated and many foods are restricted, including fish because its phosphorus content. The aim of the present study was to analyze ten fillet fish species, commonly consumed in Mexico (Cyprinus carpio carpio, Ophichthus rex, Symphurus elongatus, Eucinostomus entomelas, Chirostoma patzcuaro, Bairdiella chrysoura, Salmo salar, Oreochromis urolepis hornorum, Sphyraena guachancho, Istiophorus albicans), to determine their phosphorus (P), protein (Pr), cholesterol, sodium, potassium, vitamins D3 and E, and n-3 PUFA (EPA+DHA) according to the AOAC techniques, in order to identify which species could be included in renal diet; particularly because of their risk:benefit relations (calculated with those results). Protein values ranged from 16.5 to 33.5g/100g of fillet; the specie with the highest phosphorus contest was Salmo salar, and with the lowest, Symphurus elongatus. EPA+DHA quantity ranged from 79.64mg/100g to 1,381.53mg/100g. Considering de P/Pr relation recommended to renal patients, all analyzed species (except Salmo salar, Ophichthus rex and Istiophorus albicans) could be included in their diet. As for the P/EPA+DHA relation, the species most recommended to renal patients are Symphurus elongatus, Bairdiella chrysoura and Sphyraena guachancho.
Key words: Fish, renal diet, fatty acids n-3 EPA+DHA, protein, phosphorus.
Departamento de Nutrición Animal. Dirección de Nutrición. Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. México, D.F., México.
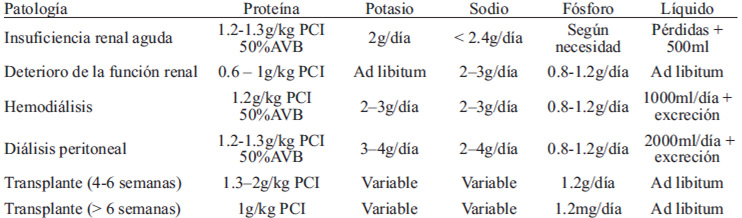
En el tratamiento de las enfermedades renales es necesario el manejo médico y nutrimental, por el gran impacto que tienen sobre la calidad de vida del paciente, ya que la mayoría de ellos presentan desnutrición energético-proteica al inicio de la terapia sustitutiva (diálisis) (1). Por lo tanto, existen varias recomendaciones nutrimentales para el tratamiento de diversas patologías renales; entre las más conocidas están las de la Fundación Nacional del Riñón de los Estados Unidos (National kidney Foundation) (Tabla 1 (2)). La literatura sugiere que una buena terapia nutrimental es esencial para tratar y disminuir las comorbilidades asociadas a la enfermedad renal, tales como desnutrición, factores de riesgo cardiovasculares y retraso de la progresión del daño renal (1).
Normalmente, en el manejo nutrimental de las enfermedades renales se prescribe una restricción de proteína, fósforo y potasio, la cual debe ser individualizada, tomando en cuenta las condiciones físicas e indicadores clínicos de cada paciente (Tabla 1). Debido a lo anterior, la proteína más recomendada en la dieta del paciente renal es aquella de alto valor biológico. Este tipo de proteína se encuentra en los alimentos de origen animal, entre los cuales, el pescado es considerado como un alimento con proteína de alto valor biológico pero con alto contenido de fósforo en muchas de sus especies (>160 mg/porción de 85g o 3 oz.) (3-6). Algunos estudios han demostrado que existen especies de pescado que por su bajo contenido de fósforo (<110mg/porción) pueden incluirse en la dieta renal (3,4,7).
El pescado, además de proporcionar proteína de alto valor biológico, es la principal fuente alimenticia de los ácidos grasos poliinsaturados n-3 (AG n-3): ácido eicosapentaenoico y ácido docosahexaenoico, conocidos por sus siglas en ingles como EPA y DHA (8,9). Estos AG n-3 son importantes antiinflamatorios, debido a que desplazan en el metabolismo al ácido araquidónico, un potente pro-inflamatorio. Los procesos inflamatorios son en parte responsables de la hipoalbuminemia, prurito, resistencia a la eritropoyetina, nefropatía por inmunoglobulina A y nefritis lúpica (10). El uso de los AG n-3 ha recibido mucha atención en los últimos años debido a sus posibles aplicaciones terapéuticas renales, tales como: retraso de la progresión de la enfermedad, mejora de la hipertrigliceridemia, disminución de la enfermedad cardiovascular, trombosis y aumento de niveles de albúmina (10,11).
Existen pocos estudios epidemiológicos que traten sobre la incidencia y prevalencia de las enfermedades renales en América latina, particularmente en las primeras etapas de la Insuficiencia Renal Crónica (IRC). En Argentina la prevalencia de pacientes que se encuentran en tratamiento de diálisis, aumenta alrededor de 6 – 8% cada año, lo que significa que más de 24,000 pacientes se encuentran en este tipo de terapia (12). Esta cifra es alarmante si se considera que por cada paciente en terapia sustitutiva hay aproximadamente 100 pacientes con los primeros estadios de IRC (12). En Colombia se estima que aproximadamente el 12% de la población padece alguna enfermedad renal, cifra que tiene un gran impacto social y económico en las familias involucradas y en el sector salud de cada país (13).
Siendo la enfermedad renal, al igual que sus complicaciones, un problema de salud pública, es importante establecer estrategias eficaces de prevención y manejo de dichas patologías (13), que abarquen tanto aspectos médicos como nutrimentales. Es por esto, que el objetivo del presente estudio fue analizar, evaluar e identificar de entre 10 especies de pescado, de consumo cotidiano en México, aquellas que podrían incluirse en la dieta del paciente renal.
Se analizó la porción comestible (filetes sin espinas) de 10 especies de pescado de consumo cotidiano en México. En la Tabla 2 se presenta el nombre científico de cada especie; así como, los nombres comunes con que se conoce en algunos países de América latina y España (14).
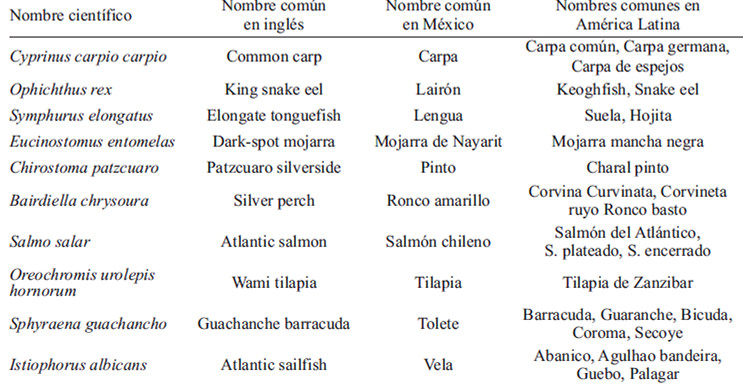
Las muestras se obtuvieron del Mercado de Pescados y Mariscos “La Nueva Viga” en la Ciudad de México; este es el mercado de productos pesqueros más grande de Latinoamérica (7). De cada especie se obtuvieron diversos ejemplares para alcanzar un mínimo de 15 pescados de cada una, los cuales se filetearon para obtener la porción comestible equivalente a filete sin espinas crudo. Los filetes se molieron y homogeneizaron para posteriormente obtener al azar 100 g para llevar a cabo los análisis químicos por triplicado (7).
Los análisis de proteína se llevaron a cabo de acuerdo al método descrito por la Asociación Oficial de Químicos Analíticos, conocida por sus siglas en inglés como AOAC (método: 976.04/920.05/977.14), (15). Para la proteína se utilizó un equipo automático (kjeltec 1035, Tecator, Ho¨gana¨s, Suecia); para el análisis del contenido de fósforo se siguió el método N968.08(b) de la AOAC, con un espectrofotómetro marca Beckman, modelo Du70; El sodio y el potasio fueron digeridos en un sistema de microondas con un horno PerkinElmer/Anton-Parr Multiwave 3000 y analizados mediante espectrofotometría de absorción atómica en un equipo PerkinElmer, modelo AAnalyst 800, según métodos 976.25 y 965.17 de la AOAC, respectivamente (15).
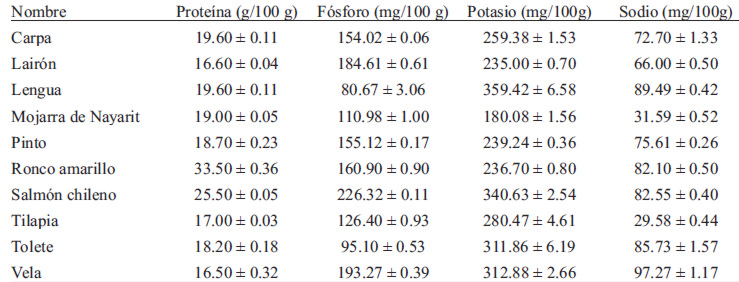
Se cuantificaron las vitaminas D3 y E, utilizando un HPLC de acuerdo con los métodos propuestos por keller (16). El contenido lipídico (lípidos totales) se llevó a cabo con una extracción con solventes orgánicos, mientras que los ácidos grasos n-3 se identificaron por cromatografía de gases (7). Para la determinación de colesterol se utilizó la técnica descrita por la AOAC (15). Se presenta la media de tres repeticiones; y los resultados de los nutrimentos analizados se agruparon en tablas descriptivas (Tablas 3 y 4). Posteriormente, se calculó la relación existente entre los nutrimentos benéficos y los limitantes por gramo de proteína y mg de fósforo (Tabla 5).
De aquí en adelante y para fines prácticos se utilizan los nombres comunes de los pescados en México (Tabla 2).
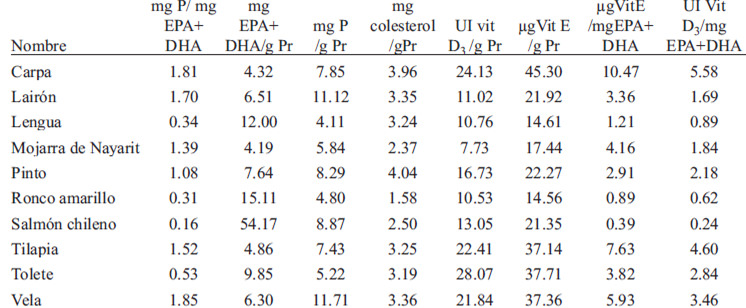
En las Tablas 3 y 4 se presentan los nutrimentos de las especies de pescado analizadas. La proteína (Pr) se cuantificó en un intervalo desde 16.5g/100g de filete (Vela) hasta 33.5g/100g de filete (Ronco amarillo); el 80% de las especies presentó menos de 20g Pr/100g de filete. El pescado con menor contenido de fósforo (P) fue Lengua (80.67 mg/100g de filete); mientras que únicamente el Salmón chileno presentó un contenido de P mayor a 200 mg/100g de filete (226.32mg/100g), lo cual lo clasificaría como un alimento con alto contenido de fósforo (>160 mg/porción de 85g) (3). Cuatro especies de pescado reportaron un contenido de P menor a 150mg/100g de filete, lo que las clasifica como bajas en fósforo (3). El contenido de potasio (k) se encontró en un intervalo desde 180.08 mg/100g (Mojarra de Nayarit) hasta 359.42 mg/100g (Lengua); el 40% de las especies presentó valores de k mayores a 300mg/100g. Considerando el contenido de sodio (Na) de las especies analizadas, todas presentaron valores bajos; Tilapia fue la que menor contenido reportó, con tan sólo 29.58 mg/100g, mientras que en Vela se encontró la mayor concentración (97.27mg/100g). Todas las especies aportan menos del 5.6% de la cantidad recomendada de Na (Tabla 1).
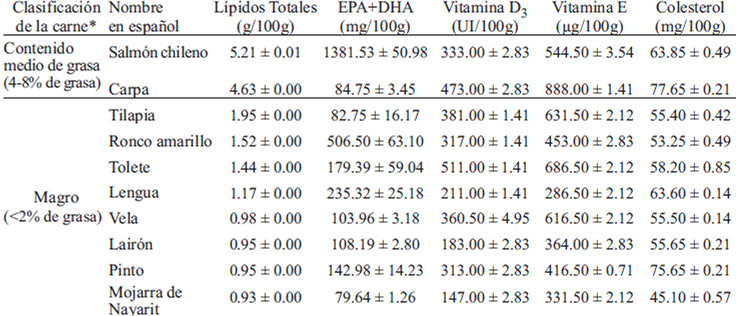
Tomando en cuenta el contenido total de lípidos (Tabla 4), el 80% de las especies fueron especies magras, con un contenido de grasa menor al 2.0% (17); y únicamente dos especies (Salmón chileno y Carpa) se consideran especies con contenido medio de grasa o semigrasas, pues presentaron un contenido de grasa entre 4.0 y 8% (17). Asimismo, los pescados estudiados presentaron una gran variedad en su contenido de EPA+DHA, siendo el valor mínimo encontrado de 79.64mg/100 g de filete en Mojarra de Nayarit, y el valor máximo de 1381.53mg/100g en Salmón chileno. El 30% de las especies presentó cantidades elevadas de estos ácidos grasos (>200mg/100g); y con igual porcentaje de especies para valores por debajo de 100mg/100 g de filete.
El contenido de vitamina D3 se presentó en un intervalo desde 147 UI/100g (Mojarra de Nayarit) hasta 511 UI/100g (Tolete). Mientras que se observó un intervalo mayor en el contenido de vitamina E, desde 286.5μg /100g (Lengua) hasta 888 μg/100g (Carpa); el 60% de las especies presentó valores entre 400 y 700 μg/100g.
En todas las especies analizadas, el colesterol presentó concentraciones por debajo de 80mg/100 g de filete, siendo Mojarra de Nayarit el pescado con el menor contenido de colesterol (45.1mg/100g).
En la tabla 5 se presenta la relación entre los nutrimentos limitantes y benéficos para pacientes renales, de las especies analizadas, donde se observa que las relaciones que pudieran tener mayor impacto en los pacientes fueron: P/EPA+DHA, EPA+DHA/Pr y P/Pr. El 40% de las especies analizadas reportó un bajo aporte de P en relación a la cantidad de EPA+DHA. Considerando la relación entre estos ácidos grasos y la proteína, tres especies presentaron una cantidad mayor a 10mg de EPA+DHA por cada gramo de proteína (Lengua, Ronco amarillo y Salmón chileno). El contenido de P por gramo de proteína fue desde 4.11 (Lengua) hasta 11.71 (Vela).
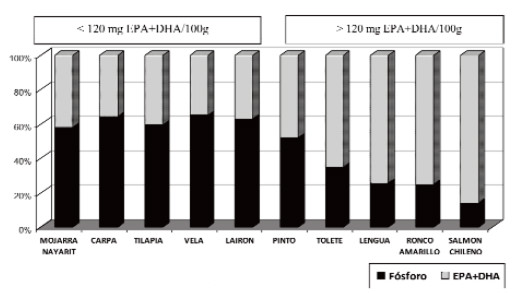
La figura 1 representa de manera porcentual el aporte de P y EPA+DHA, a modo de poder detectar aquellas especies con un menor índice riesgo/beneficio para la dieta del paciente renal; éste índice presentó valores mayores a 1 para las siguientes seis especies: 1.39 - Mojarra Nayarit, 1.82 – Carpa, 1.47 – Tilapia, 1.86 – Vela, 1.70 – Lairón, 1.08 – Pinto. Con índices menores a 1 se encontraron: Tolete - 0.53, Lengua – 0.34, Ronco amarillo 0.33 y Salmón chileno – 0.16.
La discusión se llevó a cabo considerando las restricciones nutrimentales más estrictas, según la National kidney Foundation, para Insuficiencia Renal Crónica en estadios avanzados (etapas 4 y 5). Los pescados con valores de proteína, fósforo, potasio y sodio que están dentro del intervalo de restricción más severo, serán potencialmente benéficos para pacientes con cualquier otra enfermedad renal, donde las restricciones son menos severas. Por lo tanto, cuando en el presente trabajo se utilice el término Insuficiencia Renal Crónica (IRC), se hará referencia a las últimas etapas de la Insuficiencia Renal; mientras que la expresión Enfermedad Renal englobará distintas patologías del riñón.
La enfermedad renal, en cualquiera de sus variantes, es una patología muy compleja a la que se asocian numerosas comorbilidades que repercuten en el estado de salud, estado nutrimental y calidad de vida del paciente (7,18). Por lo tanto, su manejo médico y nutrimental debe orientarse no sólo al tratamiento del daño renal, sino también a la prevención de las complicaciones asociadas a éste. Asimismo, considerando las altas tasas de desnutrición energético-proteica que caracteriza a muchos de estos pacientes, otro de los objetivos de la terapia médica nutrimental debe ser mantener un buen estado nutricio (19).
Los planes de alimentación para los pacientes renales normalmente prescriben una restricción en el aporte de proteína, la cual debe ser calculada individualmente considerando la patología y condiciones particulares de cada paciente (Tabla 1); asimismo, es importante considerar que la mayor parte de la proteína que se aporte sea de Alto Valor Biológico (AVB) (20). El pescado provee proteína en cantidad y calidad similares al compararlo con otros productos de origen animal (carne de res, pollo, cerdo) (4,21).
Tomando en cuenta la cantidad sugerida por el Sistema de Alimentos Equivalentes para Pacientes Renales (4), todas las especies analizadas proporcionan entre 13.2g/porción de 80g hasta 27g/porción de 80 g. (Tabla 3), correspondiente a dos equivalentes por comida en un paciente con IRC, sin embargo, se debe tomar en cuenta que la cantidad sugerida debe ser personalizada de acuerdo a los requerimientos diarios y condiciones clínicas de cada paciente.
La cantidad de fósforo administrada a estos pacientes también debe ser estrechamente monitoreada, por lo que comúnmente se presenta una restricción de dicho nutrimento. Se ha reportado que niveles elevados de fósforo en la sangre se asocian a los índices de mortalidad en los pacientes renales, por lo que es importante que se mantenga en el plasma entre 2.7 y 4.6mg/dL (22). El aporte de fósforo puede llegar a restringirse hasta 800 mg/día, en pacientes con insuficiencia renal crónica de estadios avanzados; para calcular la cantidad permitida, se deben considerar la patología, los fármacos y las terapias de reemplazo a las que dichos pacientes son sometidos (22) (Tabla 1). Tomando en cuenta la clasificación de alimentos por su contenido de fósforo se asume que el 40% de los pescados corresponderían al grupo de bajos en fósforo (<110mg/porción de 85g) (Lengua, Tolete, Mojarra Nayarit y Tilapia) (3), 40% pertenecen al grupo de alimentos moderadamente altos en fósforo (110-160mg/85g) (Carpa, Pinto, Ronco amarillo y Lairón) y 20% son alimentos altos en fósforo (>160mg/85g) (Vela y Salmón chileno).
Sin embargo, debido a que las principales fuentes de proteína son alimentos de origen animal con un importante aporte de fósforo, en la dieta renal se debe considerar, no sólo la cantidad de fósforo que aportan, sino la relación fósforo:proteína de los alimentos (23). Una relación menor a 10mg P/g de proteína se sugiere como la cantidad permitida en el tratamiento nutrimental, para asegurar un adecuado aporte de ambos nutrimentos y prevenir el riesgo de desnutrición (23). De las especies analizadas, dos tienen una relación por encima de lo recomendado (Lairón y Vela) (Tabla 5), sin embargo y aunque el Salmón chileno presentó valores de 8.87mg de P/g de proteína, se deberá tomar en cuenta su elevada cantidad de fósforo, como se menciona en el párrafo anterior; el resto de las especies podría formar parte de la alimentación de los pacientes renales.
El sodio y el potasio, son otros minerales que además deben ser monitoreados en los pacientes renales (20,24), debido a que la enfermedad ocasiona desequilibrios hidroelectrolíticos, además de que normalmente está acompañada de hipertensión, dislipidemia, enfermedad cardiovascular, cerebrovascular o diabetes. En pacientes que no padecen problemas hipertensivos el consumo de sodio no parece afectar la función renal (25), aunque se debe monitorear su consumo ya que normalmente sobrepasa la recomendación de <2,000mg/día (25). Sin embargo, pacientes renales que además padecen diabetes deben restringir su consumo de sodio, pues un consumo elevado de dicho mineral se ha asociado a progresión de la enfermedad e incluso a mayor mortalidad (25). De las especies analizadas, todas aportan menos de 100mg de Na en 80g de filete, lo que representa menos del 6% de la recomendación. El aporte de potasio debe ser de 2 a 3g/día para pacientes con deterioro renal (Tabla 1), y todas las especies analizadas proveen menos del 10% de la cantidad permitida (Tabla 3).
La principal causa de mortalidad de las enfermedades renales es la alta prevalencia de enfermedad cardiovascular que afecta a los pacientes (11), pues tienen una mayor incidencia de ateroesclerosis, hipertensión, dislipidemias, trombosis, eventos cardiovasculares, entre otros (24). Al respecto Foley y sus colaboradores (26), encontraron que el 75% de los pacientes renales padece anormalidades cardiacas y circulatorias, pues muchos de los riesgos cardiovasculares de dichos pacientes son consecuencia del daño renal (23,26); parte fundamental del tratamiento de la enfermedad renal es prevenir este tipo de comorbilidades. El consumo cotidiano de ácidos grasos n-3 (particularmente EPA y DHA) tiene beneficios cardiovasculares (11), y efectos positivos en los lípidos sanguíneos, presión arterial y función vascular, además de que disminuye el prurito y retraso del daño renal, especialmente en la nefropatía por IgA (10,27). Siendo el pescado la principal fuente alimenticia de estos ácidos grasos (7) su consumo debe promoverse en aquellos individuos vulnerables al desarrollo de enfermedad cardiovascular, entre los que se encuentran dichos pacientes. La recomendación para el consumo de los ácidos n-3 es del 0.6-1.2% de la energía total diaria, y 10% de esta cantidad debe provenir de EPA y DHA (28), aunque la cantidad puede variar entre 1 y 8g (10). Un consumo menor a los 3g/día de EPA+DHA, es poco probable que cause alguna toxicidad en el organismo (28). Asimismo, la Sociedad Americana del Corazón (American Heart Association) recomienda cuando menos el consumo de 1g/día de EPA y DHA (28-30). Los pescados analizados proveen desde 79.64mg EPA+DHA/100g de filete (Mojarra de Nayarit) hasta 1381.00mg EPA+DHA/100g de filete (Salmón chileno), sin embargo, no se debe olvidar la cantidad elevada de fósforo presente en éste último, razón por la cual a pesar de su elevado contenido de éstos ácidos grasos, su consumo no se recomienda; el Ronco amarillo aporta más del 50% de la recomendación diaria de EPA+DHA en un filete de 100g (Tabla 4); el 40% de las especies aportan entre el 10 y 20% de la recomendación, 30% aportan menos del 10% y una de las especies aporta por 100g de filete más del 23% de lo recomendado (Lengua).
De acuerdo a la clasificación de kocatepe y cols. (31), Ronco amarillo, Lengua y Salmón chileno se consideran excelentes fuentes alimenticias de EPA+DHA (>210mg/100g) para la población en general, y dos especie (Pinto y Tolete) son buenas fuentes de estos ácidos grasos (>120mg/100g de filete), sin embargo, para pacientes renales el salmón no es recomendable por su contenido de fósforo y potasio (Tabla 3).
Los pacientes con enfermedad renal están en riesgo de desarrollar deficiencias de otros micronutrimentos como las vitaminas, por lo que éstas no deben olvidarse en su tratamiento nutrimental (32). La deficiencia de vitamina E y D3 en los pacientes renales no es tan común como la de otros micronutrimentos. En el caso de la vitamina E, se ha reportado que sus niveles plasmáticos disminuyen durante la hemodiálisis y diálisis peritoneal ambulatoria crónica (32), por lo que se debe vigilar su adecuado aporte en la alimentación. No existe una recomendación de ingesta de las vitaminas E ni D3 para los pacientes renales, pero la ingesta máxima superior actual de vitamina E es de hasta 4 mg/día (30,32). De los pescados estudiados, ninguno es una fuente rica de dicho nutrimento (Tabla 4), con valores desde 229.2 hasta 710.4 μg/80 g de filete. En cuanto a la vitamina D3, los pacientes renales no están en riesgo de desarrollar deficiencia o toxicidad de dicho micronutrimento (32) y la ingesta recomendada es de 400UI/día (33). Las especies estudiadas aportan desde 117.6 (Mojarra de Nayarit) hasta 408.8 (Tolete) UI/en 80g, lo que representa desde 29.4% hasta 102.2% de la recomendación diaria.
La relación entre los nutrimentos benéficos y limitantes de los pescados analizados (Tabla 5), permite determinar cuáles son las especies más recomendadas para los pacientes renales con la restricción más estricta. Los pescados recomendados con una relación <10mg de fosforo/g proteína son: Carpa, Lengua, Mojarra, Ronco Amarillo, Tilapia y Tolete, de los cuales los más ricos en ácidos grasos omega 3 (> 210mg/100g como fuente excelente) son: Ronco amarillo, Tolete y Lengua y como fuente buena >120mg/100 es el Pinto. En relación al contenido de EPA+DHA por gramo de proteína los más recomendados son: Lengua y Ronco amarillo.
Considerando el aporte de EPA+DHA de las especies y la cantidad de fósforo que contienen (Tabla 5), el 40% de los pescados presentados se podría recomendar para dichos pacientes (Tolete, Lengua, Pinto y Ronco amarillo), por su relación P/EPA+DHA < a 1.2. De acuerdo a su clasificación las especies recomendadas son magras (Tabla 4). De igual modo, estas misma especies son las que más EPA+DHA aportaron en relación a su contenido de proteína (Tabla 5), y su consumo cotidiano en pacientes renales no implicaría riesgos para su salud. En esta recomendación se excluye al Salmón como recomendable ya que los valores de fósforo encontrados en el presente trabajo para este pescado fueron los más elevados (226mg/100g), además si tomamos en cuenta lo informado por otros autores, la concentración de fósforo podría ser aún mayor (desde 283 hasta 361mg/100g), además de contener valores de potasio elevados de hasta 371mg/100g (34, 35).
La Figura 1 representa gráficamente el contenido porcentual de los dos nutrimentos que podrían suponer un riesgo/beneficio del consumo de pescados para los pacientes renales: fósforo/EPA+DHA. A excepción del Salmón chileno, como ya se mencionó, se podría recomendar con mayor margen de seguridad para pacientes renales el consumo de Pinto, Tolete, Lengua y Ronco amarillo, pues aportan, un menor riesgo por su menor concentración de fósforo y un mayor beneficio por ser una fuente natural de ácidos grasos n-3 (>120 mg EPA+DHA/100g). Estas cuatro especies tuvieron un coeficiente P/EPA+DHA de 1.08, 0.53, 0.34 y 0.31, respectivamente (Tabla5). El resto de las especies en la Figura 1 presentó coeficientes superiores a 1.39. Esta representación gráfica se presenta con el objetivo de tener una visión general de dos grupos de nutrimentos importantes en la dieta renal, sin embargo, dado el impacto que la concentración de fósforo tiene en la progresión del daño renal, no se debe perder de vista que aunque un pescado pareciera ser el mejor, como en el caso del Salmón chileno, su riesgo se enmascara por la alta concentración de sus ácidos grasos n-3.
Sin embargo, debido a la gran variedad en la concentración de los nutrimentos de los pescados, todos podrían aportar algún beneficio a los pacientes con Enfermedad Renal Crónica, de acuerdo a la patología y comorbilidades que presenten; por ejemplo, en aquellos pacientes sometidos a terapia sustitutiva (diálisis), cuyos requerimientos de ciertos nutrimentos (proteína, fósforo, energía, Na, Fe, Ca, etc.) se encuentran elevados, el incluir aquellas especies de pescado con un mayor contenido de fósforo, podría ser viable de formar parte de su dieta. Es importante que todos los planes de alimentación sean calculados de manera individualizada y deben ser el resultado de evaluaciones del estado de salud y nutrimental de cada paciente; asimismo, no se debe olvidar que además de las grandes variaciones existentes entre especies de pescado, su aporte nutrimental puede variar de acuerdo a la estación y a la región geográfica de la especie (33).
Debido a la gran variedad de nombres con que se conoce una misma especie en diferentes lugares del mundo (Tabla 2), es importante tomar en cuenta el nombre científico al momento de seleccionar el tipo de pescado que se recomendará, ya que esta nomenclatura es universal.
En conclusión, por su bajo contenido de proteína y fósforo, los pescados más recomendables son: Lengua, Mojarra de Nayarit y Tolete. Para pacientes con riesgo de comorbilidades cardiovasculares se recomienda el consumo cotidiano de Ronco amarillo, Tolete y Lengua por su bajo índice P/EPA+DHA, debido a que todo paciente renal tiene un alto riesgo cardiovascular, ya que la enfermedad renal crónica genera importante daño endotelial y en consecuencia cardiovascular, aumentando de manera importante la morbimortalidad cardiaca. Para pacientes renales con menor riesgo cardiovascular se sugiere incluir especies como las antes mencionadas además de Pinto, Tilapia y Mojarra de Nayarit, por su buena cantidad de EPA+DHA en relación a su proteína y su bajo contenido de fósforo. Finalmente, Salmón chileno, Lairón y Vela estarían contraindicados para pacientes renales por su elevado contenido de fósforo en relación a la proteína que aportan.
Los autores agradecen al Sr. Jorge Toral Peña, administrador del Centro de Abasto de Pescados y Mariscos La Nueva Viga, en la Ciudad de México, su contribución con todas las especies analizadas. Y a Sara Montaño, por el análisis de colesterol y vitaminas.
Recibido: 15-03-2012
Aceptado: 26-06-2012