El objetivo del estudio fue evaluar el efecto de un programa intensivo de cambio en el estilo de vida para el control de peso sobre la sensibilidad a la insulina en niños y adolescentes en el primer nivel de atención. El estudio incluyó a 42 niños y adolescentes de 9 a17 años (n=23 grupo intensivo, n=19 grupo control) que participaron en un estudio clínico aleatorizado para el tratamiento de obesidad. El programa intensivo de cambio en el estilo de vida incluyó consultas mensuales con el médico del primer nivel de atención, asesoría dietética con el nutriólogo (semanal los primeros 3 meses y luego mensual) y 12 sesiones grupales en un protocolo de cambio de conducta. El grupo control incluyó solamente las consultas médicas mensuales. La sensibilidad a la insulina se estimó por el índice de sensibilidad a la insulina (ISI(0,120)) al inicio y a los 6 meses de intervención. Los niños y adolescentes del programa intensivo mostraron un mayor efecto en la sensibilidad a la insulina a los 6 meses en comparación al grupo control ([media ± DE], + 46.8 ± 56 vs. + 5.6 ± 47, diferencia 41.2 [IC 95%, 8.5, 73.9], p= 0.01) y 65% lograron aumentar la sensibilidad a la insulina >9 unidades vs. 32% en el grupo control (p=0.03). Este estudio muestra evidencia preliminar que un programa intensivo de cambio en el estilo de vida puede ser un modelo alternativo para mejorar la sensibilidad a la insulina en los niños y adolescentes con obesidad en el primer nivel de atención.
Palabras clave: Resistencia a la insulina, obesidad, niños, primer nivel de atención.
The aim of this study was to evaluate an intensive lifestyle intervention for weight management among youth in a primary care setting on insulin sensibility, compared to a control group. The study included 42 youths 9-17 years old (n=23 intensive lifestyle intervention, n=19 control group) who completed a randomized trial for weight management in a primary care setting which included an oral glucose tolerance test. The intensive lifestyle intervention included monthly consultations with the primary care physician, nutrition counseling with a registered dietitian (weekly first 3 months and then monthly) and 12 group sessions in a behavioral change protocol. The control group attended monthly consultations with the primary care physician. Insulin sensitivity was estimated by the Insulin Sensitivity Index ISI(0,120) at baseline and 6 months posttreatment. At 6 months, the mean ± DE, increase in insulin sensitivity was greater in the intensive lifestyle intervention than the control group (+46.8 ± 56 vs. +5.6 ± 47, betweengroup difference 41.2 [CI 95%, 8.5, 73.9], p= 0.01). Sixty five percent of youths on the intensive lifestyle intervention increased insulin sensitivity over 9 units vs. 32% in the control group (p=0.03). This study shows preliminary evidence that an intensive lifestyle intervention program can be an alternative model to improve insulin sensitivity among youths in the primary care setting.
Key words: Insulin resistance, obesity, youth, primary care.
Centro de Investigación en Alimentación y Desarrollo A C.; Hermosillo, Sonora. Universidad de Sonora. Hermosillo, Sonora. Hospital Dr. Ignacio Chávez, Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado de Sonora. Hermosillo, Sonora, México.
En las últimas décadas han habido modificaciones importantes al sistema alimentario global, la mecanización y urbanización, lo cual ha repercutido sustancialmente en cambios en la dieta y actividad física (1). Lo anterior, aunado a la falta de intervenciones y regulaciones apropiadas, ha generado un ambiente obesogénico y un concomitante aumento en la obesidad en todas las edades alrededor del mundo. La obesidad en niños, tal como sucede en los adultos, puede llevar a un aumento en la resistencia a la insulina, que a su vez está relacionada con múltiples comorbilidades incluyendo diabetes tipo 2 (2, 3).
En estudios realizados en adultos se ha mostrado que a través de programas intensivos de cambio en el estilo de vida (PICEV) que incluyen protocolos de cambio de conducta y la participación de otros profesionales de salud, se puede prevenir la diabetes tipo 2 en un 58%, en personas en riesgo (4, 5). Dicho beneficio ha sido en buena medida por el mejoramiento en la sensibilidad a la insulina (6). Paralelamente, se están realizando estudios de intervención enfocados a mejorar la sensibilidad a la insulina en la población pediátrica con resultados prometedores. En este sentido, la pérdida de peso y el ejercicio han mostrado ser estrategias efectivas (7, 8). Sin embargo, se carece de intervenciones que puedan ser extrapolables a las condiciones del primer nivel de atención, especialmente en países en vías de desarrollo donde la carga por enfermedades derivadas de la obesidad es cada vez mayor.
El primer nivel de atención por su amplia cobertura a la población representa un punto estratégico para combatir la resistencia a la insulina y sus problemas asociados a través del tratamiento de la obesidad. No obstante, diversos estudios han mostrado que una alta proporción de los proveedores de salud de los niños y adolescentes, no diagnostican ni tratan la obesidad debido a diversas causas como la falta de tiempo, falta de herramientas para su manejo, así como la falta de protocolos efectivos (9) Nuestro grupo realizó un estudio clínico aleatorizado donde se evaluó un PICEV -un médico de primer contacto apoyado por el nutriólogo y un protocolo de cambio de conducta- vs. un grupo control en el tratamiento de la obesidad en niños y adolescentes en el primer nivel de atención. Al año de intervención, se encontró una diferencia de peso de 6.4 kg, 2.2 unidades de IMC (Índice de Masa Corporal, kg/m2) y 6.8 cm de cintura a favor del PICEV (10). Con la finalidad de evaluar el efecto del PICEV en la sensibilidad a la insulina, se invitó a los participantes a una prueba de tolerancia a la glucosa y mediciones de insulina al inicio y a los 6 meses de la intervención.
Los métodos, la intervención y el efecto del programa en el control de peso a 6 y 12 meses se han descrito previamente (10). El presente, es un análisis secundario del efecto del PICEV sobre la sensibilidad a la insulina en los niños y adolescentes que permanecieron en el estudio después de 6 meses del inicio de la intervención y que además contaron con mediciones de sensibilidad a la insulina. De los 76 niños y adolescentes que iniciaron el estudio (38 aleatorizados al PICEV y 38 al grupo control), hubo 26 deserciones a los 6 meses: 13 en el PICEV (causas: 5 nunca asistieron, 4 problemas para asistir, 2 no quisieron continuar, 1 pérdida de interés, 1 problemas familiares) y 13 en el grupo control (causas: 6 nunca asistieron, 2 no quisieron continuar, 3 pérdida de interés, 1 problemas familiares, 1 inconformidad con resultados). Adicionalmente, 2 niños del PICEV y 3 niños del grupo control no contaron con muestras para la estimación de la sensibilidad a la insulina y 3 niños del grupo control fueron descartados por mostrar datos de hipoglucemia (<65 mg/dL). La muestra final para el análisis incluyó a 42 niños (23 del PICEV y 19 del grupo control). Solamente se hicieron mediciones de sensibilidad a la insulina al inicio y a los 6 meses de la intervención.
Todos los participantes y sus padres otorgaron su consentimiento por escrito antes de participar en el estudio. El estudio fue aprobado por el comité de ética del Centro de Investigación en Alimentación y Desarrollo, A. C. (CIAD). Los participantes fueron reclutados en un periodo de 2.5 meses en el hospital Dr. Ignacio Chávez del Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado de Sonora el cual tiene dentro de sus instalaciones el área de primer nivel de atención. Este centro está ubicado en Hermosillo, una ciudad urbanizada del estado de Sonora en la región norte de México. El reclutamiento se hizo a través de folletos, anuncios, remisiones por médicos, anuncios en diario local y radio, y a través de la invitación a pacientes que participaron en un estudio transversal realizado por nuestro grupo.
Los criterios para participar en el estudio fueron los siguientes: tener entre 9 y 17 años de edad, un IMC mayor al percentil 95 basado en las tablas de crecimiento de los Centros para el Control y Prevención de Enfermedades de Estados Unidos (11) o un IMC mayor al percentil 90 además de una cintura mayor al percentil 90, padres o tutores con interés en el control de peso de sus hijos y disposición a asistir a sesiones educativas. Los criterios de exclusión incluyeron: intolerancia a la glucosa o diabetes tipo 2, enfermedades psiquiátricas, o cualquier otra condición médica que pudiera afectar la participación en el estudio; uso de medicamentos para la obesidad o la participación en cualquier programa de control de peso o de actividad física de forma estructurada. También se consideró como criterio de exclusión, la pérdida de peso en los últimos cuatro meses previos al estudio.
Las mediciones de las variables de interés se efectuaron en el periodo de un mes a todos los participantes en las instalaciones del CIAD. Posteriormente, un experto en estadística no involucrado con las mediciones o reclutamiento asignó aleatoriamente a los participantes 1:1 al PICEV o al grupo control mediante una aleatorización estratificada por sexo utilizando una secuencia de números generada por un programa de cómputo. El personal que midió el peso, la talla y la composición corporal (mediante absorcimetría dual de rayos X [DXA, por sus siglas en inglés]), así como los que efectuaron los análisis de laboratorio (glucosa o insulina), fueron cegados al grupo de asignación.
En la Tabla 1 se resumen los componentes del PICEV y el grupo control (10). El PICEV incluyó un programa de cambio de conducta, consultas de nutrición y las consultas médicas. El programa de cambio de conducta se basó en el programa Cambia el cual es un manual de trabajo con ilustraciones diseñado específicamente para niños y adolescentes (10). Dicho programa fue el resultado de la adaptación del programa Shapedown (12) y el cual se modificó sustancialmente tras efectuar 2 estudios piloto que incluyeron en total a 31 niños y adolescentes de diferentes niveles socioeconómicos de nuestra población.

El programa Cambia se implementó en 12 sesiones semanales de 2 horas durante los 3 primeros meses de la intervención. Las sesiones se conformaron por 10 niños/adolescentes aproximadamente, de edad similar y se llevaron a cabo bajo la dirección de un nutriólogo con experiencia en la implementación del programa. Los participantes eligieron sus propias metas respecto lograr mejoras en la actividad física y dieta con ayuda del instructor. Dichas metas se revisaron y renovaron en cada sesión. A lo largo del programa de cambio de conducta los niños utilizaron técnicas del cambio de conducta como el auto monitoreo (anotar en formatos especialmente diseñados la actividad física realizada en la semana, el tiempo viendo televisión o el apego a la dieta), establecimiento de metas (se proponían metas específicas y firmaban un compromiso), entre otras. En cada sesión se reconoció el logro de objetivos y se premió con una firma y elogios delante del grupo. Los niños fueron advertidos que se premiaría con un obsequio sorpresa (simbólico) al final del curso a los que obtuvieran una mayor cantidad de firmas. Todas las sesiones finalizaron con un breve tiempo para dinámicas o juegos a fin de hacer más atractivo el programa para los niños.
En la Tabla 1 se muestran los temas abordados en el programa de cambio de conducta. Paralelo a las sesiones con los niños y adolescentes, los padres asistieron a 6 sesiones donde se abordaron diversos temas de nutrición, el control de estímulos (modificar el ambiente del hogar en pro de estilos de vida más sanos [ejemplo, no comprar bebidas azucaradas o comida alta en grasas, entre otros]) y la importancia de el apoyo familiar para lograr los resultados. Los padres fueron motivados a ser modelos de sus hijos y perder peso en caso de que tuvieran exceso del mismo.
Los niños del PICEV asistieron también a consultas semanales con el nutriólogo durante los 3 primeros meses y posteriormente de forma mensual. Los niños recibieron una dieta individualizada de 1200 a 1800 kilocalorías dependiendo el peso y actividad física del niño/adolescente (10). Se usó el semáforo de salud como modelo de orientación en nutrición desarrollado por nuestro grupo, el cual integra el sistema mexicano de alimentos equivalentes. Además, el modelo utiliza los colores del semáforo para fomentar los alimentos ubicados en el color verde, no excederse en de color amarillo y limitar en lo posible los ubicados en el color rojo. Se promovió una pérdida de peso gradual o un mantenimiento del peso a la par con el crecimiento. El enfoque fue mejorar las conductas (dieta y actividad física) más que en llevar a cabo una dieta rígida. Los niños del grupo del PICEV no recibieron sesiones de ejercicio como parte de la intervención como se ha hecho en muchos estudios, sino que se trabajó en que fueran incrementando gradualmente su nivel de actividad física. Esto se hizo debido a que son las condiciones típicas de los centros de primer nivel de atención, donde no se cuenta con instalaciones para realizar actividad física. Adicionalmente, los niños del PICEV recibieron consultas médicas de 10-15 minutos cada mes donde fueron monitoreados en su percentil del IMC para edad y sexo, presión arterial u otros aspectos médicos, además de recibir reforzamiento y motivación para lograr el cambio de conducta.
En el grupo control los niños y adolescentes solamente recibieron consultas médicas mensuales de 10 a 15 minutos. En las consultas se monitoreó el percentil del IMC para edad y sexo. Las recomendaciones por los médicos consistieron en realizar progresivamente 30 minutos de actividad física la mayoría de los días de la semana, no ver la televisión por más de 2 horas y seguir una dieta acorde a la pirámide de alimentos (la cual se adaptó para contener alimentos típicos de la región). Se recomendó también a los padres que adoptaran patrones de alimentación sanos para facilitar el cambio de conducta en sus hijos. Los médicos que participaron en la implementación del estudio recibieron capacitación previa en obesidad antes del inicio de la intervención (10).
Se instruyó a los participantes a no hacer ejercicio o actividad física extenuante el día previo a las mediciones. Los niños y adolescentes se presentaron en la unidad metabólica del CIAD en ayuno. El peso se midió con una báscula digital (AND FV-150KA1, A&C Co Japan) y la talla con un estadiómetro calibrado (Holtain LTD. UK) (13) El IMC y el puntaje Z del IMC se obtuvieron mediante el programa Epi Info (versión 3.3.2, 2005. Centers for Disease Control and Prevention. Atlanta, GA, USA) (11). La cintura se midió a nivel de la cicatriz umbilical y en el punto medio entre la cresta iliaca y la última costilla. Ambas mediciones se efectuaron tanto en posición supina como de pie. En el presente trabajo se reportan los datos de cintura a nivel umbilical en posición supina debido a que el cambio en esta medición tuvo una mejor correlación con el cambio en la sensibilidad a la insulina. La grasa corporal se determinó mediante DXA utilizando un densitómetro, Lunar DPX-MD (GE Lunar Corporation, Madison, WI, US).
Se realizó una prueba de tolerancia a la glucosa a los participantes al inicio y a los 6 meses de la intervención. Se obtuvieron muestras de sangre en ayuno y a las 2 horas después de una carga con 75 g de glucosa (Glutol; Paddock Lab Inc. MN, USA). A partir de dichas muestras se obtuvieron los niveles de glucosa e insulina basales y posprandiales de 2 horas. La insulina se determinó por radioinmunoensayo utilizando el procedimiento Coat-A-Count (Iso-Data, IL USA) y la glucosa por el método de la glucosa oxidasa. A partir de los datos de glucosa e insulina se estimó el índice de sensibilidad a la insulina (ISI(0, 120)) con la siguiente fórmula: ISI(0, 120) = 75,000 + (Glucosa 0 – Glucosa 120) (mg/dl) X 0.19 X Peso corporal(kg)/120 X (media de glucosa (0, 120)) (mg/dl) X Log (media de insulina (0,120)) (mU/l) (14). El ISI(0, 120) ha sido validado contra el clamp euglucémico (14, 15). No se usó la insulina basal o estimaciones con fórmulas basadas en valores de insulina y glucosa basales (ejemplo HOMA-IR) debido su baja confiabilidad para estimar sensibilidad a la insulina en niños (16). Como un acercamiento a la maduración biológica de los niños y adolescentes, se mostró a estos una gráfica con los diferentes estadíos de Tanner para que ubicaran su propio desarrollo. No se hizo una valoración directa del estadío de desarrollo, ya que muchos niños y adolescentes podrían por pena a la evaluación, no participar en el estudio.
Los datos se muestran como medias y sus desviaciones estándar, errores estándar o intervalos de confianza al 95% según se especifique. Sin embargo, las diferencias entre grupos se analizaron mediante pruebas no paramétricas (Mann-Withney) cuando los datos no mostraron un comportamiento normal y con pruebas de t para muestras independientes cuando los datos tuvieron un comportamiento normal. La comparación de proporciones se evaluó con la prueba de chi-cuadrada comparando el porcentaje de niños o adolescentes entre grupos que lograron los mayores cambios en la sensibilidad a la insulina (>50 percentil de los cambios [equivale a un aumento >9 unidades de ISI(0, 120)]). También se efectuaron análisis de correlación de Spearman para ver las variables asociadas al cambio en la sensibilidad a la insulina. Se consideró un valor de p ≤ 0.05, utilizando pruebas de dos colas como criterio para indicar significancia estadística. Todos los análisis se efectuaron utilizando el programa NCSS 2007 (Number Cruncher Statistical System for Windows, Kaysville, UT, USA).
De los 76 niños y adolescentes que iniciaron el estudio (n=38, PICEV y n=38 grupo control), solamente 23 (60%) de los participantes aleatorizados al PICEV y 19 (50%) del grupo control permanecieron en el estudio y contaron con mediciones para estimar los cambios en la sensibilidad a la insulina a los 6 meses. No hubo diferencias significativas en las características basales entre los niños del presente estudio y los no incluidos (P > 0.05). La asistencia a las sesiones de actividades planeadas del estudio por parte de los niños y adolescentes del PICEV fue la siguiente: protocolo de cambio de conducta niños 77% y padres 62%, consulta con nutriólogo 68%, consulta médica 52%. En el grupo control la asistencia a las consultas médicas planeadas fue del 55%.
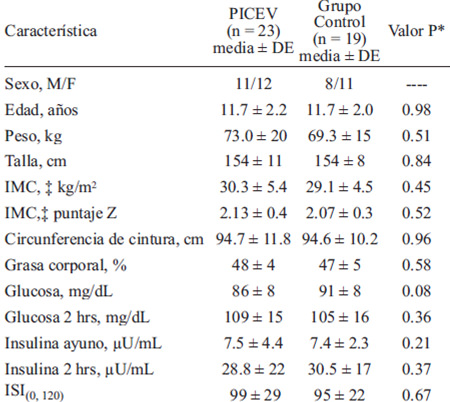
Tanto el PICEV como el grupo control fueron similares en sus características tras el proceso de aleatorización. Al inicio del estudio, no hubo diferencia en los años de estudio de los padres del PICEV y el grupo control (14.5±3.39 vs. 13.9±3.17; p=0.52), ni en el ingreso mensual (12,943±10,411 vs. 12,142 ±6,975 [pesos mexicanos]; p=0.71). Tampoco hubo diferencias significativas entre grupos en los parámetros de obesidad, glucosa basal, glucosa de 2 horas, insulina basal, insulina de 2 horas e ISI(0, 120) (Tabla 2). El estadío de Tanner reportado por los niños y adolescentes para el grupo PICEV y el grupo control respectivamente, fue de la siguiente manera: 1(21.7% vs. 21.1%), 2 (34.8% vs. 57.9%), 3 (21.7% vs. 5.3%), 4 (21.7% vs. 15.8%) y 5 (0% vs. 0%), p=0.33.
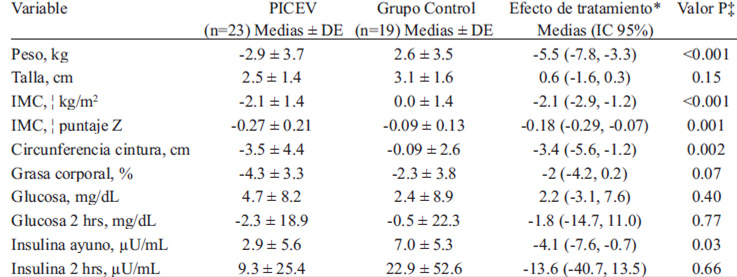
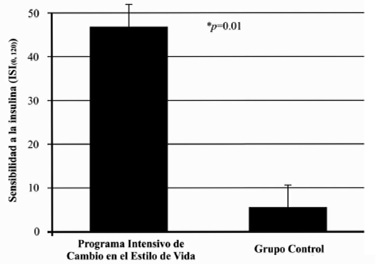
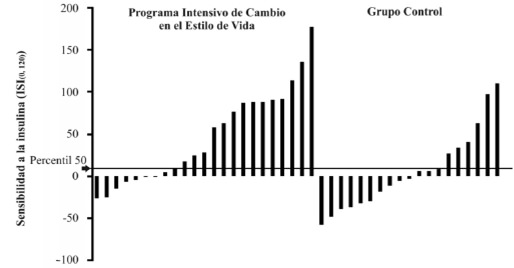
Después de 6 meses de intervención, los participantes del PICEV mejoraron los parámetros de obesidad e insulina en ayuno con respecto al grupo control, sin diferencias significativas en la talla, glucosa en ayuno y glucosa e insulina de 2 horas (Tabla 3). Tanto el grupo PICEV como el grupo control, mejoraron en promedio la sensibilidad a la insulina, (media ± DE) (+46.8 ± 56 vs. +5.6 ± 47, p= 0.01), diferencia entre grupos e IC95% (41.2 [IC 95%, 8.5, 73.9]). Sin embargo, el efecto del PICEV fue superior (Figura 1). Por último, más del doble de participantes del PICEV lograron los aumentar la sensibilidad a la insulina por arriba de 9 unidades (>50 percentil de los cambios) en comparación al grupo control (65% vs. 31.6%, p=0.03) (Figura 2).
El análisis de correlación de Spearman mostró una relación inversa entre el cambio en el ISI(0,120) y el cambio en la cintura (r= -0.30 p=0.05), mientras que con el cambio en peso, IMC y Z-IMC, la relación no alcanzó significancia estadística (r= -25 a -29, p> 0.05). Tampoco se observó una relación entre el cambio en porcentaje de grasa corporal total por DXA e ISI(0, 120) (r= -0.14 p=0.34).
Las enfermedades asociadas a la resistencia a la insulina están en los primeros lugares de morbilidad y mortalidad en muchos países en vías de desarrollo, por lo que es prioritario contar con intervenciones efectivas para mejorar la sensibilidad a la insulina que tengan un alto potencial pragmático. El presente estudio mostró que un PICEV —consultas por el médico y el nutriólogo y un protocolo de cambio de conducta—puede representar un modelo alternativo para mejorar los parámetros de sensibilidad a la insulina en el primer nivel de atención. Los participantes del PICEV mejoraron la sensibilidad a la insulina con respecto al grupo control y también una mayor proporción (65% vs. 31.6%) lograron mejorar la sensibilidad a la insulina por arriba de 9 unidades. En nuestro conocimiento, este es el primer estudio de intervención en niños y adolescentes con un efecto positivo en la sensibilidad a la insulina en el primer nivel de atención. Lo anterior representa una vía potencial para la prevención oportuna de diabetes y otras comorbilidades asociadas a la resistencia a la insulina.
Es difícil establecer comparaciones de resultados con otras intervenciones por las diferencias en los indicadores usados para la medición de sensibilidad a la insulina y por las variaciones en los protocolos para la medición de insulina. Sin embargo, nuestros resultados concuerdan con estudios realizados fuera del primer nivel de atención, que muestran que mediante la pérdida de peso a través de la dieta y/o actividad física se puede mejorar la sensibilidad a la insulina en niños y adolescentes (7, 8). A diferencia de otras intervenciones con efecto en la sensibilidad a la insulina, (7, 8) en nuestro estudio no se ofrecieron sesiones de ejercicio, debido a que en los centros de primer nivel de atención no se cuenta con instalaciones para actividad física. Es probable que de ofrecerse sesiones de ejercicio, el impacto del programa sobre la sensibilidad a la insulina podría ser aún mayor. Considerando que hubo una relación inversa entre el cambio en la circunferencia de la cintura y el cambio en ISI(0, 120), el principal efecto del PICEV sobre la circunferencia de la cintura pudiera ser una de las razones de la mejoría observada en la sensibilidad a la insulina.
La diferencia en los resultados de los dos modelos de intervención radica posiblemente en el contraste entre ambos modelos. El protocolo de cambio de conducta utilizado en el PICEV tiene fundamento en modelos teóricos de cambio de comportamiento (17) y abarca diversos factores claves en el control de peso (educación en nutrición, apoyo social, conciencia de riesgos, desarrollo de habilidades y el manejo de emociones, etc.) (10), lo cual es difícil de abordar con un modelo de tratamiento tradicional. Así mismo, el PICEV incluye el empleo de técnicas de cambio de conducta, tales como el auto monitoreo que ha mostrado eficacia en el tratamiento de obesidad en adolescentes (18). Además, la intensidad del PICEV fue mucho mayor que en el grupo control. Una revisión sistemática reciente sobre intervenciones para el tratamiento de obesidad en niños y adolescentes, encontró que solamente los programas completos (que incluyen apoyo en dieta, actividad física y técnicas conductuales) con una intensidad mínima de al menos 26 hrs de intervención, tienen un efecto positivo consistente en los parámetros de obesidad (19). El PICEV empleó un total de 33 hrs vs. <2 hrs el grupo control. Finalmente, la participación del nutriólogo como parte del equipo de tratamiento pudo ser otro elemento importante del PICEV. Son numerosas las intervenciones con resultados positivos en el control de peso y sensibilidad a la insulina tanto en niños (7, 20) como en adultos (4, 5, 21, 22) donde la participación del nutriólogo o un equipo multidisciplinario ha sido crucial. El ejemplo más ilustrativo es el programa de prevención de diabetes (22). Finalmente, también es importante mencionar que el PICEV es un programa especialmente diseñado para niños y adolescentes que incluye breves dinámicas y juegos de diversión para fomentar la permanencia, lo cual difiere con el concepto de la consulta tradicional.
El modelo de intervención que se ofrece para el tratamiento de obesidad en niños y adolescentes en la práctica clínica contrasta con el modelo del PICEV. Frecuentemente el tratamiento tradicional es de muy baja intensidad o no incluye algún protocolo de cambio de conducta validado o no involucra a profesionales en el área de la nutrición. Hay evidencia de que las intervenciones de ese tipo no tienen ningún efecto en el control de peso (tampoco se esperarían beneficios en sensibilidad a la insulina) (23, 24). Lo anterior debe considerarse para la definición de las prácticas o lineamientos en atención a la obesidad en niños y adolescentes, ya que el no considerarlo podría repercutir en el fracaso de éstas.
Una de las limitaciones del estudio es que solo se incluyó al 55% de los participantes aleatorizados al inicio. Aunque la deserción es un problema frecuente en las intervenciones en obesidad en niños y adolescentes (20, 25), ésta debe tomarse en cuenta ya que los que abandonan este tipo de estudios tienden a ser los participantes con menos apego y pérdida de peso, por lo que el efecto del programa en la sensibilidad a la insulina podría ser más conservador. Cabe mencionar que no hubo diferencias en las variables de inicio entre los que niños y adolescentes del presente estudio y los que no fueron incluidos.
El primer nivel de atención definido por el Instituto de Medicina como “la provisión de servicios integrados y accesibles por los clínicos responsables de tratar la gran mayoría de las necesidades de salud, desarrollando una relación sostenida con los pacientes y la práctica en el contexto de la familia y la comunidad” debe ser considerado como un elemento fundamental en el combate de la obesidad y la resistencia a la insulina si se pretende tener un impacto en reducir las comorbilidades asociadas en la población. El presente estudio muestra evidencia preliminar de que un programa intensivo de cambio en estilo de vida -que incluye al médico apoyado del nutriólogo y un protocolo de cambio de conducta- podría ser un modelo alternativo para mejorar la sensibilidad a la insulina en los niños y adolescentes con obesidad en el primer nivel de atención. Se requieren más estudios de intervención con programas intensivos de cambio en el estilo de vida a mayor escala para verificar la generalización de los resultados encontrados.
Recibido: 24-05-12
Aceptado: 24-10-12