Esta revisión de las recomendaciones de energía y nutrientes para la población Venezolana presenta los valores de hierro, yodo, zinc, selenio, cobre, molibdeno, vitamina C, vitamina E, vitamina K, carotenoides y polifenoles. Se adoptan definiciones internacionales de Ingestas Dietéticas de Referencia (DRIs por Dietary Reference Intakes) que incluyen: Ingesta Dietética Recomendada (RDA), Requerimiento Promedio Estimado (EAR), Ingesta Adecuada (AI) y Niveles de Ingesta Máximos Tolerables (UL). Las RDA para hierro: 11 mg/día para < 1 año, 7-10 mg/día niños, 8-11 mg/día para hombres, 8-18 mg/día para mujeres y 27 mg/día para embarazadas. RDA Yodo: 110-130 mg/día recién nacidos, 90-120 mg/día niños y adolescentes y 150 mg/día adultos, 220 mg/día embarazo y 290 mg/día lactancia. RDA Zinc: 2-3 mg/día < 1 año, 3-5 mg/día niños, 8-11 mg/día adolescentes y hombres, 8-9 mg/día adolescentes y mujeres, 12 mg/día para embarazadas y 13 mg/día durante la lactancia. RDA Vitamina C: 40-50 mg/día recién nacidos, 15-45 mg/día niños, 75 mg/día adolescentes masculinos, 65 mg/día adolescentes femeninas, 90 mg/día hombres y 75 mg/día mujeres, 80-85 mg/día embarazadas y lactancia 115-120 mg/día. También se presentan valores de cobre, selenio, molibdeno, vitaminas E, K, carotenoides y polifenoles. Estas recomendaciones contribuirán al diseño de políticas adecuadas y eficientes que puedan ayudar a evitar o a tratar las consecuencias derivadas de la deficiencia o el exceso de estos nutrientes.
Palabras clave: Hierro, yodo, zinc, selenio, cobre, molibdeno, vitamina C, vitamina E, vitamina K, carotenoides, polifenoles, Ingestas Dietéticas de Referencia, Ingesta Dietética Recomendada, Requerimiento Promedio Estimado, Ingesta Adecuada, Niveles de Ingesta Máximos Tolerables, Venezuela.
The review on iron, iodine, zinc, selenium, copper, molybdenum, vitamin C, vitamin E, vitamin K, carotenoids and polyphenols recommendations for Venezuela comprise the definitions adopted worldwide known as Dietary Reference Intakes (DRIs) that include Recommended Dietary Allowance (RDA), Estimated Average Requirement (EAR), Adequate Intake (AI) and Tolerable Upper Intake Levels (UL). The RDA for iron: 11 mg/day for infants < 1 year of age, 7 - 10 mg/day for children, 8-11 mg/day for males, 8-18 mg/day for females and 27 mg/day during pregnancy. RDA for iodine: 110-130 mg/day for infants, 90-120 mg/day for children and adolescents, 150 mg/day for adults, 220 mg/day for pregnancy and 290 mg/day during lactation. RDA Zinc: 2-3 mg/day for infants, 3-5 mg/day for children, 8-11 mg/day for male adolescents and adults, 8-9 mg/day for female adolescents and adults, 12 mg/day during pregnancy and 13 mg/day for lactation. RDA Vitamin C: 40-50 mg/day for infants, 15-45 mg/day for children, 75 mg/day for male adolescents, 65 mg/day for female adolescents, 90 mg/day for adult males, 75 mg/day for adult females, 80-85 mg/day during pregnancy and 115-120 mg/day during lactation. Recommendations for copper, selenium, molybdenum, vitamins E, K, carotenoids and polyphenols are also presented. These recommendations will help to design adequate and efficient policies that could help to avoid or to treat the consequences derived from the deficiency or the excess of these nutrients.
Key words: Iron, iodine, zinc, selenium, copper, molybdenum, vitamin C, vitamin E, vitamin K, carotenoids, polyphenols, Reference Dietary Allowances, Recommended Dietary Allowance, Estimated Average Requirement, Adequate Intake, Tolerable Upper Intake Levels, Venezuela.
Instituto Venezolano de investigaciones Cientificas, Fundación Bengoa, Universidad Central de Venezuela, ILSI Norandino, Universidad del Zulia, Industrias Parmalat, Universidad de los Andes, Organización Mundial de la Salud.
Las recomendaciones más recientes para la población, aparecen en el libro de “Valores de referencia de energía y nutrientes para la población Venezolana. Revisión 2000” (1). Como para ese entonces, lo mismo que actualmente, no había suficientes datos nacionales para establecer las recomendaciones Venezolanas, que están basadas en las RDA (Recommended Dietary Allowances) de Estados Unidos para el año 1989 (2).
Debido a las nuevas definiciones adoptadas a nivel mundial sobre el conjunto de parámetros definidos como Ingesta Dietética de Referencia (DRIs por Dietary Reference Intakes) que incluye: Ingesta Dietética Recomendada (RDA), Requerimiento Promedio Estimado (EAR), Ingesta Adecuada (AI), Niveles de Ingesta Máximos Tolerables (UL), no están disponibles en la revisión Venezolana del año 2000, en esta revisión se incluirán RDA, EAR, AI y UL, tanto como la data nacional e internacional lo permitan (3,4).
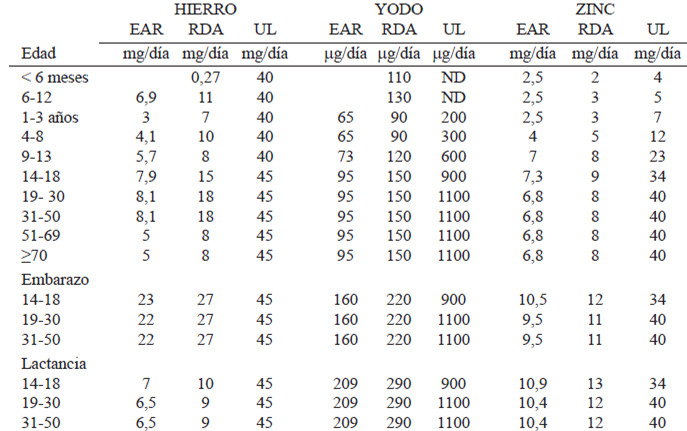
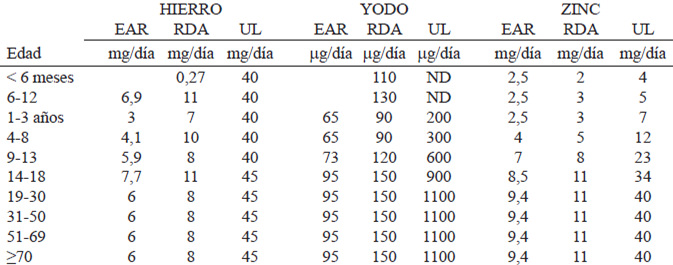
Las nuevas DRIs para Venezuela se encuentran en la Tabla 1 para minerales y en la Tabla 2 para vitaminas. Adicionalmente, se incluyen por primera vez datos sobre polifenoles y la importancia de su consumo.
El hierro es uno de los elementos más abundantes en el planeta y está presente en una importante variedad de alimentos en dos formas que son absorbidas de forma diferente: hierro hémico y no hémico. Las carnes rojas, hígado, pescado contienen hierro hemínico. Los granos, hortalizas, yema de huevo contienen hierro no hemínico.
El hierro en los alimentos de origen animal normalmente está como hierro hemínico, protegido por el anillo porfirínico y por lo tanto no es susceptible a sustancias que faciliten o inhiban su absorción. El hierro de los vegetales no está protegido y su absorción es susceptible a ser afectada.
Entre las sustancias que favorecen la absorción de hierro se encuentran las proteínas de origen animal (carnes), el ácido ascórbico (frutas cítricas), la vitamina A (hígado, yema de huevo, pescado, leche entera, mantequilla, queso) y el β-caroteno (zanahorias, espinaca, brócoli, auyama, melocotones, melón). Entre las inhibitorias se encuentran principalmente los polifenoles presentes en café y té, los fitatos presentes en los cereales, el ácido oxálico presente en espinacas y las altas concentraciones de otros cationes divalentes como el calcio y el zinc, que compiten por el transportador a nivel intestinal.
Debido a la gran variedad de factores que inciden en la biodisponibilidad de hierro, las dietas se clasifican como de alta, media y baja biodisponibilidad. Dietas de pobre o baja biodisponibilidad de hierro con una absorción promedio de 1 a 9 %, son dietas monótonas basadas en cereales, con pocas cantidades de carne pollo o pescado y bajas en vitamina C. Alto contenido de alimentos inhibitorios de la absorción de hierro como maíz, caraotas, harinas integrales, café o té. Las dietas de biodisponibilidad intermedia tienen absorciones entre 10 y 15% y consisten en cereales y tubérculos, con algunos alimentos de origen animal (carne pollo o pescado) y ácido ascórbico. La dieta de alta biodisponibilidad, cuya absorción es mayor al 15% de la dosis, contiene cantidades importantes de carne, pollo o pescado, consumidos diariamente y ácido ascórbico (5).
Es importante resaltar que el principal factor que define el grado de absorción de hierro de una dieta es el estatus y reservas de hierro del individuo y el segundo lugar la biodisponibilidad de la dieta. En Venezuela la dieta promedio es considerada de biodisponibilidad intermedia de hierro.
Dado que el hierro es considerado uno de los micronutrientes con mayor deficiencia reportada, y que no se ha demostrado fehacientemente consecuencias desfavorables por su consumo a menos que exista alguna patología asociada, se considera que el riesgo de los efectos adversos de la ingesta de los alimentos con altos contenido de hierro, incluidos los alimentos enriquecidos en algunos países, es considerado bajo.
Por otro lado se destaca, que para algunos nutrientes como el hierro, no ha sido posible establecer un Nivel de No Observación de Efectos Adversos (No Observed Adverse Effects Leve, NOAEL) ni tampoco un Nivel Inferior de Observación de Efectos Adversos (Lowest Observed Adverse Effects Level, LOAEL) esto por insuficiencia de datos experimentales o de observación.
Las hojas de balance de alimentos para el año 2007, muestran un promedio de disponibilidad per cápita de 17,7 mg de hierro al día (6). En un estudio realizado por la Fundación Bengoa de las encuestas de seguimiento al consumo durante los años 2003 a 2010 (7,8), el consumo de hierro varió entre 17,5 y 20,7 mg/persona/día en los años estudiados, valores ajustados al requerimiento actual.
Sin embargo, la principal deficiencia de micronutrientes para Venezuela es la de hierro (9). La anemia por deficiencia de hierro ha afectado predominantemente los grupos pobres y las áreas rurales. El aumento de la anemia entre las poblaciones urbanas ocurre principalmente en grupos vulnerables y es debido en parte a los cambios estructurales en la disponibilidad de alimentos y al deterioro de los patrones de consumo dietético observado durante la última década 10,11,12).
El estudio oficial disponible realizado entre 1996-98, muestra cifras de prevalencia de anemia (hemoglobina <11 g/dL) muy superiores a las de la Encuesta Nacional de Nutrición 1981-82 y Proyecto Venezuela 1981-87, cuya magnitud alcanza cifras por encima de 50% en los niños menores de 36 meses de edad y de 40% en las embarazadas (13). Este estudio presenta cifras que llaman a la reflexión y crean la necesidad de profundizar en los estudios poblacionales de estos micronutrientes.
En 2009 Ortega et al (14), realizan un estudio sobre anemia y depleción de las reservas de hierro en adolescentes de sexo femenino no embarazadas, concluyendo que existe una alta prevalencia de adecuación del hierro por debajo de los requerimientos diarios y que las adolescentes son un grupo con alto riesgo para desarrollar deficiencia de hierro y anemia.
Otro estudio sobre estado nutricional de hierro y parasitosis intestinal en niños de Valencia (15), mostró una prevalencia de deficiencia de hierro de 69,2%, que coincide con un estudio realizado en preescolares del Estado Nueva Esparta, que arrojó una prevalencia de 69,0% (16). En el estado Carabobo, reportaron 24,4% de deficiencia en niños de estrato socioeconómico bajo, de la zona sur de Valencia (17). En la encuesta realizada por Fundacredesa en el interior del país y el área metropolitana de Caracas (13) la prevalencia general fue de 17,7% (18) y en estudios posteriores la prevalencia de deficiencia de hierro fue aún más elevada, siendo para el Estado Vargas durante 2001 de 33,0%; para Caracas en 2003 de 38,9% y en los Estados Cojedes, Guárico y Portuguesa en 2004 de 33,5%.
En el 2005, García-Casal (19) señaló que los problemas de salud pública relacionados con la deficiencia de hierro continúan siendo importantes, los cuales no han podido ser controlados a pesar del programa de fortificación de harinas con hierro. Recomendó tomar otras medidas, además de la adición de hierro, debido a que otras deficiencias nutricionales parecen estar teniendo un papel importante en la aparición de anemia en los grupos estudiados.
Por su parte, en el sitio web del Ministerio de Salud y Desarrollo Social y el Instituto Nacional de Nutrición hay un articulo relacionado con situación de la deficiencia de hierro en Venezuela (20) donde cita estrategias para la prevención y control de la deficiencia de micronutrientes, entre las que se incluyen suplementación con micronutrientes, fortificación de alimentos (desde 1993 se fortifica la harina de maíz con hierro) y diversificación de la dieta, las cuales son efectivas a corto, mediano y largo plazo respectivamente (21).
Los estudios realizados por Fundacredesa y el Instituto Venezolano de Investigaciones Científicas (IVIC) los años 2001-2002, en 14 ciudades, indican que en los estratos IV y V (Graffar-Méndez Castellano), 48 % de los niños entre 6 meses y 2 años tenían anemia y 52 % deficiencia de hierro. En los niños menores de 5 años de los mismos estratos bajos, la anemia fué de 43 % (22-27).
También se han realizado estudios en embarazadas de la Gran Caracas en 2002, en la población de 0 a 15 años de Caracas en 2003 y en esos mismos grupos de edad en los Estados Cojedes, Guárico y Portuguesa (Eje Norte) en 2004 y en todos los casos la prevalencia de anemia y deficiencia de hierro es muy elevada. En el grupo de 1288 embarazadas evaluadas, la prevalencia de anemia y deficiencia de hierro fue 38,2 y 59,2%, respectivamente. En el estudio de Caracas de 1569 niños y adolescentes evaluados la prevalencia fue de 27,4 y 38,9%, respectivamente y en el estudio del Eje Norte de 1365 niños y adolescentes evaluados, la prevalencia de anemia fue de 38,9% y 33,5% de deficiencia de hierro. Especial mención merecen los niños menores de 2 años tanto en el estudio de Caracas con 57% de anemia como la del Eje Norte con 71,4% (19,25-27).
Los factores considerados por la Academia de Medicina de los Estados Unidos en 2001 para establecer los diferentes parámetros que componen la Ingesta Dietética de Referencia de hierro en los diferentes grupos de edad y sexo, fueron los relacionados con pérdidas basales de hierro y los incrementos de hierro por formación de hemoglobina, hierro tisular y de almacenamiento, así como las pérdidas menstruales (28).
Las Ingestas Dietéticas Recomendadas (RDA) de hierro para Venezuela son 11 mg/día para menores de 1 año, 7 - 10 mg/día para niños, 8 - 11 mg/día para adolescentes y adultos hombres y 8 - 18 mg/día para adolescentes y adultos mujeres, aumentado a 27 mg/día para embarazadas. Durante la lactancia se recomiendan 10 mg/día para madres entre 14 y 18 años de edad y 9 mg/día para madres lactantes mayores (Tablas 1 y 2).
En cuanto al Requerimiento Promedio Estimado (EAR) de hierro, 6.9 mg/día para menores de 1 año, 3.0 - 4.1 mg/día para niños, 5,9 - 7,7 mg/día para adolescentes y adultos hombres y 5,0 - 8,1 mg/día para adolescentes y adultos mujeres, aumentado a 23 mg/día para embarazadas entre 14 y 18 años de edad y a 22 mg/día para embarazadas mayores. Durante la lactancia se recomiendan 7 mg/día para madres entre 14 y 18 años de edad y 6,5 mg/día para madres lactantes mayores.
Los Niveles de Ingesta Máximos Tolerables (UL) para hierro son de 40 mg/día para menores de 1 año y niños, y de 45 mg/día para el resto de las edades, género y condición fisiológica (28).
Estudio de biodisponibilidad de nuevos compuestos de hierro con fines de suplementación y fortificación de alimentos. 2) Investigaciones sobre vehículos y compuestos de hierro adecuados para menores de 2 años. 3) Estudios de absorción y regulación del hierro aminoquelado. 4) Implementación de programas de suplementación y/o fortificación de alimentos. 5) Programas de educación nutricional sobre fuentes de hierro y combinación de alimentos para lograr una mejor absorción de hierro.6) Requerimiento de hierro en vegetarianos.
Según la Organización Mundial de la Salud el déficit de yodo sigue siendo la principal causa de retraso mental y parálisis cerebral evitable en el mundo, afectando en mayor o menor medida al desarrollo y bienestar de más de 1.000 millones de personas, la quinta parte de la población mundial. Se estima que cerca de 2.200 millones de personas corren riesgo de sufrir deficiencia de yodo por vivir en zonas donde la prevalencia de bocio es superior al 5 % (29).
El pescado tiene la mayor concentración natural de yodo. Los análisis sobre diversas especies de pescado mostraron que el contenido de yodo varía ampliamente entre abadejo (191 mg/100 g), bacalao (170 mg/100 g), salmón salvaje (36 mg/100 g) y salmón de piscifactoría (30 mg/100 g). En general las especies de peces que contienen menos grasa, tienen el más alto contenido de yodo (30). Las algas marinas, como wakame, nori o mekabu (utilizada en sushi, sopas, ensaladas y en forma de polvo como condimento) ampliamente consumidas en las culturas asiáticas, también contienen altas cantidades de yodo en varias formas químicas, incluyendo yodo en forma molecular y el yodo orgánico unidos a las proteínas (31,32).
A pesar del contenido de yodo en los alimentos crudos, la cantidad presente en los alimentos cocidos va a depender del proceso de preparación. Así, al freír o asar el pescado se pierde hasta 20% del yodo, mientras al hervirlo se pierde hasta 58% (33). Además, no todo el yodo ingerido se absorbe. Los estudios de captación de yodo radiactivo sugieren que el yodo administrado vía oral se absorbe total y rápidamente. Sin embargo, no ocurre así cuando coincide con una malnutrición calórico-proteica. Por otro lado, lo que puede aplicarse al yodo inorgánico ingerido en ayunas, no lo es cuando se trata de yodo orgánico ingerido con alimentos (34).
Excepto en países como Japón, que incluyen en su dieta diaria pescados y algas marinas o los países que han implementado la yodoprofilaxis, en la mayor parte del mundo existen zonas con déficit de yodo por falta de aporte dietético (35). Esto ha hecho que a nivel mundial se implemente la yodación de la sal como vehículo universal para la distribución de yodo a todas las poblaciones. No es necesario aumentar el consumo total de sal para prevenir las carencias de yodo, por lo que la puesta en práctica de un programa universal de yodación de la sal no debe inducir a aumentar el consumo de sal (36).
Sin embargo, al considerar las evidencias científicas que vinculan la ingesta elevada de sal con el aumento de la presión arterial y de las enfermedades cardiovasculares, así como las recomendaciones para reducir el consumo de sal en la población de todo el mundo, surge la necesidad de investigar vehículos alternativos para el suministro de yodo. Por ejemplo añadir yodo en aceites, puede ser una estrategia para grupos en alto riesgo como mujeres en edad de procrear, lactantes y niños pequeños (36).
Existen evidencias que el exceso de yodo puede producir efectos indeseables en sujetos susceptibles, aun cuando el mecanismo de autorregulación tiroidea permite la administración de cantidades relativamente grandes durante largos periodos, sin efectos secundarios (37,38).
Los alimentos tienen sustancias bociógenas que bloquean la captación de yodo por parte de las células tiroideas, tal como los nabos, la mandioca, la soya y las verduras de la familia de las crucíferas (col, coliflor, coles de Bruselas, lombarda). Estas sustancias se inactivan mediante el calor, por eso al cocinarlas pierden su acción nociva (33,38).
El bocio, es la consecuencia más notoria de la deficiencia de yodo desde la época de la colonia, particularmente en la región andina venezolana. En 1946 se efectuó la Primera Encuesta Nacional de Bocio, la cual reportó una mayor prevalencia en los Andes y en 1951, De Venanzi y colaboradores determinaron por primera vez el yodo urinario en la región andina venezolana (39).
Entre 1954 y 1958, el equipo de la Fundación Luis Roche realizó una serie de encuestas sobre el bocio y demostraron en Bailadores, Estado Mérida la existencia de 84,5% de bocio entre 718 adultos y de 81,3% en 641 escolares estudiados. Para esa época se realizaron dos estudios dietéticos completos efectuados en sitios de bocio endémico venezolano: el del Instituto Nacional de Nutrición en la Mesa, que se hizo en 23 familias (116 individuos) y el de la Fundación Luis Roche en Bailadores en 40 familias (253 individuos, 19% de la población), utilizando el método de inventarios (40)
En 1963 el Instituto Nacional de Nutrición (INN), realizó la Encuesta Nacional de Nutrición, mostrando una prevalencia de bocio que osciló entre 9 y 12%, y una baja excreción urinaria de yodo. En 1966, la Encuesta Nacional de Bocio, realizada también por el INN, en 470.207 niños reveló que un 13,4 % presentaba bocio, siendo la zona andina la más afectada con 32,6 % de los escolares con bocio.
En nuestro país, se inició el programa con el Decreto Presidencial Nº 657 del año1966, en el cual el Estado asume la responsabilidad de implementar el control y la vigilancia de la adición de yodo a la sal de consumo humano y animal. En el año 1976, se publica en Gaceta Oficial la obligatoriedad de las empresas salineras de añadir yodato de potasio como aditivo principal en la prevención del bocio endémico (41).
En 1981, el INN realizó otra Encuesta Nacional de Nutrición, resultando los estados andinos con una prevalencia de 33% de bocio. En 1982, el INN inicia el registro sistemático del control de la yodación de la sal en el Sistema de Vigilancia Epidemiológica y Nutricional (SISVEN). En 1990, se establece como meta la eliminación virtual de las deficiencias de yodo para el año 2000. Este mismo año, el INN y la Fundación CAVENDES, organizaron el II Taller sobre Deficiencia de Yodo, en Ureña, Edo. Táchira, donde se promulgó la “Declaración de Ureña”, la cual contempla entre otras iniciativas, el desarrollo de un programa con los componentes de control y vigilancia y de educación a la población; así como la medición periódica de la excreción urinaria de yodo, un indicador muy confiable para medir el aporte de yodo (41).
El INN en 1991, crea el Programa Nacional para la Erradicación de las Deficiencias de Yodo (PRONAEDY), que 1993 cambia al Programa Nacional para el Control y Eliminación de las Deficiencias de Yodo (PRONACEDY). En 1995 se publica en Gaceta Oficial No. 35.656, la Resolución mediante la cual se crea la Comisión Nacional de Yodación y Fluoruración de la Sal Destinada al Consumo Humano y Uso Veterinario (42).
Una encuesta nacional en 1998 para evaluar las yodurias en 137 parroquias, reveló una mediana nacional de 171 mgI/L, resultado satisfactorio considerando que una mediana mayor de 100 mgI/L indica que no existe deficiencia de yodo en el país. La mediana por área urbana y rural fue de 176 y 148 mgI/L. Estos hallazgos confirmaron que la deficiencia de yodo no era un problema de salud pública. Los consumidores en un 99% adquirían sal refinada y molida, además 80 a 100% manifestó tener conocimiento sobre la importancia de la sal yodada y de las consecuencias de esta deficiencia (42).
En 1999 un grupo de expertos de organismos internacionales (ICCIDD, UNICEF, OPS/OMS, Programa de Prevención de Deficiencias de Micronutrientes: PREDEMI-Perú, Centro Nacional de Alimentación y Nutrición: CENAM) realizó la evaluación externa del programa a solicitud del Ministerio de Salud y Desarrollo Social, otorgándosele a Venezuela la certificación como país virtualmente libre de desórdenes por deficiencia de yodo (42).
Sin embargo, tradicionalmente en Venezuela la deficiencia se circunscribe a la región de los Andes, en los estados Mérida, Trujillo y Táchira. Las encuestas en escolares de esos estados entre 1993- 95, reportaron una prevalencia de bocio endémico de 66%, 65% y 60% respectivamente, confirmando que la deficiencia de yodo era un problema de salud pública. Esta situación desencadenó la puesta en marcha de varias iniciativas, como la intervención con aceite yodado por vía oral en comunidades aisladas, mejor supervisión y control de la yodación y fluoración de la sal, que se acompañó de un programa de educación a la comunidad y monitoreo de las deficiencia de yodo (43).
En los estados andinos en el 2001 se encontró un incrementó en la excreción urinaria de yodo en escolares. La mediana de yoduria fue >300 mgI/L en 18 de las 30 parroquias evaluadas en los estados Táchira, Trujillo y Mérida. Una mediana de yoduria > 300mgI/L es considerada como una “ingesta excesiva de yodo” y lo deseable es 100 a 200 mgI/L (43). También en 2001, se evaluaron estados aledaños al pie de monte andino. Las medianas de yoduria fueron las siguientes: Lara 277 mgI/L y 91% de consumo de sal yodada en hogares y en el 2002 Apure 317 mgI/L y 89% de consumo de sal adecuadamente yodada en hogares. En la encuesta de 2001 el contenido de yodo en la sal fue adecuado en los hogares y el cumplimiento varió entre 86 a 94%. Por el contrario, se ha encontrado un incumplimiento constante de la norma nacional de yodación (norma: 40-70 mg/kg de sal), que viene descendiendo de 43,5% a 34% entre 2001y 2002 (43).
Durante los años 2003, 2004 y 2005 se monitoreó la sal en hogares de 30 localidades de los estados Táchira, Mérida y Trujillo, encontrándose 42 y 55% de sal adecuadamente yodada pàra los años 2003 y 2004, una mediana de yoduria siempre mayor de 100 μgI/L y 73% de consumo de sal adecuadamente yodada en todas las localidades (42).
Desde el año 2002, se ha venido reportando un deterioro en la calidad de la sal que se consume en las comunidades de mayor riesgo para los DDY en Venezuela, ya que desde entonces no se logra alcanzar el nivel recomendado de 90% con contenido adecuado de yodo para muestras en hogares (38, 41,42).
En Venezuela, es obligatoria la yodación de la sal, tanto para el consumo humano como para el consumo animal, según Decreto Presidencial número 657 de 1966. La normativa vigente (COVENIN 3163: 1998), establece un nivel de yodación de la sal de 40 a 70 mg/Kg de sal (42).
Hasta el momento no hay información disponible en las Hojas de Balance de Alimentos, en torno a la disponibilidad alimentaria de yodo para nuestra población (6).
Las Ingestas Dietéticas Recomendadas (RDA) para Venezuela (Tablas 1 y 2) son 110-130 μg/día para recién nacidos, 90 a 120 μg/día para niños, y adolescentes y 150 μg/día para adultos (hombres y mujeres), aumentando a 220 μg/día para el embarazo y 290 μg/día para lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años) (28,1,2).
En cuanto a Requerimiento Promedio Estimado (EAR), 65 μg/día para niños, 73 μg/día para adolescentes y 95 para adultos (hombres y mujeres), aumentando a 160 μg/día para el embarazo y 209 μg/día para lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años).
Los Niveles de Ingesta Máximos Tolerables (UL) para yodo son 200-300 para niños, 600-900 μg/día para adolescentes y 1100 para adultos (hombres y mujeres), incluyendo entre 900 y 1100 μg/día durante el embarazo y la lactancia, en sus diferentes rangos de edad (14-18, 19-30 y 31-50 años) (Norma venezolana COVENIN3163:1998) (44).
1) Evaluación del sistema de vigilancia para el control de los desórdenes por deficiencia de yodo y de la sostenibilidad del mismo. 2) Medición de los niveles de yodo en la leche materna de madres lactantes. 3) Evaluar los niveles de yodación de la sal y el programa en general. 4) Estudio del contenido de yodo de los alimentos de consumo humano y animal. 5) Investigar estrategias sobres otras vías de suministro de yodo, diferentes a la sal.
La cantidad de zinc que ingresa al organismo, depende no solo de la cantidad ingerida sino también de su biodisponibilidad en los alimentos o dietas. Existe una variedad de sustancias que afectan la biodisponibilidad del zinc, algunas actúan como facilitadores de la absorción, tales como las proteínas, los aminoácidos histidina y cisteína, el citrato y el ácido picolínico. Entre los inhibidores se incluyen los fitatos, los oxalatos, ciertos componentes de la fibra dietética, el ion ferroso, el calcio, el cobre y el cadmio.
Las carnes rojas son buenas fuentes de zinc biodisponible, así como los pescados y aves. Aunque los cereales integrales contienen cantidades importantes de zinc, este no está disponible para su absorción a nivel intestinal, debido a la presencia de fitatos y algunos tipos de fibra dietética que se asocian con el zinc y evitan su absorción, perdiéndose en las heces. Altas concentraciones de calcio y hierro en la dieta también van a afectar negativamente la absorción de zinc (45).
La FAO/WHO en 2004 (46) hace una importante subdivisión de la ingesta recomendada según la biodisponibilidad de zinc de la dieta, definiéndola como de baja, media o alta biodisponibilidad. La clasificación de la dieta en alguna de estas categorías se basa en dos criterios: la naturaleza de la dieta en cuanto al contenido de facilitadores e inhibidores de la absorción de zinc y el contenido de zinc de la dieta. La absorción calculada para cada una de estas dietas sería 50, 30 y 15%, para alta, moderada y baja biodisponibilidad, respectivamente. La biodisponibilidad de zinc de una dieta promedio occidental es entre 20 y 30%.
Las dietas de alta biodisponibilidad incluyen cereales refinados, con bajo contenido en fitatos y relaciones molares fitato: Zn <5, adecuado contenido de proteínas, principalmente de origen animal. La de biodisponibilidad intermedia incluye dietas con contenido proteico mixto (animal y vegetal), relaciones molares fitato: Zn 5-15 y consumo moderado de cereales refinados o fortificados con calcio. La dieta del venezolano se clasifica como de biodisponibilidad intermedia, ya que consume carne por lo menos 2-3 veces por semana y el cereal que mas se consume es el maíz como harina de maíz precocida (con un bajo contenido en fitatos). Las de baja biodisponibilidad contienen cantidades importantes de granos de cereales no refinados, no fermentados o no germinados, especialmente si están fortificados con calcio. También incluyen bajas cantidades de proteínas de origen animal y la relación molar fitato: Zn >15.
No se reportan efectos adversos por consumo excesivo de zinc proveniente de alimentos. Las alteraciones reportadas por altos consumos asociados al uso crónico de suplementos de zinc, incluyen principalmente la dificiencia de cobre y con menos frecuencia la supresión de la respuesta inmunitaria y la disminución de lipoproteínas de alta densidad (45,3).
En Venezuela no existen datos de disponibilidad de zinc en las hojas de balance de alimentos y sólo a partir de 1998 se reporta el contenido en Zn en nuestra tabla de composición de alimentos (6). En un estudio realizado por la Fundación Bengoa para Alimentación y Nutrición de las Encuestas de Seguimiento al Consumo durante los años 2003 a 2010 (7) el consumo de zinc se ha mantenido estable durante esos años, fluctuando entre 5,3 y 6,2 mg/persona/día.
Estudios realizados en Venezuela sobre el contenido de zinc en leche humana mostraron que el calostro contiene las mayores concentraciones y que presenta alta biodisponibilidad (47-49).También se ha evaluado el zinc en escolares y adultos mayores (50-52), encontrándose consumos inferiores a las recomendaciones, acompañados de niveles de zinc sérico y en general de estado nutricional muy variado, que incluye desde valores normales hasta francas deficiencias (53,54).
En los últimos 10 años, se han realizado importantes esfuerzos para determinar la prevalencia de deficiencia de zinc en algunos grupos de edades. Estudios en niños muestran prevalencias de déficit que varían desde 19% en el Estado Carabobo (55), 20% en Lara (56), 45% en escolares del Estado Mérida (57) y alcanza una prevalencia de 93% en escolares de la etnia Barí (54).
Un hallazgo recurrente en la literatura, es que las embarazadas muestran disminución significativa de los niveles de zinc sérico a medida que progresa el embarazo, aunque este hallazgo no necesariamente significa que estén o se hagan deficientes de zinc si están bien nutridas (58,59). El problema es que las probabilidades de hacerse deficientes durante el embarazo aumentan a medida que se eleva la prevalencia de deficiencia de Zn de las mujeres en edad fértil. En nuestro país, se ha reportado 42% de deficiencia de zinc en mujeres en edad reproductiva de 15 a 45 años (60).
El principal indicador seleccionado por la Academia de Medicina de los Estados Unidos en 2001 para establecer el Requerimiento Promedio Estimado (EAR), fue la absorción de zinc (más específicamente, la mínima cantidad de zinc absorbido necesaria para igualar la excreción total diaria de zinc exógeno) (3).
Las Ingestas Dietéticas Recomendadas (RDA) (Tablas 1 y 2) para Venezuela son de 2 - 3 mg/día para menores de 1 año, 3 - 5 mg/día para niños, 8 - 11 mg/día para adolescentes y adultos hombres y 8 - 9 mg/día para adolescentes y adultos mujeres, aumentado a 12 mg/día para embarazadas entre 14 y 18 años de edad y a 11 mg/día para embarazadas mayores. Durante la lactancia se recomiendan 13 mg/día para madres entre 14 y 18 años de edad y 12 mg/día para madres lactantes mayores (1, 2,28).
En cuanto al Requerimiento Promedio Estimado (EAR), 2,5 mg/día para menores de 1 año, 2,5 - 4 mg/día para niños, 7 – 9,4 mg/día para adolescentes y adultos hombres y 6,8 – 7,3 mg/día para adolescentes y adultos mujeres, aumentado a 10,5 mg/día para embarazadas entre 14 y 18 años de edad y a 9,5 mg/día para embarazadas adultas. Durante la lactancia se recomiendan 10,9 mg/día para madres entre 14 y 18 años de edad y 10,4 mg/día para madres lactantes adultas.
Los Niveles de Ingesta Máximos Tolerables (UL) para Zn son de 4-5 mg/día para menores de 1 año, 7-12 mg/día para niños, 23 - 34 mg/día para adolescentes y 40 mg/día para adultos (hombres y mujeres), incluyendo embarazo y lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años).
El requerimiento de zinc podría ser 50% mayor en vegetarianos, especialmente los estrictos, cuyas dietas están basadas en el consumo de cereales y legumbres con relaciones molares fitato: Zn mayores de 15:1. De igual manera, el consumo crónico de alcohol se asocia a disminución en la absorción, aumento en la excreción y por lo tanto tendencia a deficiencia de Zn, por lo que el requerimiento estaría aumentado en individuos alcohólicos (3).
El contenido de selenio en los alimentos es muy variado y depende principalmente de la cantidad del mismo que exista en el suelo y que pueda ser absorbido por las plantas (61,62). En general se consideran buenas fuentes de selenio el pan, los cereales, la carne y las aves. Los vegetales no se consideran buenas fuentes a excepción de las nueces del Brasil y vegetales como el ajo, porque pueden almacenarlo siempre que crezcan en suelos ricos en selenio. Recientemente se reportan cambios en los suelos que afectan la biodisponibilidad de selenio, debido a lluvias ácidas y al uso de fertilizantes.
En Venezuela, los trabajos sobre contenido de selenio en suelos se realizaron entre los años 1960 y 1970. Se estudiaron 268 muestras de vegetales provenientes de diferentes zonas del país y las muestras con mayor contenido de selenio (>10 ppm), provenían de los Estados Portuguesa, Barinas, Cojedes y Lara, la mayoría de ajonjolí. Se encontraron lotes de estas semillas con 42 ppm de selenio, mientras el contenido en lotes de zonas no seleníferas fue de 2 ppm (63-66).
Consumos elevados de selenio (>900 μg/día) a través de agua, alimentos o suplementos dietéticos, se han reportado que producen alteraciones en el crecimiento de las uñas y caída del cabello. Se ha asociado también a síntomas gastrointestinales, caída de los dientes y hepatotoxicidad, pero la causalidad directa no ha sido demostrada aun (67).
Recientemente han surgido dudas acerca de los métodos utilizados para la cuantificación de selenio de los alimentos debido a limitaciones en los procesos de extracción, por lo que se concluye que no existen en la actualidad métodos confiables que extraigan el 100% del contenido de selenio de los alimentos, sin potencialmente alterar las formas químicas (61,68).
En nuestro país, son pocos los estudios realizados con este oligoelemento y en su mayoría están orientados a determinar el consumo o ingesta del mineral y su valor en sangre (69,70).
Estos estudios reportan un consumo de selenio más alto que las recomendaciones. Por lo tanto, no parece necesario que la población general consuma complementos de selenio. Solo se justifica en pacientes con alimentación artificial enteral y parenteral prolongada con sueros sin selenio o en niños menores de un año alimentados con fórmulas para infantes carentes de selenio. Sin embargo se pueden presentar casos de deficiencia por posibles efectos tóxicos que se han logrado producir en ensayos con ratas (71-73). En ratas que recibieron dietas con 10 ppm y 4,5 ppm de selenio, se detectaron entre otras, lesiones hepáticas, valores bajos de hemoglobina, hematocrito y fibrinógeno
Hasta el momento no hay información disponible en las Hojas de Balance de Alimentos, en torno a la disponibilidad alimentaria del selenio para nuestra población (6).
Mientras no existan otras investigaciones, la evidencia existente indica que en Venezuela el selenio no es un nutriente problema, por lo tanto no es necesario cambiar las dosis actuales de ingesta recomendada, sino ajustarlas a los parámetros más recientes, que se basan en evidencia científica
Según el IOM, el cálculo de EAR para selenio en adultos fue establecido en 45 μg (0,57 μmol) y se basó en 2 estudios de intervención (China y Nueva Zelanda) y en el criterio de que esa cantidad de selenio maximiza la actividad de la glutatión peroxidasa. Para niños durante el primer año de vida, el cálculo de requerimientos se basó en que la leche humana se reconoce como el mejor alimento por lo menos durante los 6 primeros meses de vida, por lo que las necesidades de selenio en esas edades se basa en la ingesta adecuada (AI) de selenio en leche humana (28).
Las Ingestas Dietéticas Recomendadas (RDA) para Venezuela (Tablas 3 y 4) son 15 y 20 μg/día para recién nacidos, 20 a 30 μg/día para niños, 40 μg/día para adolescentes y 55 μg/día para adultos (hombres y mujeres), aumentando a 60 μg/día para el embarazo y 70 μg/día para lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años) (1, 3,4).
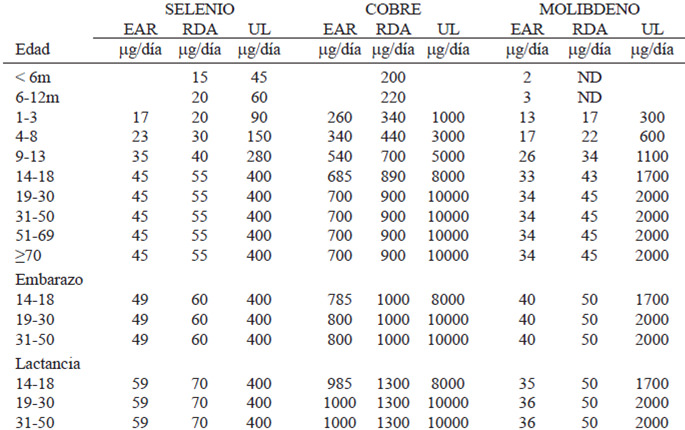
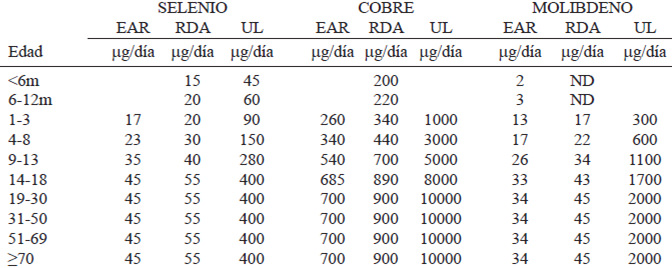
En cuanto a Requerimiento Promedio Estimado (EAR), 17 a 23 μg/día para niños, 35 μg/día para adolescentes y 45 para adultos (hombres y mujeres), aumentando a 49 μg/día para el embarazo y 59 μg/día para lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años).
Los Niveles de Ingesta Máximos Tolerables (UL) para selenio son 45 a 60 μg/día para recién nacidos, 90-150 μg/día para niños, 280 μg/día para adolescentes y 400 para adultos (hombres y mujeres), incluyendo embarazo y lactancia, en cualquiera de sus rangos de edad (14-18, 19-30 y 31-50 años).
1) Contenido de selenio en suelos. 2) Papel de dosis elevadas de selenio en el tratamiento de cáncer. 3) Deben hacerse esfuerzos para mejorar las técnicas existentes, así como estandizar nuevas técnicas de cuantificación de selenio en alimentos. También deben hallarse biomarcadores más sensibles para medir el estatus de selenio. 4) Debido a toda la nueva información que ha surgido acerca de las diferentes formas de selenio y su biodisponibilidad real, así como de lo limitado de las técnicas para su determinación, deben revisarse las recomendaciones dietéticas para selenio.
El cobre se distribuye ampliamente en los alimentos orgánicos, como las carnes, alimentos del mar, nueces y semillas así como en el trigo y los granos completos.
El contenido de cobre en la leche de vaca, es de 0,07 mg % y se ha reportado que la leche humana es más rica en cobre que la de otros mamíferos. Además se sabe que los tratamientos térmicos como pasteurización y UHT, no disminuyen la disponibilidad de hierro, cobre o zinc en leches (74).
Los alimentos más ricos en cobre contienen desde 0,3 – 2 mg/100 g, entre los cuales se encuentran mariscos, nueces, semillas, cacao, legumbres, hígado, vísceras, frutas secas, pasas, tomates, cambur, uvas y papas. Las carnes suelen tener un contenido intermedio de cobre: desde 0,1 – 3 mg/100 g (75).
Entre los nutrientes que afectan la biodisponibilidad del cobre se incluyen el hierro, el zinc y el ácido ascórbico. A su vez, niveles altos o bajos de cobre pueden afectar el metabolismo de tales nutrientes.
Se ha reportado que los valores bajos de zinc suelen acompañarse de un incremento en los niveles de cobre, especialmente en pacientes con enfermedades cardiovasculares, respiratorias y cáncer, reportándose con frecuencia el incremento en la relación cobre/zinc en estas enfermedades. Los adultos mayores tienen mayor riesgo de presentar niveles bajos de zinc, mas no de cobre (76). Por otra parte las ingestas excesivas de zinc por periodos prolongados disminuyen los niveles de cobre en humanos y animales (75).
Por otra parte el cobre y el hierro pueden interactuar de muchas formas y en estados de deficiencia de cobre se altera el metabolismo del hierro. La anemia suele acompañarse de acumulación de cobre a nivel hepático, mientras que un exceso de hierro puede ocasionar disminución de los niveles de cobre (75).
La toxicidad por cobre es rara porque el organismo regula la excreción por vía biliar, por lo que la toxicidad puede ocurrir por obstrucción del ducto biliar con acúmulo hepático de cobre. Los síntomas de la toxicidad incluyen náuseas, vómitos, hemorragias gastrointestinales, diarrea, dolor abdominal y anemia hemolítica. La ingestión excesiva y crónica de cobre puede llevar a cirrosis hepática, conocida como enfermedad de Wilson (75).
En Venezuela son pocos los estudios en relación al cobre, entre estos, se describen los siguientes: En población una infantil de la etnia Bari en el Edo Zulia, los niveles plasmáticos de minerales en μg/ml de Fe: 0,44 ± 0,10; Zn: 0,32±0,04; Cu: 0,76±0,06, y no hubo diferencias por género. El 88,1%, 92,9% y 69,1% de los niños presentaron valores bajos de Fe (<0,50 μg/ml)), Zn (<0,70 μg/ml), y Cu (<0,90 μg/ml), respectivamente. La ingesta diaria de minerales fue muy deficiente, con adecuaciones de 59,77% Fe, 7,37% Zn y 14,67% Cobre. En la muestra estudiada se encontró deficiencia de hierro, cobre y zinc y alta prevalencia de desnutrición (77).
El estudio de las concentraciones séricas de zinc y cobre en una población rural del Estado Lara, en una muestra de 292 menores de 15 años, reveló una prevalencia de deficiencia de 24,32 y 4,45 %, respectivamente (78).
En pacientes con cáncer de mama de Maracaibo Edo Zulia se reportaron niveles séricos elevados de cobre en comparación con un grupo sano y con enfermedad benigna (79). El grupo con cáncer incluyó pacientes con enfermedad metastásica y se hizo evidente que la elevación del cobre se relacionaba con la malignidad de la enfermedad, haciendo entonces el planteamiento de que el incremento de cobre sea una respuesta fisiopatológica del organismo para incrementar enzimas implicadas en la antioxidación o para inducir apoptosis en la célula tumoral. Por otra parte, se planteó que dicha elevación sea un mecanismo tumoral para la estimulación de la angiogénesis, lo que permitiría el crecimiento y sembrar las metástasis por vía hematógena.
En otro estudio en un ambulatorio del Estado Mérida, se encontró que la administración de cobre (5 mg/día) a pacientes hipertensos redujo significativamente los valores de las presiones sistólica y diastólica (80). Este hallazgo indica una alteración funcional en la regulación de la presión arterial durante la carencia moderada de cobre y sugiere que el cobre podría ser una herramienta en el tratamiento de la hipertensión arterial moderada estable.
En las Hojas de Balance de Alimentos no hay información disponible en torno a la disponibilidad alimentaria del cobre para nuestra población (6). En un análisis realizado por la Fundación Bengoa para Alimentación y Nutrición de la Encuesta de Seguimiento al Consumo durante los años 2003 a 2010 (7) el consumo de cobre se ha mantenido estable, fluctuando entre 1,2 y 1,3 mg/persona/día.
Mientras no existan otras investigaciones, la evidencia actual indica que en Venezuela el cobre no representa un problema epidemiológico por exceso o defecto, sin embargo es importante y necesario realizar investigaciones que validen el consumo y biodisponibilidad de dicho nutriente en nuestro país.
Puesto que los datos nacionales son insuficientes, se tomarán como referencia las RDA (Recommended Dietary Allowances) de Estados Unidos para el año 2001, recomiendan una ingesta adecuada de Cobre, en aumento gradual con la edad, entre los 200 μg/día y los 900 μg / día para mayores de 70 años, tanto hombres como mujeres. En la gestante los valores llegan a cifras de 1000 μg/día, mientras que durante la lactancia es 1300 μg/día (28) (Tablas 3 y 4).
1) Estudios longitudinales sobre el papel del cobre en la patogénesis del cáncer. 2) Papel del cobre en la patogénesis y tratamiento de la hipertensión arterial. 3) Definir marcadores de referencia para establecer el estado de cobre en el organismo. 4) Datos nacionales de disponibilidad y consumo de cobre.
El molibdeno es un oligoelemento esencial para casi todas las formas de vida. Funciona como un cofactor para una serie de enzimas que catalizan las transformaciones químicas importantes en los ciclos globales del carbono, nitrógeno y azufre, por lo tanto no solo es necesario para algunas enzimas en la salud humana, sino también para la salud de nuestro ecosistema (81).
Las leguminosas como frijoles, lentejas y arvejas, son las fuentes más ricas en molibdeno. Los productos de granos y frutos secos son considerados buenas fuentes, mientras que los productos animales, frutas y muchos vegetales son generalmente bajos en molibdeno (28). El contenido de molibdeno de los alimentos puede variar considerablemente, debido a que depende del contenido en el suelo y a otras condiciones ambientales (82).
El molibdeno en los suplementos dietéticos, se presenta generalmente en forma de molibdato de sodio o de molibdato de amonio (83).
La toxicidad de compuestos de molibdeno parece ser relativamente baja en los seres humanos. Se ha reportado el aumento de los niveles séricos de ácido úrico y ceruloplasmina en trabajadores expuestos en una planta de tostado de molibdenita (84). Síntomas similares a la gota también se han reportado en una población Armenia, que consumen de 10 a 15 mg de molibdeno en su comida diaria (85). En otros estudios, los niveles de acido úrico en sangre y orina, no se elevan con una ingesta de molibdeno de hasta 1,5 mg / día (28).
Se ha reportado en la literatura un solo informe de toxicidad aguda relacionada con molibdeno a partir de un suplemento dietético. Un hombre adulto el cual presuntamente consumió un total de 13,5 mg de molibdeno durante un período de 18 días (de 300-800 μg/día), desarrollando psicosis aguda con alucinaciones, convulsiones y otros síntomas neurológicos (83). Sin embargo, en un estudio controlado en cuatro hombres jóvenes y sanos, se encontró que la ingesta de molibdeno desde 22 hasta 1.490 μg/día, no produjo ningún efecto adverso durante 24 días (86,87).
El Instituto de Medicina de Estados Unidos, encontró poca evidencia de que el exceso de molibdeno, estuviese asociado con resultados adversos para la salud en personas sanas (28).
Las deficiencias de molibdeno son raras, pero no se sabe a ciencia cierta los efectos sobre la salud puedan causar su deficiencia probada. En Venezuela no existen hasta el momento estudios sobre la posible deficiencia de molibdeno en la dieta diaria del venezolano. En un estudio sobre el “efecto de altos niveles de hierro y molibdeno sobre la nutrición del cobre en vacas mestizas”, los autores concluyen que los altos niveles de molibdeno y/o hierro provocaron una disminución de la concentración de Cu en el tejido hepático, por debajo de los niveles críticos, sin afectar la concentración sérica de Cu. Los altos niveles de Fe ingeridos en un suplemento mineral administrado como sulfato ferroso de alta disponibilidad, provocaron aumentos del Fe a nivel sérico (88).
En algunas regiones del país, el consumo de leguminosas (frijoles, caraotas y quinchonchos) es casi diario, principalmente en las poblaciones rurales (22), por lo que muy probable que en estas poblaciones no exista déficit de moblideno.
En la última revisión de las recomendaciones dietéticas para la población venezolana del 2000 (1) no hay recomendación alguna sobre molibdeno, así como no hay datos en las Hojas de Balance de Alimentos (6).
Las recomendaciones para Venezuela, mientras no existan datos propios, se sustentan en las nuevas definiciones adoptadas a nivel mundial sobre el conjunto de parámetros definidos como Ingesta Dietética de Referencia (FNB/IOM 2001) (28).
Las Ingestas Dietéticas Recomendadas (RDA) para Venezuela (Tablas 3 y 4) son de 2-3 μg/Kg/día para recién nacidos, 17-34 μg/día para niños, 43 μg/día para adolescentes y 45 para adultos (hombres y mujeres), aumenta a 50 μg/día en el embarazo y la lactancia, en cualquiera de los grupos de edad (14-18, 19-30 y 31-50 años).
En cuanto al Requerimiento Promedio Estimado (EAR), 13-26 μg/día para niños, 33 μg/día para adolescentes y 34 para adultos (hombres y mujeres) y aumenta a 40 μg/día para el embarazo y a 35 μg/día durante le lactancia en madres de 14-18 años, y a 36 μg/día a partir de los 19 años.
Los Niveles de Ingesta Máximos Tolerables (UL) para molibdeno son 300-1100 μg/día para niños, 1700 μg/día para adolescentes y 2000 μg/día para adultos (hombres y mujeres), incluyendo embarazo y lactancia, de acuerdo a la edad de la madre.
1) Estudiar el contenido de molibdeno en suelos y alimentos. 2) Analizar el comportamiento de las dosis elevadas de molibdeno en el tratamiento del cáncer de esófago y de estómago. 3) Mejoramiento de las técnicas existentes y estandarización de nuevas técnicas de cuantificación de molibdeno en alimentos venezolanos.
La vitamina C se encuentra en frutas como la grosella, guayaba, cítricos, kiwis y vegetales como el pimentón, brócoli y coles (89). Su contenido varía en los alimentos y puede verse afectado por la estacionalidad, el transporte, la vida útil del alimento, el tiempo de almacenamiento, los métodos de cocción y la cloración del agua. Adicionalmente los cortes, magulladuras, el calentamiento y la exposición al cobre, hierro o condiciones ligeramente alcalinas pueden destruir el ascorbato. También se puede diluir o aclarar en el agua durante la cocción.
En general, la evidencia sugiere que esta vitamina no se asocia con efectos adversos significativos ni tóxicos específicos (89,90).
Los efectos adversos más comunes son los gastrointestinales, asociados con la dosis aguda de vitamina C. También se ha sugerido que el consumo de la vitamina C puede aumentar la excreción de oxalato, aunque los estudios en humanos no han revelado un aumento sustancial de cálculos de oxalato urinario con una ingesta elevada de vitamina C. La vitamina C también favorece la absorción del hierro no hem y esto puede incrementar el daño tisular inducido por el hierro en individuos con hemocromatosis, aunque la posibilidad de esos efectos adversos en ese grupo no ha sido sistemáticamente examinada (89).
En Venezuela se han realizado algunos estudios relacionados con vitamina C, por ejemplo se estudió el patrón de consumo en 438 niños de 4-14 años de una comunidad urbana pobre al norte de Valencia, encontrándose un consumo adecuado de varios nutrientes, incluyendo la vitamina C (91). Este mismo grupo había reportado un consumo adecuado de energía y nutrientes en niños viviendo en pobreza extrema en otra comunidad del mismo Estado (92). Asimismo, el estudio de indicadores del estado nutricional de las vitaminas B1, B2, B6, y C en una población de estudiantes universitarios de Caracas, mostró que no había alteraciones en los nutrientes estudiados (93).
Se ha determinado el contenido de vitamina C en mieles de abeja de la región andina venezolana. Los valores encontrados fueron bajos, oscilando entre 12,74 y 40,13 mg vitamina C/100 g miel, con una media de 20,9 ± 2,9 (94).
Otro tipo de estudio realizado en 14 pacientes, 12 mujeres y 2 hombres diabéticos tipo 2, en tratamiento por 8 y 16 días con vitaminas E 200 mg/ día y C 2 gr/ día, mostró una reducción estadísticamente significativa de los valores de hemoglobina glicosilada, mientras que la glucosa plasmática en ayunas y postprandial así como la insulina, permanecieron sin cambios durante el estudio (95).
Las Hojas de Balance de Alimentos para el año 2007, muestran un promedio de disponibilidad per cápita de 85 mg de vitamina C al día (6). En un estudio realizado por la Fundación Bengoa para Alimentación y Nutrición se analizó la Encuesta de Seguimiento al Consumo de Alimentos (ESCA) durante los años 2003 a 2010 (INE 2011) (3) 7, se encontró que el consumo de vitamina C fluctuó entre 105,9 y 112,7 mg/persona/día.
Las Ingestas Dietéticas Recomendadas (RDA) para Venezuela (Tablas 5 y 6) son 40-50 mg/día para recién nacidos, 15-45 mg/día para niños, 75 mg/día para adolescentes masculinos, 65 mg/día para adolescentes femeninas, 90 mg/día para hombres adultos y 75 mg/día para mujeres adultas, aumentado a 80 mg/día para embarazadas de 14-18 años de edad y a 85 mg/día para el embarazo en mayores de 18 años. Durante la lactancia el requerimiento de vitamina C es de 115 mg/día para madres de 14 a18 años de edad y de 120 mg/día para madres de 19 a 50 años de edad (1, 4,96).
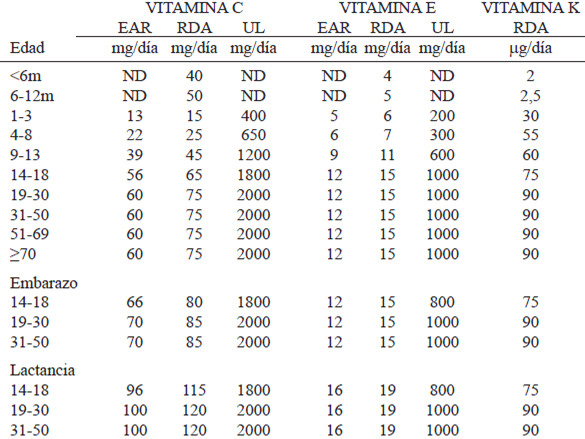
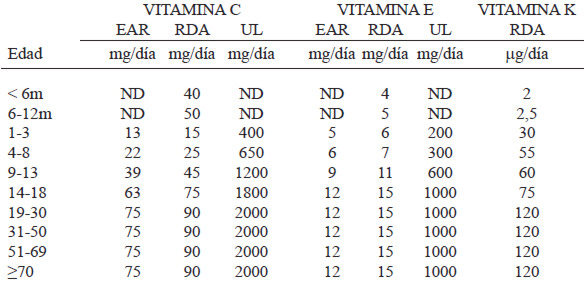
En cuanto a Requerimiento Promedio Estimado (EAR) para vitamina C, 13-39 mg/día para niños, 63 mg/día para adolescentes masculinos, 56 mg/día para adolescentes femeninas, 75 mg/día para hombres adultos y 60 mg/día para mujeres adultas, aumentado a 66 mg/día para embarazadas de 14-18 años de edad y a 70 mg/día para el embarazo en mayores de 18 años. Durante la lactancia el requerimiento de vitamina C es de 96 mg/día para madres de 14 a 18 años de edad y de 100 mg/día para madres de 19 a 50 años de edad.
Los Niveles de Ingesta Máximos Tolerables (UL) para vitamina C son 400-1200 mg/día para niños, 1800 mg/día para adolescentes y 2000 mg/día para adultos. El UL durante el embarazo y la lactancia es de 1800 mg/día para las madres de 14 a 18 años de edad y de 2000 mg/día para mayores de 18 años.
1) Estudios de consumo y de contenido de vitamina C en los diferentes climas y grados de maduración de los vegetales. 2) Consumo de vegetales y las frutas en la población venezolana, por regiones y estratos sociales. 3) Evaluar los efectos de la Vitamina C en enfermedades crónicas tipo diabetes, por el comportamiento de la hemoglobina glicosilada. 4) Investigaciones en pacientes en cuidados intensivos y el uso de dosis supra fisiológicas puntuales para disminuir la estancia hospitalaria y el tiempo conectado a ventilación mecánica.
La principal fuente de Vitamina E o tocoferoles se encuentra en los aceites vegetales como los de girasol, soya, ajonjolí, maíz y palma y sus productos derivados, como mayonesa y margarina. El germen de trigo y los frutos secos como nueces, almendras y avellanas poseen altas concentraciones de tocoferoles y también los productos elaborados de pastelerías que contienen margarinas y aceites vegetales. El calor utilizado en el procesamiento de los alimentos puede disminuir las concentraciones de los tocoferoles (97).
En general, la mayor proporción de vitamina E proviene de la grasa añadida a la dieta con un importante porcentaje proveniente de los postres. Sin embargo, en ciertos grupos poblacionales el consumo de suplementos pudiera representar una fuente importante de esta vitamina (98).
La mayoría de los aceites contienen cantidades variables de tocoferol y pocos aceites contienen tocotrienol, el aceite de girasol y el germen de trigo contienen altas cantidades de α tocoferol, mientras que el aceite de maíz y el de soya contienen mayor proporción de γ tocoferol y algo de tocotrienol. El aceite de palma contiene grandes cantidades de α y γ tocotrienol y algo de α tocoferol. Las nueces especialmente las almendras contienen alto contenido de vitamina E, mientras que las frutas y vegetales tienen poca (99).
La vitamina E parece tener baja toxicidad y el límite de 1.000 mg/día de cualquier forma de tocoferol suplementario se fundamenta en estudios en animales sobre la toxicidad hemorrágica. Algunos estudios indican que dosis hasta de 3.000 mg/día pueden considerarse inocuos y que por encima de esto pudiera tener efectos adversos que no son graves (problemas gastrointestinales, creatinuria y alteración de la coagulación sanguínea) y desaparecen rápidamente al suspender la vitamina E o reducir su dosis (97,99).
La vitamina E reduce la adhesión plaquetaria y las altas dosis de suplementos pueden aumentar los tiempos de coagulación por lo tanto es importante considerar esto cuando se tratan a pacientes que toman anticoagulantes o presentan deficiencias de vitamina K.
En Venezuela en los últimos años ha habido cierto interés en investigar sobre los efectos de la vitamina E en el organismo; algunos de estos estudios han sido revisiones sobre aspectos farmacológicos relacionados con la vitamina E y los antioxidantes (100) y también estudios sobre aspectos básicos y métodos de determinación de la vitamina (101).
Hasta el momento no hay información disponible en las Hojas de Balance de Alimentos, en torno a la disponibilidad alimentaria de vitamina E para nuestra población (6).
En cuanto a la determinación del nivel de vitamina E sérico en diferentes grupos de edad, se realizó un estudio en 223 adultos de Caracas con una edad promedio de 40,28 ± 7,94 años y una concentración sérica de 932 ± 360 μg/dL (rango: 195-1900 μg/dL) (102). Otro estudio en niños pre-escolares sanos con edades entre 2 y 6 años del Edo. Mérida, encontró concentraciones séricas de 587 ±43 μg/dL (103). Desde el año 2000, se incluyen recomendaciones de vitamina E para la población Venezolana, pero basada en los datos de los Estados Unidos de América. Un estudio realizado en adultos mayores de 60 años reportó deficiencia de vitamina E (104) y niveles séricos disminuidos de vitamina E, que también son frecuentes en pacientes con diagnóstico reciente de diabetes tipo 2 (105).
Hay dos estudios nacionales relacionados con fumadores. El primero en adolescentes, determinaron los niveles de vitaminas A, C y E y observaron que la vitamina C fue significativamente menor en los fumadores, pero no hubo diferencias significativas en el α-tocoferol. Sin embargo, el 96,9% y 98,5% tuvieron deficiencias en vitamina A y E respectivamente, no asociadas con el hábito tabáquico (106). El otro estudio realizado tuvo como objetivo evaluar en fumadores el efecto de la administración de vitamina E individual y de vitamina E conjuntamente con vitamina C sobre la afinidad de la LDL por proteoglicanos arteriales. Se concluyó que el suministro de vitaminas C y E mostró un efecto sinergístico, al disminuir en mayor proporción la afinidad de la LDL por los proteoglicanos arteriales en comparación con la administración individual de la vitamina E (107).
Villarroel y colaboradores en 2008 (108) en un estudio con individuos sanos, encontraron que el consumo continuo de vitamina E podría alterar los valores de protrombina y tromboplastina y por ende modificar el proceso de coagulación normal.
Estudios en animales han mostrado que la deficiencia de vitamina E se asocia con diarreas más severas en ratas (109) y que el consumo del aceite de palma parcialmente refinado disminuye el colesterol y mejora la relación colesterol/HDL en las ratas con hiperlipidemia inducida (110).
Todos estos hallazgos indican que debe seguirse investigando sobre la vitamina E y sus efectos, pero en el país no hay estudios sobre cambios en las recomendaciones de la ingesta. Como ya se mencionó, las HBA del año 2007 no incluyen información relativa a la disponibilidad alimentaria de la vitamina E para la población venezolana, por lo que es conveniente adaptarlas de los estándares internacionales, donde han realizado mayores estudios al respecto (FNB/IOM 2001) (28).
En relación a la ingesta dietética recomendada (RDA) para Venezuela (Tablas 5 y 6) es 4-5 mg (9,2-11,5 μmol) de α-tocoferol por día para infantes, 6-7 mg (13,9-16,3 μmol) para niños, 11-15 mg (26,6-34,9 μmol) para adolescentes, 15 mg (34,9 μmol) para adultos (hombres y mujeres) y 19 mg (44,2 μmol) durante la lactancia (15-50 años).
En cuanto al Requerimiento Promedio Estimado (EAR) (Tablas 3 y 4), no hay datos para los recién nacidos, 5-6 mg (11,6-14,0 μmol) por día de α-tocoferol para niños, 9-12 mg (20,9-27,9 μmol) para adolescentes y 12 mg (27,9 μmol) para adultos (hombres y mujeres) y embarazadas. Se recomiendan 16 mg (37,2 μmol) por día de α-tocoferol durante la lactancia (15-50 años).
Los Niveles de Ingesta Máximos Tolerables (UL) de la vitamina E para los recién nacidos no es posible establecerlos, 200-300 mg (465-698 μmol) por día de α-tocoferol para niños, 600 mg (1395 μmol) por día de α-tocoferol para niños de 9-13 años y 800 mg (1860 μmol) por día de α-tocoferol para adolescentes y 1.000 mg (2.326 μmol) por día de cualquier forma de suplemento de α-tocoferol para adultos mayores de 19 años, 800 mg (1860 μmol) por día de α-tocoferol para embarazadas y lactancia entre las edades de 14-18 años y 1.000 mg (2326 μmol) por día de α-tocoferol para embarazadas y lactancia de mujeres de mayores de 19 años (28).
1) Estudios sobre el contenido de vitamina E en alimentos, así como de consumo en diferentes grupos poblacionales. 2) Efectos de las otras formas de Vitamina E, diferentes de α –tocoferoles. 3) Grado de toxicidad de la Vitamina E y el uso de suplementos. 4) Papel de la vitamina E en la prevención y tratamiento de enfermedades crónicas no transmisibles.
Se conocen 3 formas de la vitamina: la forma natural, filoquinona (K1), presente en plantas verdes, la bacteriana (K2) producida por la flora intestinal conocida como menaquinona y la forma sintética, menadinona (K3). Todas son solubles en lípidos e insolubles en agua, y su principal función conocida es en el proceso de coagulación sanguínea (111).
Se ha propuesto que pueda tener otras funciones en la prevención de osteoporosis (112-115), enfermedades cardiovasculares (115-117) y más recientemente en el control de procesos inflamatorios. En ninguno de estos roles se ha demostrado un papel claro y la evidencia es aun controversial. Recientemente se ha determinado que los mamíferos pueden convertir la vitamina K natural o filoquinonas en menaquinonas específicamente MK-4, que parecen estar involucradas en la regulación de procesos como inflamación estrés oxidativo y apoptosis (118,119).
La vitamina K se encuentra ampliamente distribuida en los alimentos consumidos en las dietas de la mayoría de la población. La que se consume con mayor frecuencia es la filoquinona que se encuentra principalmente en alimentos vegetales de hojas verdes (ej. espinaca, brócoli, coles de Bruselas) y algunos aceites vegetales (soya, algodón y oliva). También se encuentra en carnes, leche de vaca, huevos, productos de soya y algunas mayonesas.
Las menaquinonas se encuentran en algunos tejidos animales y productos fermentados como los quesos pero su mayor aporte proviene de la flora bacteriana que la sintetiza a nivel intestinal. Esta producción intestinal contribuye a cubrir una fracción importante de las necesidades diarias y su amplia disponibilidad disminuye las posibilidades de deficiencia en la mayor parte de la población.
En humanos, las dosis altas de menadiona pueden causar daño oxidativo, fragilidad de glóbulos rojos y la formación de metahemoglobina. Dosis altas de vitamina K3 en bebés prematuros para tratar hemorragia pulmonar, causó hiperbilirrubinemia y sobrecarga del hígado inmaduro, asi como toxicidad cerebral. Debido a las alteraciones y riesgos de daño hepático con la forma sintética de vitamia K (menadiona o K3), su uso terapéutico fue descontinuado.
En nuestro país, son pocos los estudios sobre esta vitamina y hasta el momento no hay información en las Hojas de Balance de Alimentos, en torno a la disponibilidad alimentaria de vitamina K para nuestra población (6).
Mientras no existan otras investigaciones, la evidencia existente indica que en Venezuela la vitamina K no es un nutriente problema, por lo tanto no es necesario cambiar las dosis actuales de ingesta recomendada, sino ajustarlas a los parámetros más recientes, que se basan en evidencia científica.
Las Ingestas Dietéticas Recomendadas (RDA) para Venezuela (Tablas 5 y 6) serian 2 a 2,5 μg/día para recién nacidos, 30-55 μg/día para niños, 60-75 μg/día para adolescentes, 120 μg/día para hombres y 90 μg/día para mujeres. El requerimiento durante el embarazo y la lactancia depende de la edad de la madre, siendo de 75 μg/día en embarazadas adolescentes y de 90 μg/día cuando la madre es mayor de 18 años (1,2,28). (Tablas 3 y 4).
Para vitamina K no hay ni Requerimiento Promedio Estimado (EAR), ni Niveles de Ingesta Máximos Tolerables (UL). Esto último es debido a que con la limitada información disponible, no se han reportado efectos adversos por consumo elevado de alimentos o suplementos ni en humanos ni en otros animales, por lo que no puede establecerse un UL (28).
1) Contenido de vitamina K en alimentos, así como el consumo en diferentes grupos poblacionales. 2) Estudios de biodisponibilidad de las diferentes formas de vitamina K. 3) Otras investigaciones deben concentrarse en aclarar las funciones de las proteínas Gla extrahepáticas y su posible importancia en enfermedades óseas e isquémicas.
Los carotenoides son tetraterpenoides que se encuentran en vegetales, bacterias no fotosintéticas, levaduras y algunos productos de origen animal como el salmón, la langosta y la yema de huevo (120). En los vegetales son responsables de los pigmentos rojos, naranjas y amarillos que se encuentran en frutas y verduras. Hasta la fecha se han identificado más de 600 carotenoides, aunque solo unos 20 se encuentran en cantidades detectables en el organismo y se les ha adjudicado alguna función biológica. El β-caroteno es el carotenoide más estudiado en términos de metabolismo y potenciales efectos sobre la salud, pero el licopeno, la luteína, la zeaxantina, el α-caroteno y la β- criptoxantina han sido evaluados en años más recientes por su abundancia, actividad antioxidante y su potencial de convertirse en vitamina A (α-caroteno, β-caroteno y β-criptoxantina) (121).
Tanto a nivel intestinal como hepático los carotenoides con actividad provitamina A, pueden escindirse centralmente y producir dos moléculas de retinal. Recientemente se ha detectado la presencia de la enzima responsable de la conversión (β-caroteno monooxigenasa 1) en otros tejidos. Este hallazgo de que la conversión en vitamina A a partir de β-caroteno puede ocurrir fuera del intestino, ha generado gran interés investigativo por las implicaciones de generar vitamina A en otros tejidos (122).
La eficiencia de esta conversión es aún muy investigada y parece depender de varios factores como de la matriz del alimento, el tipo de carotenoide y las reservas de vitamina A del individuo, entre otras. Se ha sugerido que en humanos, la conversión de β-caroteno, (administrado en aceite como suplemento) a vitamina A varía de 2:1 hasta 16:1. Cuando se administra como frutas y verduras, la conversión es de 12:1 en frutas y de 24:1 en verduras. Debido a las grandes variaciones entre individuos, a los cambios en el tiempo después de la absorción y al carotenoide en consideración, resulta difícil establecer un factor de conversión para la población, aunque parece ser mayor del inicialmente establecido de 6:1, para acercarse al propuesto en 2001 de 12:1 (28,122-124).
El Comité de Expertos de la FAO/WHO en 2004, establece como factores de conversión de β-caroteno: vitamina A 6:1 y para otros carotenoides: vitamina A 12:1 (46).
Aunque la ingesta de β-caroteno varía ampliamente y no se distribuye de forma homogénea en la población, se ha calculado para países como los Estados Unidos y el Reino Unido, un consumo promedio de 1 a 2 mg/día, aunque se reportan consumos diarios de hasta 10 mg. Este consumo es importante no solo por los efectos del β-caroteno per se, sino por su conversión en vitamina A, la cual calculando un factor de conversión β-caroteno: vitamina A de 6:1, podría suplir las necesidades de vitamina A en vegetarianos (28).
El β-caroteno se encuentra en vegetales de hojas verdes como la espinaca y el brócoli, en algas, en hortalizas y frutas amarillas como los mangos, naranjas, zanahorias, batata y auyama. El licopeno se encuentra en tomates y sus productos, toronja rosada, duraznos, patilla, guayaba y lechosa. La luteína y zeaxantina se encuentran en vegetales de hojas verdes como la espinaca, mandarinas, yema de huevo, maíz, entre otros. Las principales fuentes de α-caroteno y β-criptoxantina son zanahorias, naranjas y su jugo, tomates y sus preparaciones y espinacas.
El contenido de β-caroteno y otros carotenoides en leche materna es muy variado y depende en gran medida de la dieta de la madre.
La biodisponibilidad de los carotenoides en general aumenta con el cortado, procesamiento, cocción ligera y uso de grasas (122,125).
Especial mención merece el arroz dorado (Golden Rice), un alimento modificado genéticamente, en el cual dos genes han sido insertados en el genoma del arroz que llevan a la síntesis y acumulacion de beta-caroteno en el grano de arroz. Desde que se produjo por primera vez en 1999, se han generado nuevas líneas con mayor contenido de β-caroteno. La meta es ofrecer el 100% del requerimiento en 100-200 g de arroz, que en algunas partes del mundo es el único alimento de consumo diario (126).
No se han reportado efectos adversos por altos consumo de carotenoides (hasta 180 mg/día de β-caroteno para el tratamiento de protoporfiria eritropoyética) más allá de la coloración amarilla de la piel por acumulación de carotenoides conocida como carotenodermia.
En un estudio realizado por la Fundación Bengoa para Salud y Nutrición en base al análisis de las encuestas de seguimiento al consumo durante los años 2003 a 2010 (6), se observa que el consumo de carotenos ha variado considerablemente durante esos años, fluctuando entre 3107,2 y 3844,5 equiv/persona/día.
En el país se han realizado algunos trabajos con carotenoides y se ha incluido su contenido en la revisión del año 2000 de la Tabla de Composición de Alimentos, estableciéndose también prioridades de investigación en esta área (127). Los esfuerzos investigativos también se han centrado en evaluar el contenido de carotenoides en frutas y algas (128-135) su concentración y modificación en aceites durante los procesos de extracción (136,137) y los niveles séricos en pacientes con cáncer (138).
Los trabajos realizados a nivel mundial para establecer las necesidades reales son limitados ya que no se dispone de la evidencia científica necesaria para establecer inequívocamente su función, su medición y las consecuencias de su deficiencia (1, 2, 4, 46, 28, 89,139-142). La única función claramente establecida para algunos carotenoides (α-caroteno, β-caroteno y β- criptoxantina) es su actividad provitamina A, por lo que el establecimiento de requerimientos para carotenoides debe estar en estrecha relación con las Ingestas Dietéticas de Referencia (DRIs) para vitamina A (28).
Aunque Estados Unidos y Canadá no establecen requerimientos para carotenoides en general o para β-caroteno en particular, apoyan las recomendaciones de ingerir abundantes frutas y vegetales. Además, debido a que la evidencia hasta ese momento no indicaba ningún beneficio adicional de los suplementos de β-caroteno en la prevención de enfermedades crónicas y que por el contrario podían causar efectos nocivos en ciertos subgrupos de población, no recomiendan el uso de suplementos de β-caroteno para otro uso que no sea como fuente de provitamina A en poblaciones a riesgo de deficiencia de vitamina A (28).
Debido a la insuficiencia de datos experimentales y la imposibilidad actual de establecer el requerimiento para carotenoides, se decide apoyar la recomendación existente de consumir por lo menos 5 porciones de frutas y vegetales al día, lo cual proveería entre 3 y 6 mg/día de β-caroteno. Aunque tampoco es posible establecer la ingesta máxima recomendada de carotenoides, no se recomienda el uso de suplementos de β-caroteno para la población general, debido a que los estudios realizados hasta el momento no demuestran un beneficio por el uso de suplementos y por el contrario, algunos de ellos muestran posibles efectos dañinos en ciertos grupos de población. La recomendación sobre los suplementos no aplica en caso de que se trate de poblaciones deficientes o a riesgo de deficiencia de vitamina A (28).
1) Funciones de los carotenoides en humanos. 2) Estudios de consumo de β-caroteno y otros carotenoides que permitan definir su requerimiento. 3) Eficiencia de conversión de carotenoides en vitamina A. 4) Papel del β-caroteno como prooxidante y definir si aumenta el riesgo de ciertos tipos de cáncer en determinados grupos de población como los fumadores. 5) Contribución de los carotenoides, especialmente el β-caroteno, para cubrir los requerimientos de vitamina A.
Debido a algunas evidencias científicas, hay un intenso interés sobre el papel de polifenoles como antioxidantes y en la prevención y tratamiento de enfermedades crónicas no transmisibles. Debido a que este grupo de trabajo realizó la revisión de los requerimientos de carotenoides como nutriente, como fuente de vitamina A y como antioxidante, decidimos incluir los polifenoles como parte de la revisión. Si bien no pueden considerarse nutrientes y no se han establecido dosis recomendadas hasta ahora, creemos interesante presentar a los lectores algunos contenidos y dosis que se consumen en varios países, así como ciertas evidencias de riesgos y beneficios de su consumo, asi como aspectos importantes de elucidar.
Históricamente los compuestos fenólicos y polifenoles se han considerado antinutrientes debido a que algunos de ellos, especialmente los taninos, mostraron tener efectos adversos en el metabolismo humano debido a cierta habilidad de enlazar proteínas, carbohidratos y enzimas digestivas, reduciendo así la digestibilidad del alimento; pero recientemente, los estudios han señalado su rol como antioxidantes, por lo que se debe repensar sobre los beneficios a la salud de estos compuestos fenólicos (143), aunque su papel como pro-oxidantes no ha sido totalmente descartado (144).
Los polifenoles están presentes en todos los alimentos de origen vegetal (vegetales, cereales, leguminosas, frutas, nueces) y bebidas (vino, sidra, cerveza, té, cacao). Los niveles varían grandemente entre cultivares de una misma especie. Las mayores concentraciones de estos compuestos se encuentran generalmente en hojas y las partes externas de las plantas ya que su formación depende de la luz (143,145-148).
Entre los compuestos fenólicos con una reconocida actividad antioxidante destacan los flavonoides, los ácidos fenólicos (principalmente ácido hidroxicinámico, hidroxibenzoico, cafeico, clorogénico), taninos, chalconas y coumarinas (145). Sin embargo, debe existir cautela en cuanto a su uso ya que se ha reportado que el uso de flavonoides purificados, administrados en altas dosis como suplementos, podrían afectar el estatus de elementos trazas, folatos y vitamina C (149).
El rango de consumo va desde alrededor de 20 mg/dia (Estados Unidos, Dinamarca, Finlandia) hasta 70 mg/dia (Holanda). Estos valores se consideran mucho menores que los estimados en estudios anteriores, quizás debido a insuficientes datos en la tabla de composición de alimentos de una o más sub-clases de flavonoides (150).
La ingesta promedio de proantocianidinas o taninos condensados (grado de polimerización > 2) en Estados Unidos de América para la población de 2 años es de 53,6 mg/día. En España parece ser mucho mayor, estimándose que la ingesta de proantocianidinas está entre 240 y 450 mg/día (151).
En un estudio realizado en Finlandia el promedio de ingesta de polifenoles fue 863 ± 415 mg/día, determinado por análisis de alimentos, junto con el registro de consumo individual de alimentos. Los ácidos fenólicos fueron el grupo dominante de polifenoles (75% de la ingesta total), seguido de las proantocianidinas (14%) y antocianidinas y otros flavonoides (10%). Por el alto consumo y altas concentraciones de ácidos fenólicos, el café y los cereales fueron los principales contribuyentes a la ingesta de polifenoles. “Berries” y los productos de “berries” fueron las fuentes principales de antocianidinas, elagitaninos y proantocianidinas, siendo las frutas las principales fuentes de flavonoles, flavonas y flavanonas. Los resultados dan un soporte adicional a las recomendaciones para una dieta variada, que incluya frutas, cereales y vegetales (152).
Diversos trabajos han evaluado el contenido de polifenoles y la capacidad antioxidante en vegetales y cervezas, encontrándose que en las semillas de túpiro, mamón, sorgo y chiga están en el rango de 557- 4450 mg-EAG/ 100 g muestra seca (153,154); los pericarpios de mamón y chiga 1400-3640 mg EAG/100 g de muestra (154); las pulpas de ajíes verdes y rojos así como las pulpas de tres variedades de túpiro contienen entre 740 -1392 mg EAG/100 g de muestra seca (153,155); la nuez de cacao contiene 6660 mg EAG/100 g de muestra seca (154). Las cáscaras y/o pieles de las frutas evaluadas estuvieron en el orden de 2620 y 7790 mg EAG/g muestra seca (156-158). Las cervezas, así como los ingredientes utilizados en su fabricación, mostraron valores de polifenoles entre 146 y 260 mg EAG/l para las cervezas y 3,83-319 mg EAG/100 g muestra seca para los ingredientes (159). En todas las muestras estudiadas hubo una alta correlación entre el contenido de polifenoles y la actividad antioxidante.
En la Universidad de los Andes, Estado Mérida, evaluaron la fresa (Fragaria vesca L.) con el propósito de aislar e identificar los polifenoles presentes en esta fruta, encontrándose actividad inhibitoria sobre la enzima α-amilasa del suero sanguíneo valorada por espectrofotometría (160).
En otro estudio se evaluaron los taninos, polifenoles, antocianinas y la capacidad antioxidante de la pulpa del acai (Euterpe oleracea Mart), recolectada en el Amazonas venezolano, provenientes de dos cosechas del año 2005. Los resultados expresados en base seca indicaron que el acai de las dos cosechas contienen polifenoles 5,02 y 2,20 g/100 g; taninos 0,70 y 1,37 g/100g; antocianinas 0,73 y 1,60 g/100g y la capacidad antioxidante fue 88,03 y 87,87%, respectivamente, constituyendo una buena fuente de antioxidantes y que podría ser industrializado para aprovechar al máximo sus propiedades (161).
1) Estudios sobre los polifenoles con actividad antioxidante y los niveles óptimos necesarios para lograr una actividad detectable. 2) Estudios de eficacia de polifenoles naturales y sintéticos como antioxidantes. 3) Polifenoles como antimicrobianos. 4) Efectos del procesamiento sobre los compuestos fenólicos en frutas y vegetales.