La obesidad se relaciona con mayor concentración de ácidos grasos libres (AGL) circulantes. En adultos obesos el perfil de AGL difiere comparado con individuos de peso adecuado, en adolescentes los resultados son contradictorios. El objetivo fue comparar el perfil de AGL de jóvenes obesos con y sin Síndrome Metabólico (SM) y explorar la asociación entre estos AGL con las alteraciones metabólicas propias de la obesidad y el SM. Estudio transversal, con 96 jóvenes entre 10 y 18 años divididos en 3 grupos: 1) obesos con SM, 2) obesos sin SM y 3) peso adecuado (PA), pareados uno a uno por edad, sexo, maduración puberal y estrato socioeconómico. El estado nutricional se clasificó según el índice de masa corporal (IMC) en obesos (IMC>p98) y Peso Adecuado (PA) (IMC p15-p85) según OMS/2007, se evaluó circunferencia de cintura, adiposidad, perfil lipídico, proteína C reactiva ultra sensible (PCRhs), glucemia, insulina y resistencia a la insulina (RI) según homeostatic model assessment (HOMA). La concentración sérica de AGL se determinó mediante cromatografía gaseosa. Ambos grupos de obesos presentaron mayor adiposidad, inflamación, AGL totales y frecuencia de palmitoléico-16:1n7 comparados con PA. Los obesos con SM presentaron más alteraciones metabólicas, mayor cantidad de dihomo-γ-linolénico (DHGL-20:3n6) y relación 20:3n6/18:2n6 indicativa de mayor actividad de Δ6 desaturasa (D6D). Los AGL totales, palmitoléico-16:1n7, DHGL-20:3n6, actividad D6D y PCRhs correlacionaron significativamente con variables de adiposidad, RI y triglicéridos. Los resultados en obesos con SM permiten asociar la obesidad central con inflamación, lipolisis aumentada en el tejido adiposo visceral y alteraciones metabólicas.
Palabras clave: Obesidad, síndrome metabólico, ácidos grasos libres, jóvenes
Obesity produces greater circulation of free fatty acids (FFA). In adults, the FFA composition changes in states of obesity; in adolescents, the results are contradictory. This study compare the FFA profile of obese youth with and without Metabolic Syndrome (MetS) and explore the association between FFA and metabolic alterations of obesity and MetS. A cross–sectional study with 96 young people between 10 and 18 years old was divided into three groups: 1) obese youth with MetS, 2) obese youth without MetS; and 3) adequate weight (AW), matched according to age, gender, pubertal maturation and socioeconomic stratum. The nutritional status was classified according to the body–mass index (BMI), according to the World Health Organization 2007 (WHO, 2007); the waist circumference (WC), adiposity, lipid profile, highly–sensitive reactive C protein (hsRCP), glucose, insulin and insulin resistance (IR), according to the homeostatic model assessment (HOMA Calculator Version 2.2.2). The FFA serum concentration was determined by gas chromatography. Both obese groups had higher adiposity, inflamation (hsRCP), FFA totals and frequency palmitoleic–16:In7, compared to AW. The obese with MetS presented more metabolic alterations, a greater amount of dihomo–γ–linolenic (DHGL-20:3n6) and a 20:3n6/18:2n6 relation, indicative of increased activity of Δ6 desaturase (D6D). The FFA totals, palmitoleic–16:1n7, DHGL–20:3n6, D6D activity and hsRCP significantly correlated with variables of adiposity, IR and triglicerides. The results in obese with MetS corroborate the association among central obesity, inflammation and increased lipolysis in visceral adipose tissue and metabolic alterations.
Key words: Obesity, metabolic syndrome, free fatty acid, young
https://doi.org/10.37527/2014.64.4.004
Grupo Investigación Alimentación y Nutrición Humana. Universidad de Antioquia. Medellín, Colombia
El exceso de peso actualmente constituye una pandemia que afecta 34,3% de la población adulta y se presenta en la mayoría de países, estratos y edades (1); la obesidad y el grado de adiposidad está asociada con enfermedades metabólicas graves como diabetes (DM), dislipidemia, hipertensión arterial (HTA), síndrome metabólico (SM) y en consecuencia mortalidad prematura, cada vez más frecuentes en países no industrializados y con diferentes estadios de transición epidemiológica (2,3). En 2008, 170 millones de menores de 18 años padecían exceso de peso (1). Se estima que en América Latina se encuentren entre 16,5 y 22,1 millones de adolescentes obesos, con prevalencias de exceso de peso desde 16,7% en Colombia, 20% en Brasil, hasta 35% en México y Chile (4).
La obesidad, principalmente abdominal induce alteraciones del metabolismo como intolerancia a la glucosa y resistencia a la insulina (RI), disminución en la concentración de las lipoproteínas de alta densidad (cHDL), elevación de los triglicéridos (TG) y aumento de la presión arterial, las cuales en conjunto configuran el SM (5).
La conexión entre obesidad central y las alteraciones propias del SM podrían ser los ácidos grasos libres (AGL), producidos por la disfunción del tejido adiposo tras un crecimiento hipertrófico e hiperplásico generado por el sometimiento crónico a un balance positivo de energía, este crecimiento desordenado produce infiltración y activación de macrófagos, sustancias proinflamatorias, aumento en el número de receptores β3 adrenérgicos que tienen una menor sensibilidad a la señal antilipolítica de la insulina en los adipocitos viscerales (6), lo que se traduce en liberación de grandes cantidades de AGL y lipotoxicidad; estos AGL en órganos como el hígado afectan la síntesis de lipoproteínas y podrían generar hígado graso, en el páncreas afectan la producción de insulina y en tejidos periféricos como el músculo producen RI por activación de vías como protein kinasa C isoforma θ (PKCθ) (7). Los AG circulan en el suero esterificados en diferentes fracciones: esteres de colesterol (EC) (8), fosfolípidos (FL) (9), triglicéridos (TG) (10) o como AGL (11); el pefil de AG difiere entre estas fracciones; en los EC, FL y TG el contenido de AG se afecta por la ingesta alimentaria a corto plazo, por lo cual pueden reflejar más el consumo de alimentos que los procesos metabólicos, mientas que la fracción de AGL refleja más los AG liberados desde el tejido adiposo (12), por esto la fracción de AGL circulantes, obtenida de suero en ayunas, podría reflejar la composición de AG del tejido adiposo y utilizarse en individuos con obesidad central como un marcador de daño metabólico temprano conducente a enfermedad crónica.
En adultos sanos se ha encontrado un patrón de AGL caracterizado por una mayor proporción de AG palmítico-16:0 y oleico-18:1n9, en menor proporción esteárico-18:0, mirístico-14:0 y palmitoléico-16:1n7, los cuales se ha visto que tienen correlación con la composición del tejido adiposo (12). Algunos estudios en adultos han encontrado relación de los AGL con RI y obesidad abdominal (13), no obstante, esta asociación entre AGL, RI y SM aún es controversial, posiblemente porque en los estudios se utilizan diferentes fracciones lipídicas, lo que dificulta la comparación de resultados y confunde las asociaciones.
Los estudios en adultos que solo comparan la fracción AGL también presentan controversia, algunos reportan bajas proporciones de AG saturados (AGS) y altas de AG poliinsaturados (AGPI) (14) y otros altas proporciones del total de AGS y monoinsaturados (AGM) y bajas de AGPI tanto omega 6 como 3, esta variabilidad en las asociaciones dentro la misma fracción podría deberse a que en los adultos hay mayor efecto de variables intervinientes que modifican el perfil, como desórdenes metabólicos avanzados, enfermedad ateromatosa, exposición a variables de estilo de vida (sedentarismo, comida en exceso, consumo de alcohol y tabaco), que aumentan con los años (15).
En jóvenes la identificación de la composición de AGL podría contribuir a un mejor entendimiento de la relación obesidad - RI - SM, dado que en edades tempranas los análisis se afectan menos por factores de confusión como las variables del estilo de vida y la presencia de enfermedades crónicas. No obstante, en jóvenes los estudios son pocos y nada concluyentes.
Por lo anterior el objetivo del estudio fue comparar el perfil de AGL de jóvenes obesos con y sin SM y explorar la asociación de estos AGL con variables metabólicas: como colesterol total (CT), colesterol LDL (cLDL), colesterol HDL (cHDL), TG, glucemia, insulina, HOMA (homeostatic model assessment), PCRhs (proteína C reactiva ultra sensible) y presión arterial.
Diseño del estudio. Se desarrolló un estudio transversal, que incluyó 96 jóvenes, hombres y mujeres, de 10 a 18 años, seleccionados entre 851 jóvenes participantes en un estudio poblacional previo (16), en el cual se seleccionaron aleatoriamente los participantes, se citaron a una institución prestadora de salud, donde se evalúo antropometría y se les tomó una muestra de sangre para evaluación de parámetros bioquímicos, tanto acudientes como jóvenes firmaron consentimiento informado.
Para el presente estudio se definió el tamaño de muestra con el software Primer® considerando: la diferencia mínima esperada entre el grupo control y caso en la concentración de los AGL palmítico y esteárico de un estudio previo (10), comparación de tres grupos, error alfa de 0,05 y potencia del 85%, para un número de 32 jóvenes por grupo.
Conformación de los grupos. 1) obesos con SM (OBSM): con IMC >P98 (17) y diagnóstico de SM. 2) Obesos sin SM (OBNSM): IMC >P98 y sin SM. 3) Peso Adecuado (PA): IMC entre P15 - P85 y ninguno de los componentes del SM. Los grupos fueron equiparados uno a uno, por: sexo, edad, maduración puberal y estrato socioeconómico.
Criterios de exclusión. Se excluyeron los jóvenes que consumían medicamentos hipolipemiantes, antihipertensivos, hipoglicemiantes, corticosteriodes, hormonas tiroideas y suplementos nutricionales, jóvenes con diabetes tipo 1, deportistas de alta competencia y jóvenes embarazadas o en período de lactancia.
Estrato socioeconómico. Se definió basado en la clasificación del Departamento Administrativo Nacional de Estadística colombiano, como estrato bajo (estrato 1 y 2), medio (estrato 3 y 4) y alto (estrato 5 y 6), el cual se reporta al usuario en la factura de servicios públicos (18).
Evaluación antropométrica. Se midió peso y estatura, y se construyó el índice de masa corporal (IMC: peso/estatura2 (kg/m2) y se clasificó según el estándar de la Organización Mundial de la Salud 2007 (17), se tomaron pliegues de grasa: tricipital (PGT) y subescapular (PGS) y se calculó y clasificó el % de grasa corporal según Lohman (19), se tomó circunferencia de cintura (CC) y se clasificó según Fernández (20). Las mediciones se realizaron con equipos y técnicas de uso internacional (19).
Análisis clínicos y bioquímicos. La maduración puberal se realizó y clasificó por autoreporte según metodología de Tanner. La presión arterial se tomó con tensiómetro de mercurio marca Riester® y se clasificó según metodología de Fourth Task Force (21). Para las pruebas bioquímicas se tomó muestra de sangre venosa antecubital con ayuno entre 10-12 horas y se obtuvo suero que se almacenó a -80°C. Se determinó el CT, cHDL, cLDL y TG por espectrofotometría, en fotocolorímetro RA-50 (Bayer, serie 71663), con kits colorimétricos enzimáticos específicos (BioSystems Reagents and Instruments). Se calculó el índice de Castelli como medida de riesgo cardiovascular, según la fórmula CT/cHDL, y se clasificó como alto riesgo valores >5 para hombres y >4,5 para mujeres (22).
La glucemia e insulina se determinaron por Enzimoinmunoensayo en micropartículas (MEIA). Se definió hiperglucemia con glucemia >100mg/dL según ATPIII (23). La RI fue estimada por el modelo matemático índice HOMA (Homeostasis Model Assessment) utilizando el software HOMA Calculator Version 2.2.2 de © Diabetes Trials Unit de la Universidad de Oxford. Se definió RI con un valor ≥3.1, con base en tres criterios: 3.1 fue el valor de RI en el p95 de los 851 jóvenes de la población del estudio marco de la cual se derivó esta investigación (16), según el punto de corte ya publicado por Lee JM et al en 2006 (24) y confirmado como clasificatorio de RI en pre-púberes y púberes por Yin et al en 2013 (25). La PCRhs se determinó mediante inmunoturbudimétria y se clasificó como riesgo cardiovascular bajo <1mg/L, promedio entre 1-3mg/L y riesgo alto >3mg/L (26).
Clasificación de SM. Se diagnosticó SM cuando el joven presentaba tres o más de los siguientes criterios: TG≥110 mg/dL, cHDL≤40 mg/dL, glucemia en ayunas ≥100 mg/dL, presión arterial en mmHg ≥ P90 y CC≥ P90 (27).
Perfil de ácidos grasos libres circulantes. Para la extracción de lípidos del suero humano y derivatización de AG los lípidos fueron extraídos con cloroformo/metanol (2:1) basados en el método de Folch (28). En el análisis por cromatografía de gases (GC) los metil-esteres de AGL fueron analizados en un cromatógrafo de gases Agilent 6890N con detector de ionización en llama (FID), columna capilar TR-CN100, 60 m x 250 μm x 0.20 μm ID, inyector split/splitless con una relación Split 100:1, volumen de inyección 1.0 uL, temperatura del inyector 260°C, programa de temperatura del horno, iniciando a 90°Cx7 min, aumento a una tasa de 5°C/min hasta 240°C por 15 min, temperatura del detector 300°C, gas de arrastre He a un flujo de 1.1 mL/min. Para la identificación de los AG se utilizó estándar (FAME Mix de 37 componentes, Supelco). Los resultados se presentan como cantidad relativa de cada AG (% del total AG).
Las concentraciones del total de AGS, AGM y AG omega 6 (AGω6) fueron calculados por la suma de cada uno de los AG de 14 a 22C de cada una de las familias. Para la familia omega 3 (AGω3) no se realizó sumatoria, ya que α-linolénico-18:3n3 y eicosapentaenoico-20:5n3 (EPA-C20:5n3) se detectaron pero en cantidades no cuantificables, de esta familia se tomó en cuenta el docosahexaenoico (DHA-22:6n3). Se calculó la relación ω6/ω3 (18:2n6+20:3n6+20:4n6/18: 3n3+22:6n3), cuando linolénico-C18:3n3 fue cuantificable, cuando no, se tuvo en cuenta solo DHA-22:6n3. Se calcularon las relaciones producto/precursor como indicador indirecto de la actividad de las enzimas desaturasas, las relaciones estimadas fueron: delta 9 desaturasa (D9D)=16:1n7/16:0 (palmitoléico/palmítico) y 18:1n9/18:0 (oleico/esteárico), delta 5 desaturasa (D5D)=20:4n6/20:3n6 (araquidónico/DHGL) y delta 6 desaturasa (D6D)=20:3n6/18:2n6 (DHGL/AL), como previamente se ha reportado (8,29)
Manejo ético. La investigación clasificó con riesgo mínimo según el Ministerio de Salud de Colombia, resolución 008430, artículo 11, Octubre de 1993. El proyecto fue aprobado por el Comité de Bioética de la Sede de Investigación Universitaria (SIU) de la Universidad de Antioquia, certificado número 10-11-328. Todos los participantes y padres firmaron el consentimiento informado que incluyó la declaración de Helsinki.
Análisis estadístico. Se comprobó normalidad de las variables continuas con la prueba Shapiro Wilks, la diferencia entre grupos se evalúo por ANOVA ó Kruskal Wallis ó prueba t ó U de Mann Whitney, según corresponde; las frecuencias de variables categóricas se realizó con Chi2. Las correlaciones se realizaron mediante R de Pearson o Rho de Spearman. La asociación entre cada AG con algunas variables categóricas se hizo mediante razón de disparidad (OR). Se consideró como significativo una p<0,05. Para el análisis estadístico se usó el programa Statistical Package for the Social Sciences, SPSS® V 21.0.
Características antropométricas y bioquímicas de los jóvenes. Las variables de equiparamiento entre los grupos no mostraron diferencias significativas (Tabla 1). 56,3% de los jóvenes eran hombres, la edad promedio fue 14,1±2,4 años; 88,5% pertenecía a los estratos medio y bajo, 12,5% eran pre-púberes y 63,5% pos púberes.
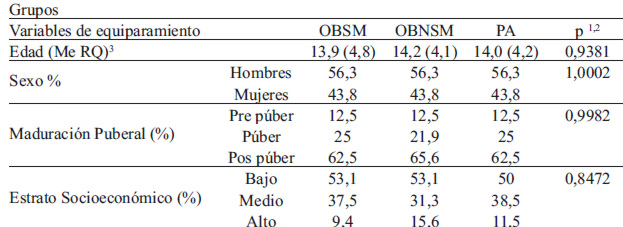
Los promedios de IMC y CC mostraron diferencias significativas entre los tres grupos (P<0,001 ambas medidas), siendo mayores en el grupo OBSM, en el cual 53,1% de los integrantes tenían la CC alta (P>90) mientras que en los otros grupos no se encontró obesidad central. Las variables de adiposidad (PGT, PGS y % de grasa) no presentaron diferencias significativas entre los 2 grupos de obesos, pero si con el grupo de PA (Tabla 2).
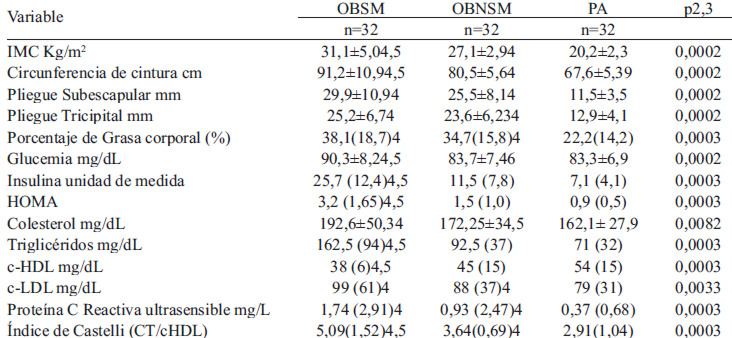
La glucemia mostró diferencias significativas (P<0,001) entre OBSM y los otros grupos, pero no entre OBNSM y PA, 18% de los jóvenes OBSM tenían hiperglucemia; las concentraciones de insulina y HOMA fueron significativamente mayores en OBSM, que triplico y duplico los valores frente a OBNSM y PA, respectivamente (P<0,001). 53,1% de OBSM presentaron alto HOMA, (Tabla 2) y CC alta; estas dos medidas mostraron correlación positiva (Rho=0,718; P=0,0001).
Los TG y el cHDL mostraron diferencias significativas entre OBSM y los otros grupos (P<0,00 ambas medidas) (Tabla 2). 93,7% de los OBSM presentaron al mismo tiempo TG altos y cHDL bajas. El índice de Castelli fue más alto en OBSM (5,2) con respecto a OBNSM y PA (3,5 y 2,9 respectivamente) y significativamente diferentes entre todos los grupos (P<0,001) (Tabla 2). 65,6% de los OBSM presentaron riesgo coronario alto.
La PCRhs no mostró diferencias significativas entre OBSM y OBNSM, pero si al comparar estos dos grupos con PA, con valores mayores en los obesos (P<0,001) (Tabla 2), además el riesgo de inflamación crónica leve (PCRhs >1mg/dL) en los jóvenes obesos fue 2,6 veces mayor comparado con los de PA (OR 2,6; IC 1,272 – 5,544; P=0,001).
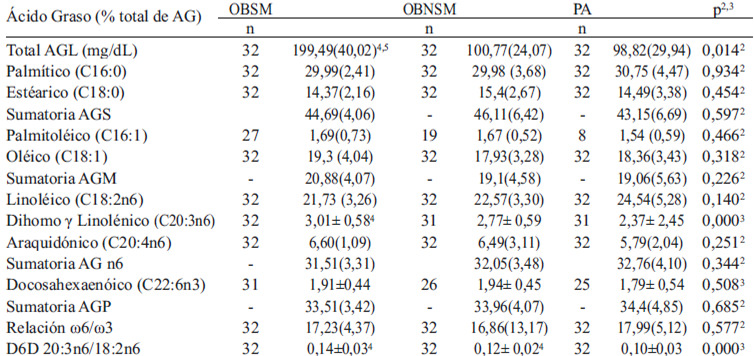
Composición de AGL. El total de AGL fue significativamente mayor en el grupo OBSM, con concentraciones del doble comparado con los otros grupos (P=0,014). La mayor proporción de AGL fue de AGS, seguida de AGPI y la menor fue de AGM en todos los grupos, sin diferencia significativa. Los AGS con mayor concentración fueron palmítico-16:0 y esteárico-18:0. El oleico-18:1n9 fue el AGM de mayor concentración sin diferencias por grupo. El palmitoléico-16:1n7 se presentó en el 71,9% de los obesos y solo en el 25% de los adecuados, lo que evidenció una asociación significativa de este AG con obesidad (P<0,001).
La suma de AGPI no mostró diferencia significativa entre los grupos. La concentración más alta de AGPI fue de linoléico-18:2n6, aunque sus concentraciones fueron más bajas en los grupos de obesos; araquidónico-20:4n6 y DHGL-20:3n6 se encontraron más altos en los grupos con obesidad (OBSM y OBNSM), siendo significativamente más alto DHGL-20:3n6 en OBSM que en adecuados. De la familia omega 3, no se pudo cuantificar αlinolénico-18:3n3 y EPA-20:5n3 solo se encontraron pequeñas concentraciones de DHA-22:6n3. La relación omega6/omega3 no mostró diferencias significativas entre los grupos.
En las relaciones producto/precursor se encontró que la relación DHGL-20:3n6/linoléico-18:2n6 fue significativamente más alta en los grupos de obesos que en el grupo de PA (P<0,001), pero no entre los obesos (Tabla 3), las relaciones estimadas de D9D y D5D no mostraron diferencias significativas.
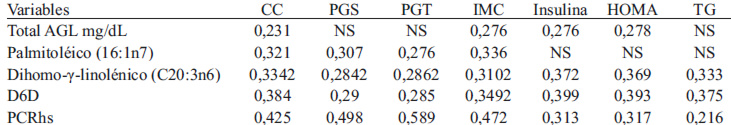
Correlación entre variables bioquímicas y AGL. Se encontró asociación positiva y significativa entre el total de AGL con IMC, CC, insulina y HOMA, además entre el AG palmitoléico-16:1n7 y medidas de adiposidad. También entre el DHGL-20:3n6 con insulina, estas y otras correlaciones se aprecian en la Tabla 4.
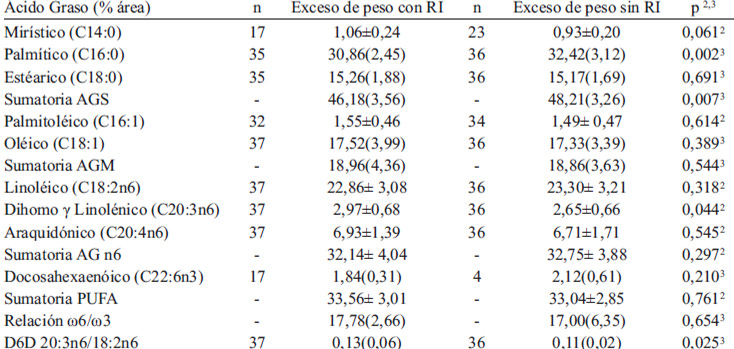
Con el fin de explorar si la relación DHGL-20:3n6 y SM se asociaba específicamente con la presencia de RI se realizó un sub-análisis, derivado del mismo estudio marco (13), comparando dos grupos de jóvenes con exceso de peso, uno con RI (n=37) y otro sin RI (n=36). Se encontró que el grupo de jóvenes con exceso de peso y RI también tenía significativamente mayor concentración de DHGL-20:3n6 y mayor relación DHGL-20:3n6/linoléico-18:2n6 (D6D) que los jóvenes con exceso de peso sin RI (Tabla 5). Además en jóvenes con exceso de peso y RI el DHGL-20:3n6 correlacionó directa y significativamente con variables como PCRhs, insulina, HOMA, TG, % de grasa y CC (datos no publicados).
Las características comunes a los dos grupos de obesos (OBSM y OBNSM) independiente del desarrollo de SM fueron la mayor adiposidad y el mayor estado inflamatorio (PCRhs), igualmente los obesos presentaron significativamente mayor frecuencia del AGM palmitoléico-16:1n7, que ya se había reportado en adultos, en diferentes fracciones (8,30). Paillard reportó altas concentraciones de palmitoléico-16:1n7 en adultos con exceso de peso comparados con PA, y encontró fuerte asociación entre este, los TG y la CC (30), igualmente Warensjö y Perxachs en adultos con SM encontraron el palmitoléico-16:1n7 más alto (8,31). En niños se han encontrado patrones similares, Okada determinó que el palmitoléico-16:1n7 fue más alto en obesos y correlacionó con variables antropométricas como % de grasa y CC, igual a lo hallado en esta investigación (11). Gil-Campos encontró que el palmitoléico-16:1n7 se encuentra más alto en el total de AGL, TG y EC en niños OBSM comparados con los de PA (10), igual a lo encontrado por Decsi en EC y FL (9), este AG correlacionó positivamente con la ingesta de carbohidratos y el riesgo de SM (10); el aumento de este AG se deber posiblemente a un aumento de la lipogénesis en obesidad, ya que este AG, junto con el palmítico-16:0, es uno de los productos finales de la síntesis endógena y no se encuentra comúnmente en los alimentos, lo que refleja el flujo de carbonos aportados por las grasas y carbohidratos dietarios para la síntesis de AG y el almacenamiento hepático de lípidos (10,11).
El grupo OBSM mostró diferencias significativas con valores mayores que los OBNSM y PA, en la CC, glucemia, insulina, HOMA, TG, e índice de Castelli y más bajos de cHDL, con 51,3% de los jóvenes con CC alta y RI. Estos hallazgos confirman la asociación entre la obesidad central y las alteraciones propias del SM, similares a los de Gil (10). Los OBSM presentaron concentraciones significativamente mayores de AGL totales similar a lo hallado por Reinehr (32), este además encontró correlación significativa entre el total de AGL, CC, insulina y HOMA (32), lo que sugiere que en quienes se presenta obesidad central, los adipocitos aumentan la liberación de AG, que una vez circulantes son lipotóxicos y se asocian con el desarrollo de RI y SM. Las variables TG, cHDL, glucemia, insulina y HOMA más altas en OBSM, no fueron significativamente diferentes entre los jóvenes OBNSM y los de PA, estos grupos tampoco difirieron en el total de AGL, ni en los tipos de AGL del suero. Estos resultados indican que el riesgo de enfermedad en los adolescentes obesos no está directamente asociado con el IMC, y que la conexión entre la obesidad y las alteraciones metabólicas (configuradas en SM) está más asociada al exceso de grasa visceral, que produce liberación de AG, que pueden causar lipotoxicidad, RI y finalmente producir acumulación de lípidos en el hígado y generar enfermedad de hígado graso no alcohólico (33).
Lo anterior sugiere que la susceptibilidad de los jóvenes obesos a sufrir alteraciones metabólicas que incrementan el riesgo de enfermar no es igual para todos, posiblemente por el diferente grado de exposición que puedan tener a factores ambientales, del estilo de vida y genéticos que predisponen a obesidad, en este sentido un estudio realizado en estos jóvenes encontró que la asociación de algunas variantes génicas con obesidad se modificaba según el estilo de vida, por ejemplo el genotipo I/I de SNP19 de la calpaína (CAPN10) se asoció significativamente con exceso de peso aún en jóvenes activos, mientras algunas variantes de los genes FTO y UCP3 mostraron tener efecto sobre la obesidad solo cuando los jóvenes eran sedentarios (34).
El grupo OBSM presentó significativamente mayor concentración de DHGL-20:3n6 que PA, resultado que concuerda con lo reportado en adultos, en quienes se ha asociado DHGL-20:3n6 en EC con obesidad y SM (8,35); en niños y jóvenes con exceso de peso y SM se ha encontrado mayor proporción de este AG tanto en FL (9,29) como EC (15,29). Esta asociación con SM se reforzó al encontrar que DHGL-20:3n6 presentó correlación positiva y significativa con CC y HOMA, igual que en el estudio de Steffen (29), aunque estas correlaciones fueron débiles, orientaron a pensar que DHGL-20:3n6 podría estar alto en aquellos jóvenes obesos con SM y RI, más que en aquellos obesos con SM sin RI. Por lo anterior, se realizó un sub-análisis que permitiera confirmar la asociación de DHGL-20:3n6 con RI, en jóvenes con exceso de peso, en el cual se encontró que este AG correlacionó con PCRhs, insulina, HOMA, TG, % de grasa y CC. En adultos reportaron resultados similares donde el DHGL-20:3n6 en EC y FL se asoció con marcadores de RI y DM (36). Este AG (DHGL-20:3n6) se produce a partir del AG esencial linoléico-18:2n6 después de ser desaturado por la D6D y elongado; posteriormente otra desaturación catalizada por la D5D produce el araquidónico-20:4n6 (8); esta línea da origen a eicosanoides vasoactivos que se incrementa en obesidad abdominal asociándose con inflamación (PCRhs). Sin embargo, en los jóvenes con obesidad y SM de este estudio el aumento de DHGL-20:3n6 no se acompañó de incremento en el AG araquidónico-20:4n6. Esta mayor concentración de DHGL-20:3n6 precursor de tromboxanos y prostanoides de la serie 1 por la vía de la ciclooxigenasa, podría potenciar la actividad antiinflamatoria y posiblemente indicar que el aumento del DHGL-20:3n6 sería un mecanismo compensatorio para mantener el balance entre sustancias pro y antiinflamatorias, más que el causante de las alteraciones metabólicas de SM, como RI, estrés oxidativo y mayor estado inflamatorio (37).
La relación para D6D (DHGL-20:3n6/linoléico-18:2n6) fue significativamente mayor en los dos grupos de obesos frente al de PA, debido a la mayor proporción de DHGL-20:3n6. En adultos esta relación en FL correlacionó con IMC y RI y asoció con riesgo de SM (8), además se ha relacionado con altos niveles de péptido C (marcador temprano de insulinemia y RI) (36); en niños D6D se ha encontrado más alta en jóvenes con sobrepeso, que de PA en FL y EC, y se han encontrado asociación con medidas de adiposidad como IMC y CC, y bioquímicas como triglicéridos e insulina en la fracción de FL (29), igual que en la presente investigación pero en la fracción de AGL.
En estos jóvenes no se detectó, en la fracción de AGL, αlinolénico ni EPA, solo DHA y en concentraciones muy bajas. Estudios previos ya habían relacionado la obesidad con depleción de AGPI omega 3 (9), posiblemente por una desaturación defectuosa del αlinolénico por parte de las desaturasas D6D y D5D. Los AGPI de cadena larga reprimen la expresión de las desaturasas D5D y D6D, por lo tanto la depleción de AGPI ω3 podría inducir su expresión y la de los receptores SREBP-1c promoviendo lipogénesis, mientras deprime la expresión de PPARα y con ello la βoxidación de AG, lo cual podría explicar la asociación que se encontró en este estudio entre la D6D con adiposidad, (38,39). En el grupo OBSM aunque sin diferencia significativa, se observó una tendencia a mayores concentraciones de AGM y menores de omega 6, frente a los dos grupos pero menores concentraciones de AGS y DHA-22:6n3 frente al grupo OBNSM, resultados similares a los reportados por Decsi y Platat en FL (9,15) quienes encontraron menor cantidad del total de AG omega 6 y linoléico-18:2n6, y altas cantidades del total de AGM y DHGL-20:3n6 en niños OBSM frente a PA (9,15), debido posiblemente a un cambio en el metabolismo en SM, pues el aumento en la lipogénesis, podría estimular la producción de AGM como palmitoléico-16:1n7 y AGP como DHGL-20:3n6, disminuyendo los AG precursores de esas vías. En el análisis con dos grupos (RI y no RI), el grupo con RI se repite el comportamiento, mayores cantidades de AGM, menores de omega 6, DHA-22:6n3, AGS y palmítico-16:0, estos últimos significativamente más bajos frente al grupo sin RI.
Este estudio presentó algunas limitaciones metodológicas, el diseño “transversal” no permite establecer relaciones causales; no se analizó el componente alimentario, el cual pudo tener influencia en los resultados obtenidos; la estimación de las enzimas desaturasas se realizó con por la medición de la relación producto/precursor, que es un método indirecto y puede estar influenciado por el consumo de alimentos y por último este estudio solo tuvo en cuenta la PCRhs como estimativo de estado inflamatorio, reconociendo que el estado pro-inflamatorio de bajo grado es componente importante del SM y hay otras medidas que pueden estimar de manera más precisa este componente
Los obesos desarrollaron mayor CC, inflamación (PCRhs) y cLDL; en relación con los AGL, los obesos presentaron con mayor frecuencia AG palmitoléico-16:1n7 y mayor concentración media de DHGL-20:3n6 reflejando mayor lipogénesis. Una vez el joven obeso desarrolla SM y CC alta, permanece la inflamación y aparece la RI, las alteraciones metabólicas y los índice de riesgo cardiovascular se hacen más grades; aumenta el total de AGL circulantes, el DHGL-20:3n6 y la relación 20:3n6/18:2n6 indicativa de la actividad de D6D, con lo que se confirma la asociación entre obesidad central, los componentes del SM, lipolisis aumentada en el tejido adiposo visceral y la inflamación.
Este estudio fue financiado con recursos de Colciencias, Convocatoria 569, contrato 487- 2012 y la Universidad de Antioquia con fondos del CODI 2013-2014.
Recibido: 08-08-2014
Aceptado: 14-11-2014