En este trabajo se evaluaron la composición, algunas características físicas (densidad, índice de refracción y color), capacidad antioxidante (DPPH) y perfil de ácidos grasos de semillas de mostaza negra (Brassica nigra) y amarilla (Brassica alba), sus aceites y residuos de la extracción del aceite. La densidad de los aceites de mostaza negra y amarilla fue de 0,912 ± 0,01 y 0,916 ± 0,01 g/mL, respectivamente; y el índice de refracción fue de 1,4611 ± 0,01 y 1,4617 ± 0,01, respectivamente, no mostrando diferencias significativas (p>0,05) entre las dos mostazas. Los parámetros de color del aceite de semilla de mostaza negra y amarilla tienden hacia los tonos amarillos-verdosos y tonos amarillos-rojizos, respectivamente; respecto a la actividad antioxidante, se observó una variación desde 25 mg equivalentes de Trolox/100 g en el aceite de semilla de mostaza amarilla hasta 1,366 mg equivalentes de Trolox/100 g en la pasta residual de mostaza negra. El perfil de ácidos grasos de la semillas de mostaza negra muestran que el ácido graso predominante es el oleico (22,96%), seguido por linoleico (6,63%) y linolénico (3,22%), mientras que para la semilla de mostaza amarilla es el erúcico (6,87%), seguido por oleico (5,08%) y linoléico (1,87%).
Palabras clave: Capacidad antioxidante, DPPH, mostaza negra (Brassica nigra), mostaza amarilla (Brassica alba).
The composition, some physical properties (density, refraction index, and color), antioxidant capacity (DPPH), and fatty acid profile of seeds of black (Brassica nigra) or yellow mustard (Brassica alba) were evaluated, as well as for their oils and residues from oil extraction. Density of the black and yellow mustard oils were 0.912 ± 0.01 and 0.916 ± 0.01 g/mL, respectively; their refraction indexes were 1.4611 ± 0.01 and 1.4617 ± 0.01, respectively; being not significantly different (p>0.05) between two mustards. Color parameters of the black and yellow mustard oils presented greenish-yellow tones and reddish-yellow tones, respectively; regarding antioxidant activities, these ranged from 25 mg equivalents of Trolox/100 g in the yellow mustard oil to 1,366 mg equivalents of Trolox/100 g in the residues from oil extraction of black seed mustard. The fatty acid profile of the black mustard seed revealed that its predominant fatty acid is oleic (22.96%), followed by linoleic (6.63%) and linolenic (3.22%), whereas for yellow mustard seed the major fatty acid is erucic (6.87%), followed by oleic (5.08%) and linoleic (1.87%) acids.
Key words: Antioxidant capacity, DPPH, black mustard (Brassica nigra), yellow mustard (Brassica alba).
https://doi.org/10.37527/2015.65.2.008
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla, México
Existen numerosos reportes relacionados a la actividad antioxidante de fracciones de plantas y especias (1). Los antioxidantes sintéticos están siendo restringidos debido a posibles efectos negativos relacionados con la salud (2). Por otra parte, una gran variedad de especias han sido reconocidas por tener propiedades medicinales y poseer efectos benéficos para la salud, tales como actividad antioxidante, estimulación digestiva, actividad antimicrobiana, efecto hipolipidémico, actividad anti-mutagénica y potencial anti-carcinogénico, entre otros (3, 4).
La mostaza (Brassica spp.) es una de las especias que desde la antigüedad ha sido usada como fuente de aceite comestible e ingrediente en infinidad de alimentos; además en la medicina tradicional, como antídoto contra picaduras de escorpión y mordidas de víboras. Esta especia ocupa el tercer lugar como el condimento más importante después de la sal y la pimienta. Las mostazas son miembros de las familias Cruciferaceae o Brassicaceae. El género Brassica consiste de 150 especies de plantas anuales o bienales, algunas de las cuales son cultivadas para obtener aceite o ser usadas como forraje. Las tres especies de mostaza más cultivadas son las llamadas, negra (Brassica nigra), blanca o amarilla (Brassica alba) y parda (Brassica juncea). La diferencia entre estos tipos de mostazas son los compuestos químicos denominados glucosinolatos; la semilla de mostaza amarilla contiene “sinalbina” y las semillas de mostaza parda y negra contienen “sinigrina”. Estos glucosinolatos son compuestos que se encuentran en forma natural en las plantas de la familia Brassicaceae, y son parte de su mecanismo de defensa frente a insectos, los glucosinolatos pueden presentarse junto con la enzima que los puede hidrolizar, y son los responsables de los olores y sabores característicos tanto de la semilla como de los productos de mostaza (5). La toxicidad de los glucosinolatos, en dosis elevadas, es atribuida a la actividad de sus derivados hidrolizados: los isotiocianatos, tiocianatos, oxazolidinonas y los nitrilos (6).
Los extractos obtenidos de semillas del género Brassicaceae tienen potente actividad antioxidante; esta se debe a los compuestos fenólicos presentes (7). Las harinas obtenidas de semillas de mostaza contienen compuestos fenólicos bioactivos en forma de ácido sinápico y sus derivados; estos compuestos han demostrado fuerte actividad antioxidante en comparación con otros antioxidantes naturales (8). Los compuestos bioactivos son componentes minoritarios de los alimentos, considerados no nutrientes, parcialmente biodisponibles en el organismo y que han demostrado tener diversos efectos positivos en la salud del consumidor. Los polifenoles y arotenoides ejercen su principal acción biológica a través de mecanismos de anti-oxidación y secuestro de radicales libres (9).
Existen diversos estudios relacionados con la composición química y biosíntesis de algunos compuestos (10, 11) en semillas de mostaza; sin embargo, existen pocos estudios relacionados con las características físicas y actividad antioxidante de estas semillas (7, 12) así como de sus productos. El propósito de este estudio fue evaluar la composición, algunas características físicas, capacidad antioxidante y perfil de ácidos grasos de semillas de mostaza negra y amarilla, sus aceites y residuos de la extracción de dichos aceites.
Las semillas de mostaza negra (Brassica nigra) y amarilla (Brassica alba) se adquirieron en tiendas de materias primas de la Ciudad de Puebla (México). Los ácidos 2,2´-Difenil-1-picrilhidracilo (DPPH), 6-hidroxi-2,5,7,8-tetrametilcroman-2carboxílico (Trolox), pirogálico y tridecanoico, la solución de amiloglucosidasa, la solución de α-amilasa estable y proteasa fueron adquiridos de Sigma Chemical Co. (St. Louis, MO, EE.UU.). El metanol, ácido clorhídrico, éter etílico, sulfato de sodio, trifluoruro de boro (grado analítico), ácido nítrico, etanol, acetona, fosfato dibásico de sodio anhidro, fosfato monobásico monohidratado de sodio, hidróxido de sodio y ácido sulfúrico fueron adquiridos de J.T. Baker Chemical Co. (Philipsburg, NJ, EE.UU.).
Extracción de aceite: Se empleó un extractor tipo prensa para extracción de aceites marca Samson GB-9001 (Seúl, Corea del Sur) para obtener en frío el aceite a partir de semillas de mostaza amarilla y negra, el aceite extraído se filtró para eliminar los residuos. El aceite y la pasta residual después de la extracción del aceite se almacenaron en refrigeración (4ºC) hasta su análisis (no más de 1 día).
Densidad, índice de refracción y color de los aceites: La densidad de los aceites se determinó mediante el uso de un picnómetro de vidrio. Éste se llenó con el aceite y se colocó en un baño con agua destilada a 25°C durante 15 min. La densidad se calculó mediante la relación masa/volumen. El índice de refracción de los aceites de mostaza se determinó con un refractómetro digital Reichert AR200 (Depew, NY, EE.UU.) a 25ºC de acuerdo a la metodología propuesta por la AOAC (13). El color de los aceites se midió transfiriendo 15 mL a una celda de cuarzo usando un colorímetro Color Gard System 05 (BYK Gardner, Reston, EE.UU.). Se determinaron los parámetros L*, a*, b* en modo de transmitancia.
Análisis proximal: El análisis proximal se realizó en las semillas y pastas residuales (después de la extracción del aceite) de mostaza. Las determinaciones de humedad, grasa (extracto etéreo), proteína, contenido de cenizas y contenido de fibra dietética se ejecutaron de acuerdo a las metodologías reportadas en la AOAC (13). Todas las determinaciones se realizaron por triplicado. Los carbohidratos totales se calcularon por diferencia.
Capacidad antioxidante: La capacidad antioxidante se determinó en extractos obtenidos según lo reportado (14, 15) y de acuerdo al método descrito por Sreeramulu y Raghunath (12) y por Yu et al. (16). Se obtuvieron extractos de acuerdo a la metodología reportada por Sing et al. (14) con ligeras modificaciones. La extracción de los compuestos con capacidad antioxidante se realizó con diferentes cantidades de muestra dependiendo de su naturaleza (aceite, pasta residual de la extracción de aceite o semilla entera). Se emplearon 15 mL de aceites de mostaza negra y amarilla, y 500 mg de semilla entera (molida) o pasta residual de la obtención del aceite. Las diferentes cantidades de muestra se mezclaron con 20 mL de metanol al 70% acidificado con HCl al 0,1% y se agitaron durante 4 h a temperatura ambiente (13). Posteriormente, las muestras se centrifugaron a 10.000 rpm durante 15 min a 10ºC; el sobrenadante se separó y se filtró a través de papel filtro Whatman No.1.
La actividad de atrapamiento del radical DPPH se basa en la habilidad del antioxidante para atrapar cationes del radical DPPH (16). Se tomaron 100 μL de cada uno de los extractos y se colocaron en tubos de ensayo, se añadieron 2,9 mL de DPPH (0,1 mM), se mezclaron vigorosamente usando un vortex y se midió la absorbancia inicial (ABS inicial) a 517 nm usando un espectofotómetro UV-visible marca UNICO® 2800H (Dayton, NJ, EE.UU.). A la mezcla se le dejó reaccionar en oscuridad por 30 min (tiempo seleccionado en base a pruebas previas, y que corresponde al tiempo suficiente para el desarrollo de la reacción) a temperatura ambiente y se midió la absorbancia final (ABS final) a 517 nm. Con los datos anteriores se calculó el % de inhibición aplicando la Ecuación 1.
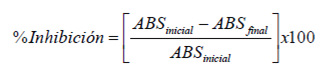
A partir del porcentaje de inhibición y la ecuación de la curva estándar del antioxidante de referencia se calculó la concentración del antioxidante (expresado en equivalentes de Trolox) en la muestra. Para la preparación de la curva estándar, en tubos de ensayo se colocaron desde 0 hasta 100 μL de Trolox de concentración 25 mg/100 mL, el volumen correspondiente de metanol al 70% acidificado con HCl al 0,1% para hacer un volumen de 100 μL, se mezclaron perfectamente y posteriormente se siguió el mismo procedimiento que para los extractos. Una vez obtenidas las absorbancias, se calculó el porcentaje de inhibición de acuerdo a la Ecuación 1 y se graficaron los promedios de cada solución estándar en función de la concentración (μg) de Trolox presente. Al graficar los datos anteriores, se obtuvo por regresión lineal la ecuación de la curva estándar para obtener la concentración de Trolox presente en las muestras analizadas.
Perfil de ácidos grasos en semillas de mostaza y aceites de mostaza: El análisis de composición de ácidos grasos fue realizado de acuerdo al método 996.06 de la AOAC (13). Los ácidos grasos fueron transformados en metil-ésteres añadiendo 2 mL de éter etílico a 100 mg de la grasa extraída de las semillas o aceite y evaporando a sequedad en un baño María a 40°C. Posteriormente se enfrío la mezcla y se añadieron 2 mL de trifluoruro de boro (7% BF3) y 1 mL de tolueno incubando a 100°C por 45 min. La solución fue enfriada y mezclada con 1 mL de n-hexano, 1 mL de agua destilada y 1 g de sulfato de sodio, esta mezcla se agitó por 1 min y se formaron dos capas; se tomaron de la capa superior los metilésteres y fueron transferidos a un vial de 2 mL y almacenados a 4°C para su posterior análisis por cromatografía. La composición de ácidos grasos se determinó por cromatografía de gases con un equipo Agilent Technologies 6890 Series GC System (Palo Alto, CA, EE.UU.) acoplado a un detector de ionización de flama y una columna capilar SUPELCO SP2560 de 32mm de D.I. x 0.25μm de df (Bellefonte, PA, EE.UU.). La temperatura inicial del horno fue 50°C (2 min) y se incrementó hasta 250°C (10 min) a 12°C/min. La temperatura del detector fue 300°C. El gas de arrastre fue helio de alta pureza (99,999%), usado a un flujo de 40 mL/s y el gas auxiliar fue nitrógeno a un flujo de 30 ml/min. El inyector Split (10:1) se mantuvo a 250°C y el volumen de inyección fue de 1,0 μL. La identificación de los metilésteres de ácidos grasos se realizó por comparación directa de sus tiempos de retención con el patrón FAME (Fatty Acid Methyl Ester Mix SUPELCO Cat. N°18918-1 AMP).
Análisis estadístico: Los resultados se expresan en términos de la media y la desviación estándar de al menos 3 determinaciones independientes. Los resultados fueron analizados mediante análisis de varianza (α = 0,05) utilizando el programa Minitab 16 (Minitab, Inc. PA, EE.UU.).
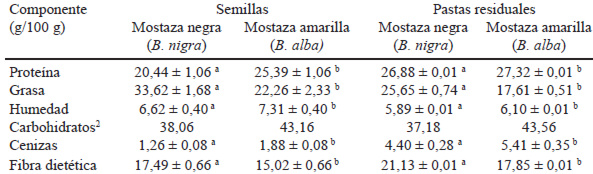
En la Tabla 1 se muestran los resultados obtenidos de la composición proximal de las semillas de mostaza negra y amarilla, así como para las pastas residuales, resultantes de la extracción de aceite. Las semillas de mostaza analizadas se caracterizan por su bajo contenido de humedad (6,62% y 7,31% para semilla de mostaza negra y amarilla, respectivamente), elevado contenido de grasa, 33,62% y 22,26% para mostaza negra y amarilla, respectivamente; así como un aporte proteínico importante Los contenidos de proteína fueron de 26,88% y 27,32% para las pastas de semillas de mostaza negra y amarilla, respectivamente, mientras que el contenido de cenizas fue mayor en la pasta de mostaza amarilla que en la pasta de mostaza negra. Otro de los componentes mayoritarios fue la fibra dietética, esta se encontró en mayor porcentaje en la pasta de semilla de mostaza negra en comparación con la encontrada en la pasta de semilla de mostaza amarilla.
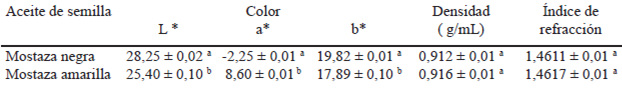
Para analizar las características físicas de los aceites, fue necesario obtener las muestras de aceite a partir del prensado mecánico de las semillas de mostaza negra y mostaza amarilla. Para el caso de la semilla de mostaza negra se obtuvo un rendimiento del 30,6% de aceite y para la mostaza amarilla del 41,2%. En la Tabla 2 se muestran los resultados obtenidos para densidad, color e índice de refracción de los aceites de las semillas de mostaza estudiadas. Los valores encontrados son similares para los aceites de ambas semillas. Con respecto al color, L* designa la luminosidad (0 negro; 100 blanco), a* la contribución de color rojo (+) o verde (-) y b* color amarillo (+) o azul (-). De acuerdo a los resultados obtenidos, el aceite de semilla de mostaza negra tiende hacia colores amarillos-verdosos y el aceite de mostaza amarilla tiende hacia colores amarillos-rojizos.
En la Tabla 3 se muestran los resultados obtenidos respecto a la capacidad antioxidante de las semillas y de los diferentes productos derivados de las mostazas estudiadas. Las semillas de mostaza contienen cantidades importantes de compuestos extraíbles en comparación con los aceites y por lo tanto mayor actividad antioxidante. La actividad antioxidante varía de 25,88 mg Trolox/100 g en el aceite de semilla de mostaza amarilla, hasta 1366,88 mg Trolox/100 g en la pasta residual de la semilla de mostaza negra.

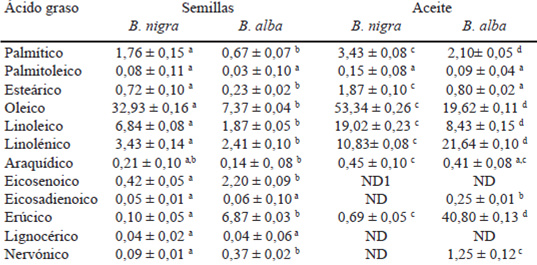
La concentración de ácidos grasos en semillas y aceites de mostazas negra y amarilla se muestran en la Tabla 4. Para la semilla de mostaza negra el ácido graso predominante es el oleico (32,93%) seguido por el linoleico (6,84%) y linolénico (3,43%). La cantidad total de ácidos grasos mono-insaturados es mayor en el aceite de mostaza amarilla en comparación con los determinados en el aceite de mostaza negra, este mismo comportamiento se observa para el caso de los ácidos grasos poliinsaturados. El perfil de ácidos grasos muestra valores importantes, en el caso de la mostaza amarilla, para los ácidos erúcico (40,80%), linolénico (21,64%), oleico (19,62%) y linoleico (8,43%) y en el caso de la mostaza negra el ácido predominante es el oleico (53,34%), seguido por linoleico (19,02%) y linolénico (10,83%). Estos porcentajes son importantes debido a que la calidad y digestibilidad de los aceites vegetales comestibles son determinadas por la cantidad y composición de ácidos grasos insaturados. De acuerdo a los resultados obtenidos (Tabla 4), los perfiles de ácidos grasos son diferentes para las semillas y los aceites de mostaza. En el caso del aceite de mostaza negra, éste contiene mayor cantidad de ácido linolénico (10,83%) y linoleico (19,02%) en comparación con la cantidad de ácido linolénico (3,43%) y linoleico (6,84%) presente en la semilla de la misma especie, este mismo comportamiento se observa para el aceite de mostaza amarilla en comparación con la semilla.
Los resultados obtenidos en el análisis proximal muestran que el aporte proteínico observado para las semillas de mostaza amarilla (25,3%) y negra (20,4%) es elevado, en comparación con otras semillas tales como chía (19,9%), linaza (19,9%), amaranto (12-19%), maíz (9,4-14,2%) y trigo (14-17%) (17). Por otra parte, la base de datos de la USDA (15) reporta valores de proteína, carbohidratos y humedad para mostazas similares a los observados en el presente estudio. Cabe mencionar que en la literatura se encuentran diversos estudios que han determinado la composición nutricional de la mostaza sin diferenciar entre las variedades amarilla o negra (15, 17).
Es importante resaltar que las pastas residuales después de la extracción de aceite de las semillas de mostaza negra y amarilla presentaron mayor contenido de proteínas (26,88% y 27,32% respectivamente), y fibra dietética (21,13% y 17,85% respectivamente). En el caso de la fibra dietética, la concentración obtenida es mayor que la encontrada en las semillas enteras y a las reportados en harina de maíz (7,7-12,0 % b.s.), harina de arroz (2,4 % b.s), avena (15,4% b.s), harina de trigo (15,6 % b.s.), y harina de sorgo (6,6% b.s), entre otros (18, 19). Es importante mencionar que la fibra dietética juega un importante rol en la salud intestinal y se ha asociado con la disminución de enfermedades del corazón, hipertensión, diabetes y obesidad (20), por otro lado se ha reportado que una parte de los compuestos bioactivos presentes en las muestras vegetales, ya sean antioxidantes o no, están asociados a los componentes de la fibra dietética, como consecuencia de la habilidad de formar complejos con proteínas y polisacáridos (20-22).Los valores de grasa y humedad de dichas pastas residuales son menores en comparación con los obtenidos para las semillas, este comportamiento era previsible debido al proceso de prensado realizado por el cual se obtuvieron las pastas y el aceite. El rendimiento de aceite obtenido es comparable con los datos reportados (23) cuyos valores oscilan entre 24-40% de rendimiento en aceite. Puede observarse (Tabla 2) que los aceites obtenidos por prensado presentaron valores similares en sus propiedades físicas a los reportados por el Codex Alimentarius (24) para aceites vegetales. Esta norma establece valores para la densidad relativa en un rango de 0,910 a 0,921 g/mL a 20°C y para índice de refracción de 1,461 a 1,469.
Respecto a la capacidad antioxidante observada para las semillas de mostaza negra (1.323,22 mg Trolox/100 g) y amarilla (1.273,57 mg Trolox/100 g), ésta fue mayor al compararla con los valores reportados (12) para girasol (850,12 mg Trolox/100 g), cártamo (228,33 mg Trolox/100 g), linaza (135,32 mg Trolox/100 g) y ajonjolí (154,14 mg Trolox/100 g). La capacidad antioxidante para semilla de mostaza negra determinada en este estudio (1.323,22 mg Trolox/100 g) es similar al reportado (1.155 mg Trolox /100 g) por Sreeramulu y Raghunath (12).
Los valores obtenidos para los aceites de mostaza negra (32,27 mg Trolox/100 g) y amarilla (25,88 mg Trolox/100 g) son mayores que los reportados (12) para aceites de cacahuate (22,1 mg Trolox/100 g), girasol (12,4 mg Trolox/ 100 g) y palma (12,1 mg Trolox/ 100 g). A partir de los resultados obtenidos en este estudio, el orden en el que se observa una mayor capacidad antioxidante de los productos de la mostaza es: pasta residual, semilla y aceite. Estos resultados coinciden con lo reportado por Arranz y colaboradores (25), quienes mencionan que la parte desgrasada de la semilla de mostaza (residuo) presenta mayor capacidad antioxidante. Es importante mencionar que los componentes de la semilla de mostaza negra (Brassica nigra) muestran mayor capacidad antioxidante en comparación con los de la mostaza amarilla (Brassica alba). Estas variaciones son similares a las reportadas para otras semillas; como es el caso del ajonjolí, en el que se menciona que la semilla de ajonjolí negra es ampliamente usada en países asiáticos, debido a su potente actividad antioxidante en comparación con la semilla de ajonjolí blanco (26).
Al analizar la composición de ácidos grasos de la semilla de mostaza amarilla, el ácido graso predominante es el oleico (7,37%), seguido por erúcico (6,87%) y linoleico (1,87%). El ácido oleico se encuentra en la mayoría de las grasas y aceites naturales, en el caso de la semilla de mostaza negra se encuentra en mayor proporción en comparación con los aceites de semillas de linaza y chía (15,76 y 8,91%, respectivamente) (27). Así mismo este valor de ácido oleico en mostaza negra se encuentra en proporciones semejantes a los valores reportados (28). La cantidad de grasa mono-insaturada se encuentran en mayor proporción en ambas semillas en comparación con las grasas saturadas y poli-insaturadas, predominando, en la mostaza negra las grasas mono-insaturadas (20.57%). El ácido erúcico es característico de las crucíferas (29). Los ácidos linoleico y linolénico son esenciales para el ser humano, a partir de estos ácidos grasos son sintetizados los ácidos araquidónico, eicosapentanoico y docosahexaenoico, los cuáles desempeñan un papel esencial en las interacciones fisiológicas de coordinación entre las células. Las principales fuentes de ácido linolénico incluyen a nueces, semillas y aceites vegetales. Las almendras, chía, nueces y linaza, aportan 0,4, 3,9, 6,8 y 22,8 g/100 g de ácido linolénico, respectivamente; comparando estos porcentajes con los resultados obtenidos para las semillas de mostaza negra (3,43%) y amarilla (2,41%) se puede considerar a la mostaza como una fuente importante de este ácido graso.
Cabe destacar que, en general los aceites de semillas vegetales aportan contenidos importantes de ácido linoleico; sin embargo, son pocos los que aportan ácido linolénico; como es el caso de canola, soya, colza y nuez que aportan 12, 7, 11 y 10 g/100 g de aceite, respectivamente (27). La presencia de ácido linoleico es fundamental, su importancia radica fundamentalmente es que es un precursor de ácidos grados de mayor longitud de cadena (30) entre ellos, el araquidónico, lo que lo caracteriza como un ácido esencial para el metabolismo y su importancia radica en que estos contienen ingredientes nutracéuticos esenciales para el crecimiento y el buen estado de la piel y el pelo así como el ácido linoleico participa en la síntesis de prostaglandinas, en la generación de membrana, y en otros procesos biológicos relacionados con la regeneración celular (30).
La cantidad del ácido linolénico presente en los aceites de mostaza amarilla (21,64%) y negra (10,83%) es alta en comparación con los aceites comunes tales como girasol (0,3%), maíz (2%), soya (4,5-11%) y palma (0,2%) (17). Cabe destacar que en el aceite de mostaza amarilla se observa la mayor concentración de ácido linolénico (21,64%). Estos datos muestran que a partir del aceite se obtendrían los beneficios de los ácidos grasos poli-insaturados (linolénico y linoleico).
Este estudio reveló que las propiedades físicas (densidad, color e índice de refracción) son diferentes para las dos especies de semilla de mostaza (negra y amarilla). Estas semillas, además de ser una fuente potencial de antioxidantes muestran que de acuerdo a su composición químico proximal se caracterizan por un alto contenido de grasa (23,9 a 29,6 g /100 g) y proteína (20,44 a 25,39 g/100g), el contenido de ácido erúcico se encuentra en mayor porcentaje en la mostaza amarilla. Existen diferencias en el contenido de antioxidantes de los diferentes productos de los dos tipos de mostaza estudiadas, tanto en las semillas (1.273,57 a 1.323,22 mg de Trolox /100 g) como en los residuos (1.130,24 a 1.366,88 mg de Trolox /100 g) y aceites (25,88 a 32,27 mg de Trolox /100 g). Este estudio proporciona información sobre la importante actividad antioxidante que exhibe esta especia, tanto como semilla o como pasta residual libre de aceite, así como el contenido detallado de los ácidos grasos contenidos en el aceite y las semillas, lo que permitirá a la industria alimentaria examinar otros usos potenciales basados en las propiedades que presentan estas semillas o sus productos.
Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (CONACyT) de México por el apoyo financiero para el proyecto. B. Mejía-Garibay agradece el apoyo para la realización de sus estudios de doctorado al CONACyT y a la Universidad de las Américas Puebla, México.
Recibido: 19-11-2014
Aceptado: 13-03-2015