Introducción
Physalis peruviana Linnaeus, conocida comúnmente como uchuva en Colombia, es una baya jugosa que se consume en fresco (ensaladas y cocteles de fruta), sometida a cocción para la preparación de mermeladas, salsas, pies, pudines y helados; o procesadas para enlatarlas, deshidratarlas o cubiertas de chocolate (1).
En la composición química de la baya se reconoce principalmente el contenido de minerales, vitamina C (46 mg / 100 g), y vitaminas del complejo B; whitanólidos (esteroide unido a una lactona), flavonoides, polifenoles, carotenoides y ácidos grasos esenciales (2,3). La uchuva contiene 15% de sólidos solubles (principalmente azúcares), un alto nivel de fructosa (29 g / 100 g), sacarosa (35 g / 100 g), aporte de fósforo considerablemente importante para una fruta (55,3 mg / 100 g) y de fibra, principalmente por la pectina, que es reconocida como un regulador intestinal y por su propiedad gelificante, ampliamente utilizada en la industria alimentaria para la producción de jaleas y mermeladas (3).
Entre los compuestos fenólicos se ha encontrado quercetina, miricetina y kaempferol. En un extracto acuoso tal como se reporta en la literatura (4), encontraron 487,1 mg catequina / 100 g peso seco flavonoides totales y un bajo contenido de carotenoides (0,92 mg β-caroteno / 100 g peso seco). De otra parte, aceite extraído de la fruta, contiene los ácidos grasos linoleico (70,5%), oleico (13%), palmítico, γ-linolénico (GLA), los fitosteroles (ST) avenasterol Δ5- y campesterol, γ- , α-tocoferoles y β-caroteno (2,3). La cantidad de Beta-caroteno y vitamina k es mayor en el aceite de la pulpa con cáscara, seguido de la baya entera y por último de las semillas (Carotenos: 0,32%, 0,22% y 0,13% respectivamente). Estos compuestos tienen una gran importancia biológica, estudios epidemiológicos han asociado el consumo de frutas ricas en carotenoides con un menor riesgo de desarrollar enfermedades crónico-degenerativas, además la industria de alimentos los utiliza como fuente de pigmentos para dar color a ciertos productos como sustituyentes de colorantes sintéticos. Por otro lado el aporte de vitamina K, especialmente de filoquinona puede tener un efecto protector frente a enfermedad cardiovascular, actividad anticancerígena, en la salud de la piel y propiedad antioxidante (3).
Con relación a la actividad antioxidante se ha descrito para el jugo mediante el ensayo del radical DPPH (1,1-difenil-2-picrilhidrazil) su capacidad de inhibir el 78% de la formación de DPPH, actividad antioxidante que alcanzó 82% luego de un tratamiento enzimático del jugo se aumentó el contenido de compuestos fenólicos en el jugo (3). A partir de un extracto acuoso de pulpa de uchuva se reportó su valor ORAC (6795,1 μg / mL Trolox / 100 g peso seco), capacidad atrapadora de especies reactivas de oxígeno (ERO) y nitrógeno (ERN) (4229,71 μg / ml Trolox / 100 g peso seco) y capacidad atrapadora de grupos hidroxilo (40803,9 μg/ml DMSO / 100g) (4). Recientemente, Valdenegro et al (5) midieron la actividad antioxidante como equivalentes de trolox (TEAC) en la fruta en estado de madurez intermedia (amarilla) y madura (naranja), donde se observó que en el proceso de maduración así como en el contenido de ácido ascórbico y fenoles totales. Sin embargo, después de cosechada la fruta madura, su valor TEAC se redujo durante el período de vida útil a 20°C a medida que aumenta la producción de etileno, efecto que se revierte cuando se empleó el inhibidor de la producción de etileno (1-metilciclopropano).
Paralelo con el estudio de las propiedades nutracéuticas de la fruta, se ha incrementado su importancia económica para Colombia, el mayor productor y exportador de uchuva en el mundo (1). Para el año 2005, el 97% de las exportaciones de uchuva se dirigían a 29 países de Europa y el resto para Estados Unidos, aunque se espera aumente para éste último gracias a la aprobación en 2014 de la importación de uchuva Colombiana sin tratamiento de frío, situación que implica ahorro de recursos y tiempo (6). Por lo tanto, el objetivo de este trabajo fue describir los cambios en la composición nutricional, contenido de fenoles, flavonoides y carotenoides totales, actividad antioxidante por DPPH y FRAP, en tres estados de la maduración de uchuva. Estos resultados serán de utilidad para un adecuado almacenamiento y preservación de la calidad de la fruta; y para conocer su potencial nutracéutico.
Materiales y métodos
Material vegetal
Se utilizaron frutos de uchuva enteros cosechados en el municipio del Retiro (Antioquia, Colombia), vereda La Amapola (16°C, altitud 2.175 msnm). Se seleccionaron frutos sanos y se clasificaron por inspección visual en los estado 1 (verde claro), estado 3 (fruto anaranjado con visos verdes hacia la zona del cáliz), estado 5 (anaranjado) según la Norma Técnica Colombiana (NTC) 4580 (7). Estos fueron lavados, desinfectados (hipoclorito 100 ppm), se elaboró pulpa con toda la fruta de cada estadio, se almacenó en bolsas plásticas herméticas que se mantuvieron a -20°C, y posteriormente deshidratas por liofilización en un Labconco Freezome (Fisher Scientific, 2-5 Plus System, Pittsburg). Se evaluó su calidad microbiológica mediante conteo total de bacterias Mesofílicas aerobias, hongos y levaduras, cuenta de Coliformes totales y fecales, Escherichia coli según NTC 4458 de 1998 (8); y Salmonella sp, para evaluar Salmonella según NTC 4574 (9); y no se obtuvo crecimiento microbiano en el producto final. Luego se prepararon extractos hidrofílicos y lipofílicos a partir del liofilizado de la fruta para cada estadio de maduración. Para el extracto hidrofílico se empleó el método de Palafox et al (2012) con modificaciones (10). Brevemente, se adicionó 0,5 g de cada muestra en 10 mL del solvente de extracción (metanol, 80%: ácido fórmico, 1%: agua, 19%), se homogenizaron (1 min), sonicaron (5 min) y centrifugaron (10500 rpm, 15 min, 5 ºC). Posteriormente se transfirió el sobrenadante, y se hizo re-extracción del sedimento de la misma manera. Para obtener los extractos lipofílicos se prepararon según Corral-Aguayo et al (2008) (11) y Rivera-Pastrana et al (2010) (12). El solvente de extracción utilizado fue la mezcla hexano / acetona / tolueno / etanol (10:7:7:6), se adicionó 10 mL a 0,5 g de cada muestra, se homogenizó y centrifugó (10500 rpm, 15 min, 5 ºC). Se re-extrajo el sedimento de la misma manera. Posteriormente se saponificó con KOH metanólico por 1 h a 50 ºC en agitación (100 rpm).
Composición de análisis proximal
Se realizó a partir de la pulpa de uchuva entera para cada estado de maduración, cuantificación de humedad (pérdida por secado) según método 1,14 agua (humedad), cenizas o minerales totales por método AOAC 923,03, grasa total mediante procedimiento GTC 6,1 grasa bruta (extracto etéreo), proteína total (N x 6,25) según método microkjeldhal y finalmente cálculo de carbohidratos y calorías totales a partir de componentes (13).
Determinación de fenoles totales
Se usó el método colorimétrico de Prior et al (2005), utilizando el reactivo de Folin-Ciocalteau (14), el cual mide la reducción de este reactivo, inducida por el poder reductor de los compuestos fenólicos, con la consecuente formación de un complejo azul que se lee a 630 nm en un espectrofotómetro (Thermo Scientific, Genesys 20, USA). A una muestra del liofilizado de uchuva en cada estadio de maduración (1 g) se le adicionó agua destilada (2 mL), 150 μL reactivo de Folin-Ciocalteu y 120 μL de una solución de bicarbonato de sodio (NaCO3) 7,1%, se incubaron por 2 h a temperatura ambiente en oscuridad. Se construyó una curva patrón usando como estándar ácido gálico. Los resultados se expresaron como mg de ácido gálico / 100 g de pulpa seca.
Determinación de flavonoides
Se midieron por colorimetría con cloruro de aluminio y nitrato de aluminio. La absorbancia se leyó a 510 nm (15). A 1 g de liofilizado de uchuva de cada estadio de maduración se le adicionó agua destilada, solución de nitrato de sodio al 5% (v/v). La mezcla se incubó por 5 min, posteriormente, se incorporó solución de cloruro de aluminio 10% (v/v) a la mezcla anterior. El contenido de flavonoides se expresó como mg catequina / 100 g pulpa seca.
Determinación de carotenoides totales
Las extracciones de carotenos y carotenoides totales se realizaron utilizando el método 970.64 (13) con algunas modificaciones (16). Las muestras de 0,5 g de liofilizado se mezclaron con 10 mL de hexano /acetona /tolueno /etanol (10: 7: 7: 6, v / v / v / v), se agitó a 56 ° C durante 20 min, se enfrío con agua corriente, y se añadió 10 mL de 10% Na2SO4, se agitó y se incubó en oscuridad hasta la separación de fases (aproximadamente 10 min). La fase superior se separó y se utilizó para la cuantificación de los carotenoides totales en espectrofotómetro a 450 nm (Beckman Coulter, DU-650, California). La concentración de carotenoides se determinó por curva de calibración utilizando β-Caroteno como sustancia patrón. Los resultados se expresaron como mg β-Caroteno / 100 g pulpa seca.
Ensayo DPPH (1,1-difenil-2-picril-hidrazilo)
Mide la capacidad de la muestra para neutralizar el radical DPPH por transferencia de hidrógeno (17). Brevemente, se tomaron 280 μL de solución metanólica de DPPH más 20 μL del extracto hidrofílico de la fruta para cada estadio, la mezcla se incubó por 30 min a temperatura ambiente en oscuridad y se leyó la absorbancia a 490 nm en un lector de microplacas (Dynex Technology, MRX microplate reader, Chantilly). Los resultados se reportaron como valores μmol equivalentes de Trolox / 100 g pulpa seca (dw).
Ensayo FRAP (2,2-diphenylpicrylhydrazyl)
Mide capacidad reductora de una muestra mediante el aumento de la absorbancia por la formación del complejo 2,4,6-tri(2-piridil)-s-triazina (TPTZ) a su forma ferrosa (Fe+2). (18) Para ello se tomó 280 μL del reactivo de trabajo (buffer acetato / TPTZ / cloruro férrico, proporción 5:0,5:0,5) más 20 μL del extracto hidrofílico de uchuva de cada estadio de maduración. La mezcla se incubó por 30 min a temperatura ambiente en oscuridad y se leyó la absorbancia a 630 nm en un lector de microplacas (Dynex Technology, MRX microplate reader, Chantilly). Los resultados se reportaron como equivalentes Trolox (TE) en μmol / 100 g dw.
Identificación de compuestos de los extractos de uchuva
Se emplearon los extractos hidrofílicos y lipofílicos de cada estadio de maduración. Del volumen final de cada extracto se tomó aproximadamente 1mL para ser filtrado con membrana de nylon de 0,22 μm para los extractos hidrofílicos y de PTFE 0,22 μm para los extractos lipofílicos. Las muestras filtradas fueron inyectadas automáticamente en un cromatógrafo, sistema HPLC (Hewlett–Packard, HP 1100, Palo Alto) equipado con un detector de arreglo de diodos (DAD). Para los compuestos hidrofílicos, el sistema HPLC fue equipado con una columna de fase reversa Xterra RP18 (4,6 mm; 250mm) con un tamaño de partícula de 5 μm. La fase móvil estaba compuesta de 1% de ácido fórmico (A) y acetonitrilo (B), y el gradiente de elución fue 2-100% (B) en 70 min. El flujo fue de 0,25 mL/ min. Los espectros de absorción de los principales picos fueron registrados a 280 y 320 nm. Para los compuestos lipofílicos, se empleó la columna de fase reversa C30 (4,6 mm; 150 mm, 3 μm) (YMC Inc., Milford, MA), la fase móvil estaba compuesta por metanol (A) y tert-butyl-methyl éter (MTBE) (B), y el gradiente de elución fue 2 a 100% (B) en 55 min. El volumen inyectado fue 100 μL, el espectro de absorción fue registrado a 450nm.
Análisis estadístico
Los resultados se analizaron con el programa Graph Pad Prism versión 6, los datos se expresaron como promedio ± error estándar de la media (ESM). Las diferencias estadísticas se evaluaron analizaron con ANOVA de una vía y post-test de comparaciones múltiples Tukey con base a un nivel de significancia de p < 0,05%. Para la correlación de la actividad antioxidante pro DPPH y FRAP con el contenido de fenoles y flavonoides totales en el extracto hidrofílicos se usó el coeficiente de correlación de Pearson.
Resultados
Análisis de composición proximal
La Tabla 1 corresponde al contenido de humedad, cenizas, macronutrientes y energía para la uchuva estado 1 (verde claro), estado 3 (fruto anaranjado con visos verdes hacia la zona del cáliz), estado 5 (anaranjado), cuyos valores muestran que es una fruta con alto porcentaje de humedad en los tres estados. El contenido de carbohidratos fue similar en los tres estados de maduración, siendo mayor en la uchuva verde y madura respecto al fruto en estado 3, siendo esto coherente con el aporte calórico. El porcentaje de grasas y proteínas fue menor a 3 para todos los estados, y en relación al contenido de cenizas, fue más mayor en uchuva pintona.
TABLA 1. Análisis de composición proximal de la uchuva en tres estadios de maduración (g / 100 g).
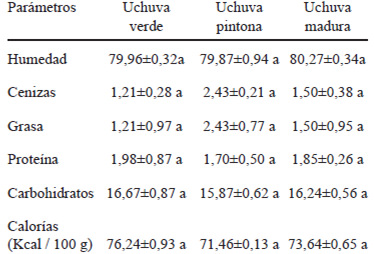
Promedio + error estándar de la media, n=3. Los valores dentro de cada tipo de variable que comparten la misma letra no son significativamente diferentes, P<0,05.
Contenido de fenoles totales, flavonoides y carotenoides
En la Tabla 2 se presenta el contenido de metabolitos secundarios, el cual varió para cada estado de maduración analizado. Para fenoles totales la cantidad promedio fue diferente significativamente entre los tres estados de maduración, siendo mayor en la uchuva verde. Mientras que el contenido de los flavonoides disminuyó con el progreso maduración pero no hubo diferencias estadísticamente significativas. El contenido de carotenoides totales fue diferente significativamente entre los tres estados de maduración, siendo mayor en la uchuva en estado de maduración 3.
TABLA 2. Contenido de fenoles, flavonoides y carotenoides totales de la uchuva en tres estadios de maduración.
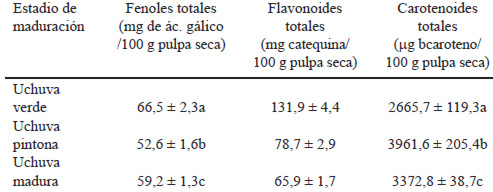
Promedio + error estándar de la media, (n=9). Los valores dentro de cada tipo de prueba antioxidante que no comparten la misma letra, son diferentes: a≠b, P<0,05.
Capacidad antioxidante de la uchuva verde, pintona y madura
En la Tabla 3 se muestra los resultados de la capacidad antioxidante determinada por el método DPPH y el método FRAP en los tres estados de maduración evaluados. Se encontró que la actividad antioxidante DPPH aumentó con el progreso de la maduración del fruto, siendo significativamente mayor en el estado maduro con respecto a la uchuva estado 1 (verde) y estado 3 (anaranjada con visos verdes hacia el cáliz). Por otra parte, la capacidad reductora FRAP no presentó diferencia significativa (p<0,05).
TABLA 3. Capacidad antioxidante por los métodos DPPH y FRAP de la pulpa de uchuva en tres estadios de maduración.

Promedio + error estándar de la media, (n=9). Los valores dentro de cada tipo de prueba antioxidante que no comparten la misma letra, son diferentes: a≠b, P<0,05.
Los resultados de la correlación para cada método de acuerdo al contenido de fenoles y flavonoides se encuentran expresados en la Tabla 4. La correlación entre el contenido de fenoles totales y los parámetros de actividad antioxidante DPPH (0,44) y FRAP (0,25) fue directamente proporcional; sin embargo hubo diferencia estadísticamente significativa entre la correlación de fenoles totales con el valor DPPH (R2 = 0, 19, p < 0,05). Mientras que la correlación del contenido de flavonoides totales fue inversamente proporcional para los parámetros antioxidantes evaluados, siendo significativa la correlación entre flavonoides totales con el parámetro FRAP (R2 = 0,17, p < 0,05).
TABLA 4. Correlación de Pearson para los métodos DPPH y FRAP con relación al contenido de fenoles y flavonoides totales.
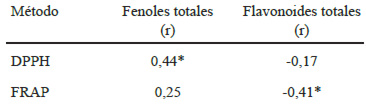
*Estadísticamente significativo P < 0.05, n= 27.
Identificación de metabolitos de la uchuva verde, pintona y madura
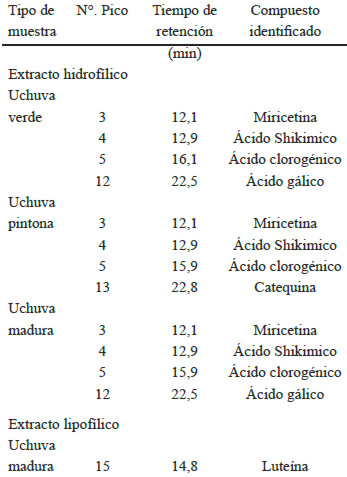
A partir de 25 picos presentes en los cromatogramas obtenidos a partir de los extractos hidrofílicos de uchuva en cada estado de maduración aquí evaluados, se identificaron seis picos como miricetina (pico 3), ácido shikímico (pico 4), ácido clorogénico (pico 5), ácido gálico (pico 12) y catequina (pico 13) cuando fueron comparados con estándares, la coincidencia fue mayor a 95% (Figuras 1 y 2). Mientras que en el extracto lipofílico de uchuva madura solo se logró identificar luteína (pico 14) con un espectro que coincidió en 99,57% con el estándar. Los picos identificados y tiempos de retención se resumen en la Tabla 5.
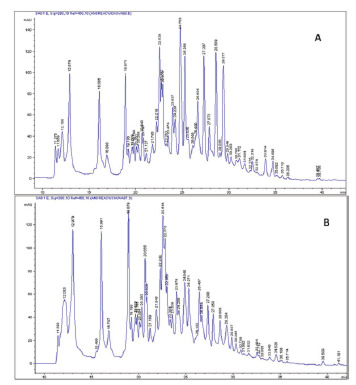
FIGURA 1. Cromatogramas HPLC de extracto hidrofílico de uchuva estado 1 (verde claro) (A) y estado 3 (fruto anaranjado con visos verdes hacia el cáliz) (B).
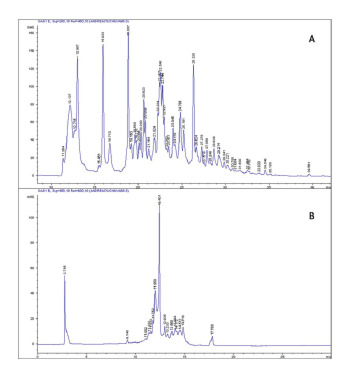
FIGURA 2. Cromatogramas HPLC del extracto hidrofílico (A) y lipofílico (B) de uchuva estado 6 (anaranjada madura).
TABLA 5. Compuestos identificados en extracto hidrofílico y lipofílico de uchuva verde, pintona y madura.
Discusión
En el presente estudio se reporta por primera vez el contenido de macronutrientes, la capacidad antioxidante, el contenido de flavonoides y carotenoides totales de la uchuva en tres estados de maduración diferentes, verde, anaranjada con visos verdes hacia el cáliz (fruta que no ha alcanzado la madurez) y madura. Dentro de los compuestos bioactivos de la uchuva se ha reportado el contenido de fenoles y carotenoides, metabolitos que epidemiológicamente se han asociado con propiedades antioxidantes y con la prevención de varias enfermedades crónico-degenerativas (3).
En este estudio las cantidades de fenoles reportados para los tres estados de maduración fueron mayores a las referidas para uchuva madura por Restrepo (40,45 mg ácido gálico/100 g fruta) (19) y Botero (39,15 mg de ácido gálico / 100 g fruta) (20). Aunque el contenido de los compuestos fenólicos de la uchuva analizada aquí disminuyó con el progreso de la maduración, tendencia también reportada por Valdenegro et al (5) con la misma fruta en dos estados de maduración (amarillo y naranja) pero almacenadas a 20°C, mismo estudio en el que se atribuyó la disminución del contenido de compuestos fenólicos a la acción del etileno, cuya reacción podía ser inhibida por el MCP-1 (1-metilciclopropeno).
En cuanto a los flavonoides, aunque no hubo diferencias estadísticamente significativas para el contenido en los tres estados de maduración, los valores si mostraron una tendencia a la disminución con la progresión de la maduración de la baya, comportamiento posiblemente asociado a cambios propios del metabolismo de estos, los cuales pueden desencadenarse a partir de múltiples reacciones enzimáticas a las que son altamente susceptibles los compuestos fenólicos y que pueden dar paso a ciertas características sensoriales relacionadas con el color, olor, amargor y astringencia de la fruta (21).
Respecto a los carotenoides se encontraron cambios significativamente diferentes entre los tres estados de maduración de la uchuva, con un aumento en la uchuva en estado 3 de maduración, el cual podría ser atribuido al aumento en pigmentos carotenoides de la clase de las Xantófilas (21) como la luteína, pigmento amarillo encontrado aquí en el extracto lipofílico de la fruta. Por otra parte, en el estado maduro el tipo de carotenoide que puede estar presente es el Beta-caroteno que confiere el color naranja característico del estado maduro de la baya, como lo indicó De Rosso y Mercadante (22), quienes reportaron que en uchuva madura el principal carotenoide fue todotrans-beta-caroteno, correspondiente al 76,8% de los carotenoides totales, seguido de 9-cis-β-caroteno y todo-trans-α-criptoxantina, contribuyendo alrededor de 3,6 y 3,4%. Debido a que en nuestro estudio, la baya madura utilizada corresponde a la clasificación cinco de acuerdo a la NTC-4580 (7), definida como baya madura de color anaranjado, mientras que la clasificación seis corresponde al fruto de color anaranjado intenso, donde podría encontrarse el mayor contenido de β-caroteno.
De otra parte, considerando que la uchuva es una fruta no climáterica, es decir, una vez cosechada no continua su proceso de maduración, si se quisiera obtener una fruta con alto contenido en compuestos fenólicos y flavonoides se debería recolectar fruta verde (estado 1). Sin embargo, al momento de la cosecha debe tenerse en cuenta los requerimientos del cliente (mercado o consumidor), siendo la fruta en estado maduro 5 (anaranjado) ó 6 (anaranjado intenso) más agradable para el consumidor, pero con menor contenido de compuestos fenólicos y flavonoides, aunque con un alto contenido de compuestos carotenoides y mayor actividad antioxidante con respecto a los estados 1 y 3. Los carotenoides protegen contra la peroxidación de lípidos neutralizando radicales libres, sobre todo el oxígeno atómico.
Los compuestos fenólicos y la actividad antioxidante de la uchuva han tomado importancia, puesto que estos influencian en gran medida las propiedades nutracéuticas que se le atribuyen a la fruta. Algunos autores como Restrepo (19) y Botero (20) han reportado valores de la capacidad antioxidante de los frutos de P. peruviana L. en función del método DPPH (210,82 y 192,51 μmol Trolox/100 g fruta respectivamente), la concentración de fenoles totales y el ensayo FRAP (56,53 y 54,98 mg de ácido ascórbico / 100 g de fruta). Para nuestro estudio, particularmente la capacidad antioxidante medida por DPPH y FRAP mostró un comportamiento similar al observado por Valdenegro et al (5), quienes también reportaron un aumento de la capacidad antioxidante contra el radical anión 2,2-azino-bis (3-etilbenzotiazolina-6-sulfónico) conforme progresó la maduración de la uchuva.
Con respecto al contenido de fenoles totales y el método DPPH, estos mostraron una correlación positiva y significativa. A partir de su coeficiente de correlación (R2) se puede inferir que la capacidad de la uchuva para neutralizar el radical DPPH por transferencia de hidrógeno se debe en un 19% al contenido de compuestos fenólicos de la fruta. De otra parte, la correlación entre el contenido de flavonoides totales de la uchuva y la capacidad para reducir el hierro férrico (Fe+3) hasta la forma ferrosa (Fe+2), fue inversamente significativa, lo que sugiere que esta propiedad antioxidante de la uchuva se atribuye a otros compuestos presentes en la fruta distintos a los flavonoides, como lo es ácido ascórbico, cuyo niveles parecen aumentar con la maduración de la baya y también pueden verse afectados en condiciones de almacenamiento a 20° C (5).
El aumento significativo en la capacidad antioxidante determinada por DPPH entre las frutas verde con respecto a la madura puede indicar que se potencia el sistema antioxidante de la células de la fruta madura para atrapar radicales libres. Se ha encontrado que las especies reactivas de oxígeno (ERO) parecen ser una característica intrínseca de las etapas de senescencia y de maduración de las frutas, lo cual podría promover el deterioro oxidativo, que a su vez contribuye a un deterioro general del metabolismo celular, en donde pueden actuar los sistemas antioxidantes propios de las células para prevenir el estrés oxidativo en las células de la fruta (23). En otras palabras, se mejora el mecanismo de defensa antioxidante de la baya cuando madura.
El estudio de la composición mediante HPLC de los extractos hidrofílicos de la fruta en tres estadios de su maduración, permitió identificar dos flavonoides (miricetina y catequinas), dos compuestos fenólicos (ácido gálico y ácido clorogénico) y su molécula precursora, el ácido shikímico cuya transformación es dependiente de la fotosíntesis y ocurre en los plastos. Esos compuestos suelen acumularse en las capas más superficiales de los vegetales y captan hasta el 90% de las radiaciones UV, impidiendo los efectos nocivos de estas radiaciones en los tejidos internos de la fruta. También, confieren aromas y coloraciones atrayentes de insectos, con lo que se favorece el proceso de polinización y hacen apetecible el fruto para los herbívoros, con lo que se favorece la dispersión de semillas con las heces (2,3).
Finalmente, el aporte del presente estudio pretende respaldar científica y tecnológicamente a la cadena productiva de esta fruta que posee un importante y creciente mercado internacional. No ha sido suficiente con la entrega de un producto con base a su aspecto, tamaño, peso, color y sabor. Por tanto, el conocimiento sobre su composición nutricional y compuestos bioactivos, debe ser tomado en cuenta para un adecuado manejo de la fruta durante su etapa postcosecha, de manera que no solo se incremente la vida útil de la misma, sino también se aproveche el contenido nutricional, compuestos bioactivos y capacidad antioxidante de la fruta, se transfiera mayor valor agregado y se ofrezca un producto de excelente calidad, que le permita un mayor mercado internacional.
Conclusiones
Los hallazgos aquí presentados sobre la uchuva nos muestran que durante el proceso de maduración se conserva un alto porcentaje de humedad, carbohidratos y aporte calórico en los tres estados de maduración, contrario al contenido de grasas y proteínas; se afectan negativamente el contenido de compuestos fenólicos y flavonoides, aumenta el contenido de carotenoides totales así como la capacidad antioxidante entre el estado verde y el maduro; información que será de gran utilidad para lograr un adecuado almacenamiento y preservación la calidad de la fruta; así como aporte para conocer el potencial nutracéutico de la uchuva.
Agradecimientos
Este trabajo fue financiado por la Estrategia de Sostenibilidad 2014-2015 de la Universidad de Antioquia. Agradecemos a COLCIENCIAS por la beca otorgada a la estudiante de doctorado.
Referencias
- Fisher G. Crecimiento y desarrollo. En: Producción, poscosecha y exportación de la uchuva (Physalis peruviana L.). Flórez RV, Fisher G, Sora RA, Editores. 2000, Universidad Nacional de Colombia: Colombia. p. 9-26.
- Zhang YJ, Deng FG, Xu RX, Wu S, Li S, Li HB. Chemical Components and Bioactivities of Cape Gooseberry (Physalis peruviana). IJFNS 2013, 3: 15-24.
- Ramadan MF. Bioactive phytochemicals, nutritional value, and functional properties of cape gooseberry (Physalis peruviana): An overview. Food Res Int 2011: 44, 1830–1836.
- Areiza-Mazo N, Maldonado ME, Rojano B. Extracto acuoso de uchuva (Physalis peruviana): actividades antiproliferativa, apoptótica y antioxidante. Perspect Nutr Humana 2013, 15: 41-55.
- Valdenegro M, Fuentes L, Herrera R, Moya M. Changes in antioxidant capacity during development and ripening of goldenberry (Physalis peruviana L.) fruit and in response to 1-methylcyclopropene treatment. Postharvest Biol Tec 2012, 67: 110-117.
- Procolombia. Estados Unidos aprobó la importación de uchuva colombiana sin tratamiento de frío. [Cited 2015 Enero 25]. Available from: http://www.procolombia.co/noticias/estados-unidos-aprobo-la-importacion-deuchuva-colombiana-sin-tratamiento-de-frio.
- Instituto Colombiano de Normas Técnicas y Certificación ICONTEC. Norma Técnica Colombiana 4580: Frutas frescas Uchuva Especificaciones. 1999, Incontec: Colombia. p. 14.
- Instituto Colombiano de Normas Técnicas y Certificación ICONTEC. Norma técnica Colombiana 4458. Microbiología de alimentos y de alimentos para animales. Método horizontal para el recuento de coliformes o Escherichia coli o ambos. Técnica de recuento de colonias utilizando medios fluorogénicos o cromogénico. 2007. Icontec: Colombia. p.15.
- Instituto Colombiano de Normas Técnicas y Certificación ICONTEC. Norma técnica Colombiana 4574 Microbiología de alimentos y alimentos para animales método horizontal para la detección de Salmonella spp. 2007. Icontec: Colombia. p.27.
- Palafox-Carlos P, Yahia EM, González-Aguilar G. Identification and quantification of major phenolic compounds from mango (Mangifera indica, cv. Ataulfo) fruit by HPLC–DAD–MS/MS-ESI and their individual contribution to the antioxidant activity during ripening. Food Chem 2012, 135: 105–111.
- Corral-Aguayo RD, Yahia EM, Carrillo-Lopez A., González-Aguilar G. Correlation between Some Nutritional Components and the Total Antioxidant Capacity Measured with Six Different Assays in Eight Horticultural Crops. J Agric Food Chem 2008, 56: 22: 10498-10504.
- Rivera-Pastrana DM., Yahia EM., González-Aguilar GA. Phenolic and carotenoid profiles of papaya fruit (Carica papaya L.) and their contents under low temperature storage. J Sci Food Agric 2010; 90: 2358–2365.
- Association of Official Agricultural Chemists. Official Methods of Analysis of the AOAC. 12th ed. 1975. The Association: Washington D.C.
- Prior RL, Wu XL, Schaich K. Standardized methods for the determination of antioxidant capacity and phenolics in foods and dietary supplements. J Agric Food Chem 2005, 53: 4290–4302.
- Debnath T, Park P-J, Debnath NC, Samad NB, Park HW, Lim BO. Antioxidant activity of Gardenia jasminoides Ellis fruit extracts. Food Chem 2011, 128: 697-703.
- Soto-Zamora G, Yahia EM, Brecht JK, Gardea A. Effects of postharvest hot air treatments on the quality and antioxidant levels in tomato fruit. Lebensm-Wiss Technol 2005, 38: 657–663.
- Rojano B, Gaviria C, Gil M, Saez J, Schinella G, Tournier H. Actividad antioxidante del isoespintanol en diferentes medios. Vitae 2008, 15: 173-181.
- Rojano BA, Zapata-Acosta K, Cortés-Correa FB. Capacidad atrapadora de radicales libres de Passiflora mollissima (Kunth) L. H. Bailey (curuba). Rev Cub Plantas Med 2012, 17: 408-419.
- Restrepo A. Nuevas perspectivas de consumo de frutas: Uchuva (Physalis peruviana L.) y Fresa (Fragaria vesca L.) mínimamente procesadas fortificadas con vitamina E. Facultad de Ciencias Agropecuarias. Tesis de Maestría en Ciencia y tecnología de alimentos, 2008. Universidad Nacional de Colombia: Medellín. p.107.
- Botero A. Aplicación de la Ingeniería de Matrices en el desarrollo da la uchuva mínimamente procesada fortificada con calcio y vitaminas C y E. Facultad de química farmacéutica. Tesis de Maestría en Ciencias Farmacéuticas énfasis en alimentos, 2008. Universidad de Antioquía: Medellín. p.185.
- Rinaldo D, Mbéguié-A-Mbéguié D, Fils-Lycaon B. Advances on polyphenols and their metabolism in sub-tropical and tropical fruits. Trends Food Sci Tech 2010, 21: 599-606.
- De Rosso V, Mercadante AZ. Identification and quantification of carotenoids by HPLC-PDA-MS/MS from Amazonian fruits. J Agric Food Chem 2007, 55: 5062-5072.
- Huang R, Xia R, Hu L, Wang M. Antioxidant activity and oxygen-scavenging system in orange pulp during fruit ripening and maturation. Sci Hort 2007, 113: 166-172.