La fenilcetonuria (PKU) es causada por una actividad deficiente de la enzima fenilalanina hidroxilasa. En los pacientes con esta deficiencia la fenilalanina (Phe) no puede ser convertida en tirosina, aumentando sus niveles en sangre y de otros metabolitos neurotóxicos, provocando un retraso mental irreversible. El tratamiento fundamentalmente se basa en una dieta controlada de Phe. Sin embargo, los alimentos libres o bajos en Phe son escasos. El objetivo de esta investigación es obtener hidrolizados proteicos con bajo contenido de Phe a partir del suero dulce de leche en polvo y harina de E. edulis Triana. El aislado proteico (96,01% proteína cruda) se obtuvo por solubilización y precipitación de las proteínas de la harina, mientras que las proteínas del suero (15,69% proteína cruda) fueron tratadas en su matriz original. Las proteínas del suero y el asilado fueron hidrolizadas enzimáticamente con pepsina y proteasa de Streptomyces griseus. La concentración de Phe se determinó por fluorometría y por HPLC, de lo cual la Phe de las proteínas del suero es liberada una hora antes que las del chachafruto, debido a que las proteínas del suero en parte fueron hidrolizadas en la elaboración del queso. Además, los resultados de la utilización del carbón activados como captor de Phe indican la reducción total del contenido de este aminoácido en los hidrolizados y la reducción de la concentración de otros aminoácidos. ALAN, 2019; 69(1): 25-33.
Palabras clave: Fenilcetonuria; fenilalanina; aislado proteico; hidrolizados proteicos; Erythrina edulis; chachafruto.
Phenylketonuria (PKU) is caused by a low activity of the enzyme phenylalanine hydroxylase. In patients with this deficiency, phenylalanine (Phe) cannot be converted to tyrosine, increasing blood levels and other neurotoxic metabolites, causing irreversible mental retardation. The treatment is fundamentally based on a controlled diet of Phe. However, free or low-Phe foods are scarce. The objective of this research is to obtain protein hydrolysates with low Phe content from sweet milk powder and E. edulis Triana flour. The protein isolate (96.01% crude protein) was obtained by solubilization and precipitation of the flour proteins, while the whey proteins (15.69% crude protein) were treated in their original matrix. Serum and asylated proteins were enzymatically hydrolyzed with pepsin and Streptomyces griseus protease. The concentration of Phe was determined by fluorometry and by HPLC, from which the Phe of whey proteins is released one hour earlier than those of chachafruto, due to the fact that the whey proteins were partially hydrolyzed in the elaboration of the cheese. In addition, the results of the use of charcoal activated as Phe captor indicate the total reduction of the content of this amino acid in the hydrolysates and the reduction of the concentration of other amino acids. ALAN, 2019; 69(1): 25-33.
Key words: Phenylketonuria; phenylalanine; protein isolate; protein hydrolysates; Erythrina edulis; chachafruto.
https://doi.org/10.37527/2019.69.1.004
Autor para la correspondencia: Amaury Pérez Martínez. Email: [email protected]
Las proteínas de la dieta, son fuente de energía, aportan aminoácidos necesarios para el desarrollo y mantenimiento de células y tejidos de nuestro organismo. Como consecuencia de la digestión de las proteínas se liberan péptidos, que se definen como cadenas con distintos números de aminoácidos (1). Sin embargo, en algunas condiciones como en los errores innatos del metabolismo (EIM), la consecuencia de las deficiencias enzimáticas congénitas provoca un bloqueo en determinada vía metabólica, por tanto, el consumo de ciertos aminoácidos puede ocasionar consecuencias patológicas en el individuo.
La fenilcetonuria, o PKU (por su nombre en inglés: Phenylketonuria) es el más frecuente de los errores innatos del metabolismo de los aminoácidos. Es una enfermedad metabólica autosómica recesiva, que se debe a una actividad deficiente o inexistente de la enzima fenilalanina hidroxilasa (PAH por su nombre en inglés: phenylalanine hydroxylase). Este déficit causa una acumulación de fenilalanina (Phe) y un descenso de tirosina (Tyr) en los fluidos y tejidos biológicos, por lo que la PKU que no es diagnosticada ni tratada tempranamente antes del mes de vida, produce una encefalopatía irreversible cuya consecuencia más grave es el retraso (2, 3).
Uno de los tratamientos de la PKU consiste en regular los niveles de Phe, limitando su ingestión. El propósito fundamental del tratamiento es reducir y mantener las concentraciones de Phe en sangre para prevenir la aparición de los efectos neuropatológicos y, al mismo tiempo, asegurar un crecimiento y un neurodesarrollo apropiado de los pacientes.
Las proteínas de origen animal deben restringirse en la dieta de los pacientes con PKU debido a que contienen 4 a 6% de Phe, y con pequeñas cantidades se cubre casi la totalidad diaria recomendada de este aminoácido. Los cereales, leguminosas, frutas y verduras también contienen este aminoácido, pero en cantidades menores, por lo que se pueden incluir en la dieta de forma cuidadosa y siempre calculando el aporte total de Phe (2).
Para limitar la ingesta de Phe y al mismo tiempo proporcionar una buena nutrición, el paciente debe recibir fórmulas especiales libres o bajas en Phe, ricas en otros aminoácidos, vitaminas y minerales. En estas fórmulas sin Phe las proteínas están predigeridas mediante hidrólisis enzimática, tratamiento térmico y ultrafiltración. El sustrato más usado para la preparación de estos hidrolizados proteicos son las proteínas de la leche, es decir, caseína y proteínas del lactosuero. Esto es debido fundamentalmente, a su disponibilidad en grandes cantidades, alto valor nutricional y moderado costo del mismo (4).
Sin embargo, el principal inconveniente de los consumidores afectados por PKU es el acceso a proteínas libres o bajas en el contenido de Phe para mantener la dieta baja en este aminoácido, ya que, en su totalidad, estos productos son importados y de costos elevados.En la búsqueda de fuentes proteicas alternativas se encuentran las proteínas de las leguminosas, que, a pesar de ser deficientes en metionina y cisteína, tienen una calidad nutricional adecuada por su alto contenido de lisina. Entre ellas se menciona el frijol de E. edulis Triana, que posee un alto contenido de proteínas (20,50%). Además de tener un aminograma comparable al del huevo y superior al del fríjol y la arveja (5).
El chachafruto, es una leguminosa multipropósito con un amplio espectro de usos, que van desde la alimentación humana (la semilla) y animal (el forraje) hasta la recuperación de suelos degradados (dada su capacidad de fijar nitrógeno en el suelo), pasando por la formación de cercas vivas y las asociaciones con otras especies (en muchas regiones del país se le usa para dar sombra a los cafetales) (6).
Con el fin de aprovechar materia prima tropical no convencional subutilizada, el propósito del trabajo es obtener hidrolizados proteicos con bajo contenido de fenilalanina a partir del suero dulce de leche en polvo y harina de chachafruto.
La materia prima usada fue suero dulce de leche en polvo de la comercializadora LGA. C.A. Venezuela y E. edulis Triana que se produce y cultiva en el estado Mérida, Venezuela. Las enzimas utilizadas son de Sigma-Aldrich: a) pepsina de la mucosa gástrica porcina P7000-100G; b) proteasa bacteriana Tipo XIV de Streptomyces griseus P5147-1G.
Caracterización proximal del suero de leche. Se realizó según los métodos descritos en las normas COVENIN (7, 8): a) Humedad; b) proteínas; c) grasa d) cenizas; e) carbohidratos-calculo por diferencia.
Preparación y caracterización proximal de la harina de chachafruto. Se elaboró la harina de chachafruto, según el método descrito por Pérez Sira, Lares Amaiz (9). Se cortaron los frijoles en trozos rectangulares (≈ 2 cm de diámetro), y deshidrataron a una temperatura de 45 °C por un periodo de 24 horas, en el deshidratador de bandeja “Mitchell Dryers” modelo N° 655149. Los trozos deshidratados fueron molidos en un molino (de martillo) y la harina obtenida fue envasada en frascos de vidrio.
La caracterización química de la harina de chachafruto se realizó de acuerdo a las normas COVENIN (7,10): a) humedad; b) proteínas; c) grasa; d) cenizas; e) carbohidratos-estimado por diferencia.
Obtención de aislados proteicos de harina de chachafruto por precipitación del punto isoeléctrico. El aislado proteico se obtuvo por extracción alcalina y precipitación en el punto isoeléctrico de la proteína, al modificar el método propuesto por (11).
La harina fue dispersada en agua destilada (1:10 p/v) y el pH ajustado a 11,0 con NaOH 0,1 M, a fin de facilitar la solubilización de la proteína. La dispersión se mantuvo bajo agitación durante 1 hora, al cabo de este tiempo se centrifugó la dispersión a 2.500 rpm durante 20 minutos. El sobrenadante fue separado y ajustado a pH 4 para precipitar la proteína, se agitó por una 1 hora y la proteína se recuperó por centrifugación a 2.500 rpm durante 30 minutos. Las proteínas recuperadas fueron liofilizadas y congeladas para su posterior hidrólisis.
Reducción del nivel de Phe de las proteínas del suero en polvo y del aislado proteico de harina de Erythrina edulis Triana. Para reducir el nivel de fenilalanina se utilizó y modificó la metodología propuesta por Arai, Maeda (12). Se prepararon soluciones acuosas al 5% de proteínas tanto del suero como del aislado de chachafruto y se calentaron a 90°C por 10 minutos, antes del tratamiento enzimático.
El proceso de hidrolisis se realizó en el fermentador ApplikonBiotechnology P100. Para esto la solución anteriormente calentada se enfrió a 37°C, ajustando el pH a 2.0 y añadiendo la pepsina en una proporción 1:100 (enzima:sustrato), manteniendo la temperatura del medio a 37°C por 2 h. Posteriormente se aumentó la temperatura a 40°C y el pH a 6,5 para añadir proteasa en una proporción 1:100 (enzima:sustrato), manteniendo el proceso de hidrólisis por 5 horas.
Finalizada la hidrólisis se inactivaron las enzimas aumentando la temperatura a 90°C. El hidrolizado enfriado se filtró a través de columnas de carbón activado para remover la fenilalanina. Es importante mencionar que durante el proceso de hidrólisis se tomaron muestras cada hora, con el fin de determinar la cantidad de fenilalanina liberada de las proteínas.
Cuantificación del contenido de Phe de los hidrolizados proteicos de suero y de chachafruto por fluorometría. El contenido de Phe se cuantifico utilizando el método Fluorometría desarrollado por Centro de Inmunoensayo (13). Este método consistente en impregnar papeles de filtro calibrado con los hidrolizados, que se secaron bajo campana. Una vez seco el papel de filtro de cada hidrolizado, se cortó un disco de 3 mm de diámetro y se depositó en una placa para su elusión, añadiendo 70 μL de etanol al 70% y se incubó durante 30 minutos a temperatura ambiente. Luego se transfirió 10 μl de los calibradores, el control y las muestras a las tiras de reacción, con una pipeta multicanal y se añade 10 μL de la mezcla de reacción (mezcla de Ninidrina, L-leucina-L-Alanina en una solución tampón de succinato) en cada orificio y se incubaron 1 hora a 62 °C en cámara húmeda.
Transcurrido este tiempo se añadió 10 μl del reactivo de cobre en cada pocillo y se incubó 10 minutos a temperatura ambiente, la intensidad de la fluorescencia emitida en la placa se leyó en un fluorómetro PR-521 marca SUMA a una longitud de inda de 460 nm. Los valores de fluorescencia de las muestras se interpolaron en un gráfico de fluorescencia contra la concentración de Phe correspondiente a la curva de calibración, obteniéndose los resultados en μmol/L o mg/dL.
Obtención del perfil de aminoácidos del suero dulce de leche, aislado proteico de harina de chachafruto y sus respectivos hidrolizados. El perfil aminoacídico de los hidrolizados proteicos se realizó según el método descrito por Waters Associates (14), como se detalla a continuación:
La preparación de la muestra se realizó con 40 mg de proteína que fueron hidrolizadas a 110 °C durante 24 horas con 15 mL de HCl 6 M. Luego se aforó a 50 mL y una alícuota de 1 mL fue filtrada a través de un filtro Millipore. Los hidrolizados fueron derivatizados usando fenilisotiocianato (PITC por su nombre en inglés: phenylthiocarbamyl).
Posteriormente se determinaron los perfil de aminoácidos en el HPLC de bomba binaria Waters 1525, acoplado a un detector de UV-Visible de onda dual Waters 2487 empleando a una longitud de onda de 254 nm, con una columna de C18 de 150 x 3,9 mm (V0= 1,8 cm3). Se inyectaron las muestras usando una jeringa Hamilton de 50 μL, el loop de la válvula de inyección debe fue de 5 μL. Las fases móviles usadas fueron, A: constituida por un buffer de acetato a pH 5,70; B: constituida por una mezcla CH3CN – H2O (60-40) a un flujo de 1,0 mL/min. Cada corrida cromatográfica se llevó a cabo en un lapso de 45 minutos a una temperatura de 40 °C (14).
Los resultados se presentan como el promedio de tres determinaciones ± desviación estándar. La comparación de los perfiles de aminoácidos del suero dulce de leche, aislado proteico de harina de chachafruto y con los respectivos hidrolizados fueron analizados con la prueba t de Student para determinar diferencias significativas en el contenido de aminoácidos.
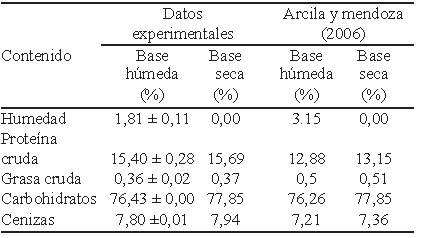
Composición del suero de leche en polvo. En la Tabla 1, se presentan los resultados obtenidos de humedad, proteína cruda, grasa cruda y carbohidratos del suero dulce de leche en base seca y base húmeda, donde el mayor contenido corresponde a carbohidratos.
Preparación y caracterización de la harina de harina de chachafruto. El rendimiento del proceso de obtención de la harina del chachafruto fue de 18,85%. Este valor es bajo y se debe al alto contenido de humedad en el grano fresco (81,5%).
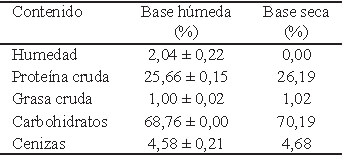
En la Tabla 2 se reporta la cantidad porcentual de humedad, proteína cruda, grasa cruda, y carbohidratos de la harina de chachafruto, donde se observa un predomino de carbohidratos y proteínas.
Obtención del aislado proteico de harina de chachafruto por precipitación del punto isoeléctrico. La disponibilidad en grandes cantidades de fuentes proteicas vegetales, su menor costo comparado con la proteína de origen animal y la tendencia a reducir la ingesta de proteínas animales por razones de salud hace que en los últimos años se esté produciendo un gran desarrollo en los procesos de extracción y mejora de estas proteínas vegetales para su uso en alimentación humana. En la Tabla 3 se presenta el valor de la concentración del contenido de proteína aislada de la harina de chachafruto. Este valor es elevado al observar los datos en base seca y base húmeda.

Reducción y cuantificación del nivel de Phe de las proteínas del suero y aislado de chachafruto tratadas enzimáticamente. Para reducir el contenido de Phe de las muestras de suero y aislado proteico de harina de chachafruto se requiere hacer una ruptura de las proteínas mediante hidrólisis enzimática, para exponer los aminoácidos y facilitar su remoción. Considerando que la hidrólisis se realizó en dos etapas: a) 2 horas con pepsina de mucosa gástrica de porcino; b) 5 horas con proteasa bacteriana de S. griseus.
Los resultados se muestran en las Figura 1 (a) y (b). El tratamiento de 2 horas con la pepsina no tiene efecto relevante en la ruptura de las proteínas o generación de péptidos, ya que no se observa un incremento significativo en la cantidad de Phe detectada. Sin embargo, con la proteasa de S. griseus luego de 1 hora de tratamiento, se cuantificó más de 2 g de Phe/16 g de nitrógeno, respectivamente, debido a que esta no tiene punto específico de acción.
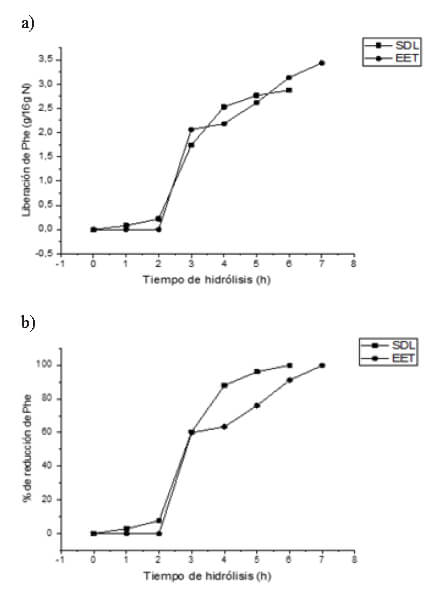
La liberación de la Phe ocurre más rápido en el suero de leche que en el aislado proteico de chachafruto, es así que en este último la separación total de la Phe ocurre una hora más tarde, asumiendo que esto puede ser debido a la matriz proteica de cada alimento. Es importante recalcar que el nivel de Phe de los hidrolizados filtrados a través de columnas de carbón activado no presenta cantidad detectable de Phe según los métodos de fluorometría y HPLC, por lo tanto, se supone la reducción del contenido del aminoácido a valores no identificables.
Perfil de aminoácidos de suero de leche en polvo, aislado proteico de chachafruto y los respectivos hidrolizados. En la Figura 2 se observa la diferencia entre el contenido de aminoácidos antes y después del tratamiento de hidrólisis para el suero dulce de leche, observándose que la Phe fue removida en su totalidad, mientras que la alanina un 85,88%, seguido de la isoleucina (65,40%), lisina (60,32%), prolina (59,07%), tirosina (54,69%), y en el resto de aminoácidos se perdió menos del 50%. Cabe mencionar que en la mayoría las concentraciones de los aminoácidos entre el suero dulce y su hidrolizado hay diferencias significativas.
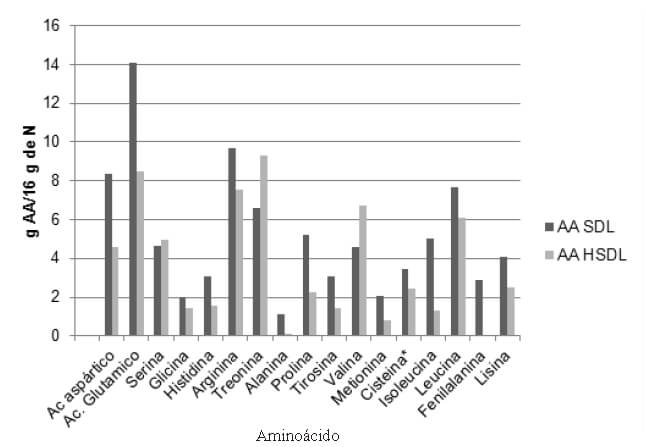
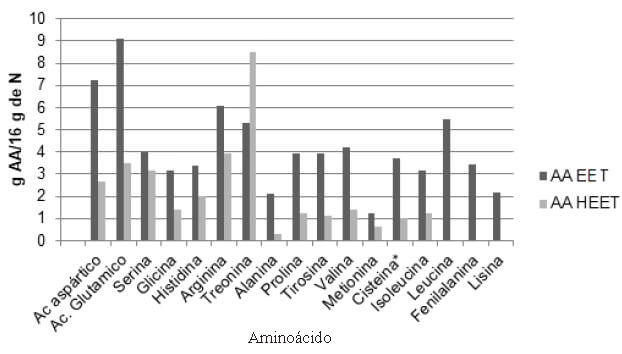
En la Figura 3 se observa la diferencia entre el contenido de aminoácidos de la chachafruto antes y después del tratamiento de hidrólisis, observándose que la Phe, lisina y leucina fueron removidas hasta valores no detectables, mientras que la mayoría fue removida sobre el 50 % de la cantidad inicial. Además, se encontraron diferencias estadísticamente significativas en el contenido de aminoácidos antes y después del hidrolizado de las proteínas del chachafruto en lo que corresponde a histidina, arginina, metionina y cisteína.
Caracterización química del suero de leche en polvo. En la Tabla 1, se presentaron los resultados obtenidos de la composición proximal del suero dulce de leche y los reportados por Arcila and Mendoza (15), de los cual, al comparar estos datos en base seca se observa que son similares. De acuerdo a lo establecido en la norma del CODEX(16) para suero en polvo (stand 289-1995), este debe tener un contenido de agua máximo de 5 % y de cenizas un 9,5%, mientras que a su vez establece que el contenido de proteína láctea debe ser como mínimo un 10%, cumpliendo el producto con lo establecido.
Preparación y caracterización de la harina de harina de chachafruto. En la Tabla 2 se reportó la composición proximal de la harina de chachafruto, donde se observa un contenido de 26,19% de proteína en base seca, valor que difiere del reportado por (17). Estos autores reportaron valores entre 18 a 21% de proteína. Mientras, que los valores de 20,5 % de proteína, 0,5% de grasa, 5,64% de cenizas y 73,33% de carbohidratos son reportados por (18). Estas diferencias, respecto a los valores obtenidos se pueden atribuir a muchos factores como son el método de extracción empleado, las condiciones ambientales-geográficas y agrarias del cultivo.
Obtención del aislado proteico de harina de chachafruto por precipitación del punto isoeléctrico. En la Tabla 3 se presentó el valor al que se llevó la proteína, contenido para que el producto sea considerado aislado proteico debe poseer más del 90% de proteínas(19). Estudios similares con pequeñas variaciones fueron realizados en la obtención de los concentrados. Esta extracción fue realizada a pH 12 de las proteínas solubles seguido de una precipitación ácida (pH 5) en el punto isoeléctrico, obteniéndose una concentración de proteína hasta un 86% (20).
Reducción y cuantificación del nivel de Phe de las proteínas hidrolizadas del suero y aislado proteico de chachafruto La Figura 1 (a) muestra la liberación de Phe y la Figura 1 (b) la cantidad de Phe removida tanto del suero como del aislado proteico de chachafruto, además se observa que el tratamiento de 2 horas con la pepsina no tiene efecto relevante en la liberación de Phe. Sin embargo, éstas tiene efecto sobre la formación de péptidos ya que hidrolizan únicamente enlaces peptídicos y exhiben preferencia por los enlaces hidrofóbicos, específicamente son favorecidos los residuos aromáticos, así como aquellos residuos azufrados, y preferentemente escinde el C-terminal de fenilalanina, leucina y en menor medida ácido glutámico (21). La pepsina no escinde enlaces que involucran valina, alanina o glicina (22).
La proteasa utilizada proveniente del microorganismo S. griseus produjo una hidrólisis relativamente importante dentro del concentrado proteico, lo cual se observa por el aumento de Phe dentro de la muestra, al aumentar el tiempo de hidrólisis. Efecto similar fue observado en los trabajos de (12, 23, 24) al utilizar esta enzima en un producto alimenticio y en leche, respectivamente.
La liberación de la Phe ocurre más rápido en el suero de leche que en el aislado proteico de chachafruto, es así que en este último la separación total de la Phe ocurre una hora más tarde, asumiendo que esto puede ser debido a la matriz proteica de cada alimento. Es importante recalcar que el nivel de Phe de los hidrolizados filtrados a través de columnas de carbón activado no presenta cantidad detectable de Phe según los métodos de fluorometría y HPLC, por lo tanto, se supone la reducción significativa del contenido del aminoácido.
No se encontró reportes en la literatura respecto a la reducción de Phe de los hidrolizados de harina de chachafruto, pero sí de otros productos. Por ejemplo en hidrolizados de caseína se logró una disminución de Phe del 92% (24). Esta discrepancia puede estar relacionada con la mayor cantidad de carbón activado o número de filtraciones del mismo. En Phaseolus vulgaris se logró remover la Phe en un 94,49% (23) y en concentrado proteico de amaranto se determinó la eficiencia de la remoción de Phe, midiendo el contenido de Phe después del tratamiento con carbón activado de lo cual obtuvo un 98,78% para el tratamiento con proteasa S. griseus y 96,16% con A. orizae, ambas a 37 °C y durante 3 horas de reacción(4).
Perfil de aminoácidos de suero de leche en polvo, aislado proteico de chachafruto y los respectivos hidrolizados. En la Figura 2 se observa el cambio en el contenido de aminoácidos del suero antes y después de la hidrólisis, además de indicar que la Phe fue removida hasta valores no detectables.
En este sentido, en los estudios realizados en la producción a escala piloto de sustancias péptidas con bajo contenido en Phe para pacientes con fenilcetonuria, lograron reducir el contenido de Phe de 40 a 0,4% una vez hidrolizando las proteínas del suero y con la utilización de carbón activado. El efecto de la utilización del carbón activado incide también sobre la concentración de los otros aminoácidos, por ejemplo: la tirosina y triptófano que se redujeron drásticamente; el ácido aspártico, treonina, prolina, valina, metionina, lisina, histidina y arginina se incrementaron levemente, mientras que la serina, ácido glutámico, glicina y alanina se vieron ligeramente disminuidos (12).
Otro estudio sobre la optimización de la extracción de hidrolizados de la proteína del arroz por medio de la acción de la enzima corolase PP y carbón activado, encontraron que el contenido final de fenilalanina en los hidrolizados osciló de 0,39 a 68,34 mg/100 g, correspondiendo a los niveles de remoción de 84 a 100% haciendo posible su uso en la preparación de las formulaciones para PKU (25). Otro resultado similar es el caso de la hidrólisis de suero donde obtuvieron una reducción significativa del contenido de fenilalanina (97,3%) y de la tirosina (63%) y se vieron afectados moderadamente la valina, lisina, glicina y leucina (26).
La Figura 3 muestra el cambio en el contenido de aminoácidos del chachafruto antes y después de la hidrólisis una vez removido la Phe con carbón activado. Un estudio de la determinación del perfil aminoacidico de péptidos de amaranto, luego del tratamiento con carbón activado indica la ausencia de aminoácidos como fenilalanina, tirosina, triptófano, metionina e isoleucina, mientras que prevalecen la histidina, arginina, cisteína, glicina (4). Es importante destacar que al comparar el perfil de aminoácidos del amaranto sin tratamiento y con tratamiento de carbón activado, determinaron una reducción sustancial en el contenido de aminoácidos aromáticos (4).
De acuerdo a los estudios mencionados anteriormente y en comparación con esta investigación, se define que la hidrólisis es un proceso que permite separar la Phe de las proteínas mediante el uso de enzimas, sin embargo, la acción de remoción mediante el uso de carbón activado no es específico para la Phe ya que, en todos los estudios incluido este, la cantidad de los otros aminoácidos también se ve afectado tanto en los hidrolizados del suero como del aislado proteico de chachafruto.
Al comparar las concentraciones de los Phe del suero dulce de leche obtenidos por fluorometría y HPLC, se determinó que no existe diferencia significativa entre los métodos aplicados, sin embargo, por la rapidez y facilidad se recomienda el método de fluorometría, que presenta el inconveniente que solo esta estandarizado para Phe, y según (27) el método de fluorometría es más sensible que el de HPLC.
Se obtuvieron hidrolizados proteicos con bajo contenido de fenilalanina a partir del suero dulce de leche en polvo y harina de E. edulis Triana, mediante un proceso de hidrolisis enzimática y filtración con carbón activado para pacientes con fenilcetonuria.
Los valores obtenidos de la composición del suero de leche se encuentran dentro de los límites establecidos por la norma CODEX. Mientras que para la harina de E. edulis Triana se obtuvo la composición proximal. El rendimiento del proceso de obtención de la harina fue bajo debido a su alto contenido de humedad. Para ambos casos los valores de fenilalanina fueron reducidos a niveles no detectables tanto por fluorometría como por HPLC.
Recibido: 29/11/2018
Aceptado: 27/03/2019