 ,
Abraham Wall-Medrano2
,
Abraham Wall-Medrano2  ,
José Luis Cárdenas-López1
,
José Luis Cárdenas-López1  ,
Ana Irene Ledesma-Osuna1
,
Ana Irene Ledesma-Osuna1  ,
Maribel Robles-Sánchez1
,
Maribel Robles-Sánchez1 
Introducción. El arándano (Vaccinium corymbosum L.) posee un alto contenido de compuestos fenólicos los cuales han sido estudiados principalmente por su actividad antioxidante, antiobesogénica, antiinflamatoria, entre otras. Objetivo. Evaluar el efecto de la digestión gastrointestinal in vitro sobre la bioaccesibilidad de compuestos fenólicos y actividad antioxidante de una formulación nutracéutica de arándano (cápsula), comparado con arándano fresco y polvo. Materiales y métodos. Se obtuvieron extractos metanólicos de muestras de arándano fresco y liofilizado y se determinó su contenido de fenoles, flavonoides y antocianinas totales, así como también actividad antioxidante. Se llevó a cabo un ensayo de simulación de digestión gastrointestinal para evaluar la bioaccesibilidad de los compuestos fenólicos presentes en las muestras. Resultados. Los resultados mostraron que la digestión gástrica de arándano en polvo y en cápsula promovió una mayor bioaccesibilidad de fenoles (42% y 40%), flavonoides (52% y 33%) y antocianinas (45% y 40%) comparado con digestos de arándano fresco. Posterior a la digestión intestinal, la bioaccesibilidad de fenoles (63%) y flavonoides (67%) fue mayor en la cápsula de arándano comparada con su contraparte arándano en polvo. Las condiciones de digestión intestinal afectaron negativamente la bioaccesibilidad de las antocianinas independientemente del tipo de muestra evaluada. Conclusión. Las condiciones de digestión gástrica promueven una mayor estabilidad de los compuestos fenólicos en arándano en polvo y en cápsula lo que pudiera ser relevante para el mantenimiento de un ambiente antioxidante a este nivel. Las condiciones de digestión intestinal afectaron de manera particular a los compuestos fenólicos de arándano fresco y polvo, pero no a la cápsula, lo que puede sugerir que el encapsulamiento protegió de las condiciones alcalinas a los fenoles presentes. Se sugieren estudios posteriores sobre absorción in vitro de los componentes remanentes en intestino y sus posibles efectos sobre biomarcadores de estrés oxidativo en modelos in vivo. Arch Latinoam Nutr 2022; 72(1): 11-22.
Palabras clave: bioaccesibilidad, compuestos fenólicos, bioactividad, arándanos.
Introduction. Blueberry (Vaccinium corymbosum L.) has a high content of phenolic compounds which have been studied mainly for their antioxidant, antiobesogenic, anti-inflammatory activity, among others. Objetive. The objective of the present study was to evaluate the effect of in vitro gastrointestinal digestion on the bioaccessibility of phenolic compounds and antioxidant activity of a nutraceutical formulation of blueberry (capsule), compared to fresh and powder blueberry. Materials and methods. Methanolic extracts of fresh and lyophilized blueberry were obtained and determined its total phenols, flavonoids, anthocyanins content, as well as antioxidant activity. A gastrointestinal digestion simulation test also was carried out to assess the bioaccessibility of the phenolic compounds found in samples. Results. The results showed that gastric digestion of powder and capsule blueberry promoted greater bioaccessibility of phenols (42% and 40%), flavonoids (52% and 33%) and anthocyanins (45% and 40%), compared to fresh blueberry digests. After intestinal digestion, the bioaccessibility of phenols (63%) and flavonoids (67%) was higher in the blueberry capsule compared to its powdered blueberry counterpart. The intestinal digestion conditions negatively affected the bioaccessibility of anthocyanins regardless of the type of sample evaluated. Conclusion. Gastric digestion conditions promote greater stability of phenolic compounds in powdered and capsule blueberries, which could be relevant for the maintenance of an antioxidant environment at this level. The intestinal digestion conditions particularly affected the phenolic compounds of fresh and lyophilized blueberry, but not the capsule, which may suggest that encapsulation protected the phenols present from alkaline conditions. Further studies on in vitro absorption of the remaining components in the intestine and their possible effects on oxidative stress biomarkers in in vivo models are suggested. Arch Latinoam Nutr 2022; 72(1): 11-22.
Key words: bioaccessibility, phenolic compounds, bioactivity, blueberry.
https://doi.org/10.37527/2022.72.1.002
Autor para la correspondencia: Maribel Robles-Sánchez, E-mail: [email protected]
Los compuestos fenólicos se encuentran distribuidos ampliamente en el reino vegetal y constituyen una gran familia de sustancias las cuales incluyen desde moléculas de bajo peso molecular como los ácidos fenólicos hasta moléculas de gran tamaño molecular como los taninos (1). En las últimas décadas los compuestos fenólicos han venido siendo materia de estudio dado los efectos benéficos que estos compuestos confieren a la salud humana, ya que se ha demostrado una relación directa entre el consumo de estos compuestos y la reducción de diversas enfermedades crónicas. Por ejemplo, los fenoles han sido estudiados por su efecto antiobesogénico (2), antidiabético (3), algunos tipos de cáncer (4) y enfermedad cardiovascular (5).
Dentro del grupo de los llamados “super alimentos” destacan las bayas, el arándano azul (V. corymbosum L.), ha sido de los más estudiados. Además de su aporte nutricional, este fruto posee un alto contenido de compuestos fenólicos, predominando los ácidos fenólicos y flavonoides, estos últimos incluyen a las antocianinas, las cuales son pigmentos que intensifican el color de los arándanos, y que además poseen algunas actividades biológicas tales como antiinflamatorias, antiobesógenicas y antioxidantes (6-10). Se ha demostrado que las antocianinas son extremadamente inestables y su degradación está influenciada por oxígeno, temperatura, pH, luz y actividad enzimática (11). Asimismo, ciertas condiciones fisiológicas como la digestión gastrointestinal asociada a la estructura de los compuestos pueden afectar su estabilidad limitando en gran medida su biodisponibilidad (12). En la búsqueda de alcanzar una mayor estabilidad y por lo tanto una mayor bioaccesibilidad de estos compuestos se han probado diferentes procesos tecnológicos, especialmente procesos de deshidratación. La obtención de polvo de arándano presenta algunas ventajas sobre el arándano fresco especialmente por el efecto de concentración de componentes que se presenta por la eliminación de agua, de tal forma que es posible su uso como aditivo en otros alimentos (13). También algunos estudios han evaluado el efecto de la microencapsulación (14-15); otros trabajos se han enfocado hacia la extracción de los compuestos fenólicos de arándano y su posterior integración con otros componentes alimentarios como proteínas o polisacáridos (16-18). Desde hace muchos años la industria farmacéutica hace uso de materiales de origen natural y biodegradables para la encapsulación de una gran variedad de fármacos, no obstante, la encapsulación de ingredientes activos provenientes de fuentes naturales o de alimentos completos es relativamente reciente. Este tipo de materiales se encuentran junto con los comprimidos, dentro del grupo de los llamados nutracéuticos (19-20).
Hasta donde se sabe, no existen formulaciones de arándano en polvo en forma de cápsulas, particularmente tomando en cuenta que algunos materiales de los que están constituidas las cápsulas pudieran presentar cierta protección a las condiciones de digestión gastrointestinal. La industria farmacéutica ha alcanzado un grado de especialización en el uso de estos materiales, sin embargo, existe poca información en relación al uso de cápsulas como contenedores de componentes derivados de alimentos. Por lo anteriormente expuesto, surge el interés de evaluar la bioaccesibilidad de compuestos fenólicos y actividad antioxidante de digestos de cápsulas de arándano. Los resultados derivados pudieran marcar la pauta para futuros estudios de tipo farmacocinéticos y de esta manera brindar una opción nutracéutica a individuos que pudieran tener un impedimento al uso de fármacos.
Para este estudio se utilizó arándano azul (V. corymbosum L.) el cual fue adquirido en un comercio de la localidad, en la Ciudad de Hermosillo, Sonora, México. Las frutas fueron lavadas con agua destilada y enseguida fueron colocadas sobre papel absorbente para eliminar exceso de agua de lavado. Se formaron dos lotes de 2 kg cada uno y un lote de fruta se destinó para los ensayos con la fruta fresca (arándano fresco), mientras que otro lote se llevó a proceso de liofilización, en el cual primeramente las frutas enteras fueron congeladas a -20°C y colocadas en charolas, para enseguida proceder a su liofilización usando un equipo de liofilización (LABCONCO Kansas City, USA), el cual fue operado a una presión absoluta de 0,34 mBar y una temperatura de condensación de -50°C durante 24 h. Las muestras liofilizadas fueron llevadas a molienda hasta obtener un tamaño de partícula de 0,5 mm utilizando un molino experimental (Laboratory Mill Mod.3100). Las muestras de polvo de arándano se separaron en dos lotes uno fue etiquetado como arándano polvo y el otro lote se destinó para la preparación de las cápsulas de arándano y etiquetado como cápsula de arándano. Se utilizaron cápsulas comerciales (Tipo 00) de gelatina bovina, con capacidad de llenado de 0,7 g de arándano polvo las cuales fueron llenadas manualmente y utilizadas para el ensayo de digestión gastrointestinal in vitro.
La preparación de los extractos metanólicos se llevó a cabo de acuerdo con la metodología propuesta por Tagliazucchi et al. (21) y Salazar-López et al. (22). Las muestras frescas y liofilizadas (1 g) fueron colocadas en tubos falcon de 25 mL y posteriormente se le añadieron 15 mL de metanol (80%). La mezcla fue sonicada a temperatura ambiente por 30 min y posteriormente centrifugada a 6000 rpm durante 15 min, y colectado el sobrenadante. El procedimiento se repitió dos veces y en la última extracción se utilizó metanol acidificado (HCl 0.1 M). Los sobrenadantes fueron colectados y filtrados en papel Whatman Num 1. Posteriormente el volumen de todos los extractos se llevó a 50 mL. La concentración final de los extractos fue de 0,02 g/mL. Los extractos fueron usados para la cuantificación de fenoles totales (FT), flavonoides totales (FLAT), antocianinas totales (AT) y actividad antioxidante.
Se determinó el contenido de fenoles totales en las muestras de acuerdo con la metodología propuesta por Singleton et al. (23), adaptada a microplaca; los resultados se expresaron como miligramos equivalentes de ácido gálico por gramo de muestra (mgEAG/g). Para la determinación de flavonoides totales se utilizó el método de cloruro de aluminio, siguiendo la metodología descrita por Robles-Sánchez et al. (24) adaptada a microplaca. El contenido total de flavonoides se calculó a partir de una curva estándar de quercetina y los resultados se expresaron como miligramos equivalentes de quercetina por gramo de muestra (mgEQ/g).
El contenido de antocianinas se midió por el método de diferencial de pH (25). Las antocianinas monoméricas totales se calcularon mediante la siguiente ecuación (Eq. 1).
Antocianinas totales (mg C3G/g) = (A×PM×FD×1000) / (ε × 1)
Donde: mgC3G/g corresponde a la unidad de expresión del resultado (mg de cianidin-3-glucósido) por cada gramo de muestra; A corresponde a la absorbancia (A510 – A700) pH1.0 – (A510 – A700) pH4.5; PM corresponde al peso molecular de cianidin-3 glucósido (449,9 g.mol-1); FD es el factor de dilución; ε es el coeficiente de extinción molar de cianidin-3-glucósido a 510 nm (26 900); 1 corresponde a la longitud (cm) del paso de luz de una celda de borosilicato.
Se determinó la capacidad de secuestramiento del radical ABTS de acuerdo a la metodología propuesta por Salazar-López et al. (22). Brevemente, 10 μL de cada uno de los extractos fueron depositados en pocillos de microplaca conteniendo una solución de trabajo de ABTS (280 μL) con una absorbancia ≈0.7. Las muestras se mantuvieron en reposo por 5 min y posteriormente la absorbancia se midió a 745 nm. Los resultados fueron expresados como μmol equivalentes de trolox por gramo de muestra (μMET/g) usando una curva de calibración de Trolox.
Para la estimación de la bioaccesibilidad de compuestos fenólicos de arándano fresco, polvo y en cápsula, fue necesario imitar las condiciones de las tres fases de digestión gastrointestinal in vitro (oral, gástrica e intestinal) de acuerdo con la metodología gastrointestinal in vitro de INFOGEST con ligeras modificaciones (26). Tres voluntarios en un rango de edad de 35-55 años, aparentemente saludables y en ayunas otorgaron su consentimiento para participar en el estudio. Los participantes masticaron durante 15 s 0,7 g de cada una de las muestras (cápsula de arándano no fue masticada tratando de simular la ingestión de este tipo de formulaciones y solamente se pasó por boca con un tiempo de residencia no mayor a 5 seg). Posteriormente, los sujetos expulsaron la muestra masticada hacia tubos falcon de 50 mL, (9 tubos por muestra), se enjuagaron la boca dos veces con 5 mL de agua durante 60 s y luego expulsaron el líquido hacia sus respectivos tubos. Para la obtención del digesto oral se retiraron tres tubos de cada set de muestras, los cuales fueron mantenidos durante tres minutos en baño maría a 37°C/100 rpm y enseguida puestos en baño de hielo para detener actividad enzimática. Los seis tubos restantes de cada una de las muestras fueron llevados a proceso de digestión gástrica, agregando a los digestos 5 mL de solución tampón HCl-KCl 0,2 M y haciendo un ajuste de pH a 1,5. Enseguida se agregaron 667 μL de solución de pepsina (300 mg/mL) y los tubos se incubaron durante 1 h en un baño de agua con agitación constante a 37°C (Precisión Scientific Mod. 66800 Winchester, VA, USA). Terminado el tiempo de incubación se retiraron tres tubos de cada una de las muestras y estas fueron llevadas a baño de hielo. Las muestras restantes fueron llevadas a proceso de digestión intestinal. A cada uno de los tubos procedentes de la digestión gástrica se les añadieron 9,0 mL de solución fosfato (0,1 M, pH 7,5) y el pH se ajustó a 7,5. Se agregó 1 mL de solución de pancreatina (17 mg/mL) y sales biliares (80 mg), y la mezcla se incubó durante 6 h en un baño de agua con agitación a 37°C y 100 rpm para obtener el digesto intestinal. Todos los digestos procedentes de cada fase fueron centrifugados durante 15 minutos a 6000 rpm a temperatura ambiente; se midió el volumen final de cada uno de los sobrenadantes y posteriormente fueron filtrados (Econofltr Nyln 0.45 μm, Santa Clara, CA, USA). En los sobrenadantes se determinó la fracción bioaccesible de fenoles, flavonoides y antocianinas totales. Para esta última determinación fue necesario eliminar las sales biliares mediante el paso por una columna de resina C18 (20). La bioaccesibilidad (%) fue calculada como la proporción entre la concentración del componente bioactivo en las tres fases de la digestión (sobrenadantes) y su respectiva concentración en los frutos (Eq. 2). Los resultados fueron expresados en términos de porcentaje (B %).

La actividad antioxidante también fue analizada por este procedimiento y expresada como % de recuperación.
Para la evaluación del efecto de los tratamientos sobre las variables respuesta, el diseño experimental del estudio fue completamente al azar, todas las muestras del presente ensayo se analizaron por triplicado y los resultados fueron analizados mediante una ANOVA. Se realizó la prueba de Tukey para diferenciación entre medias a un nivel de significancia de P<0,05, para el análisis estadístico de los datos se utilizó el programa estadístico JMP V16.
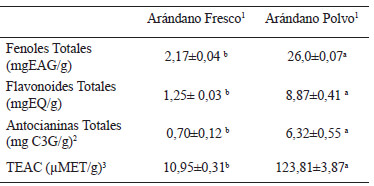
En la Tabla 1 se muestra el contenido de fenoles, flavonoides y antocianinas totales así como también la actividad antioxidante presente en arándano fresco y polvo antes del proceso de digestión. Se observa que los componentes fenólicos en su conjunto y actividad antioxidante mostraron valores más altos en la muestra liofilizada. Este incremento fue del orden de 11,0, 6,1, 7,9 y 10,3 veces más alto para fenoles, flavonoides antocianinas totales y actividad antioxidante respectivamente.
En el presente estudio, se evaluó el contenido de compuestos fenólicos (fenoles, flavonoides y antocianinas totales y actividad antioxidante) en tres fases de digestión in vitro (oral, gástrica e intestinal) de 0,7 g de arándano fresco, 0,7 g de arándano polvo y 0,7 g de arándano liofilizado y empacado en cápsula de gelatina bovina, con el fin de evaluar un posible efecto de protección de los compuestos fenólicos durante su paso por el proceso de simulación de digestión gastrointestinal.
Fenoles Totales. La Figura 1A, muestra el contenido de fenoles totales para las tres fases de digestión y para las tres muestras analizadas. Para arándano fresco se presentó un incremento gradual conforme transcurrió el proceso de digestión, con valores de 0,147±0,008, 0,582±0,019 y 1,239±0,029 mgEAG/0,7 g de muestra, para las fases de digestión oral, gástrica e intestinal respectivamente. Para el arándano polvo, se presentó un comportamiento similar al reportado para arándano fresco con la diferencia de que el contenido de fenoles totales fue significativamente más alto, en una relación aproximada de 1:30 (0,147±0,008 vs 4,650±0,144), 1:13 (0,582±0,019 vs 7,510±0,246 mgEAG/0,7 g muestra) y 1:5 (1,239±0,029 vs 6,984±0,980 mgEAG/0,7 g muestra) para digestión oral, gástrica e intestinal respectivamente. El contenido de fenoles totales en las muestras de cápsula de arándano mostró un comportamiento diferente en el sentido de que los valores se mostraron significativamente más altos en la fase intestinal (+65%) respecto a las muestras de arándano polvo.
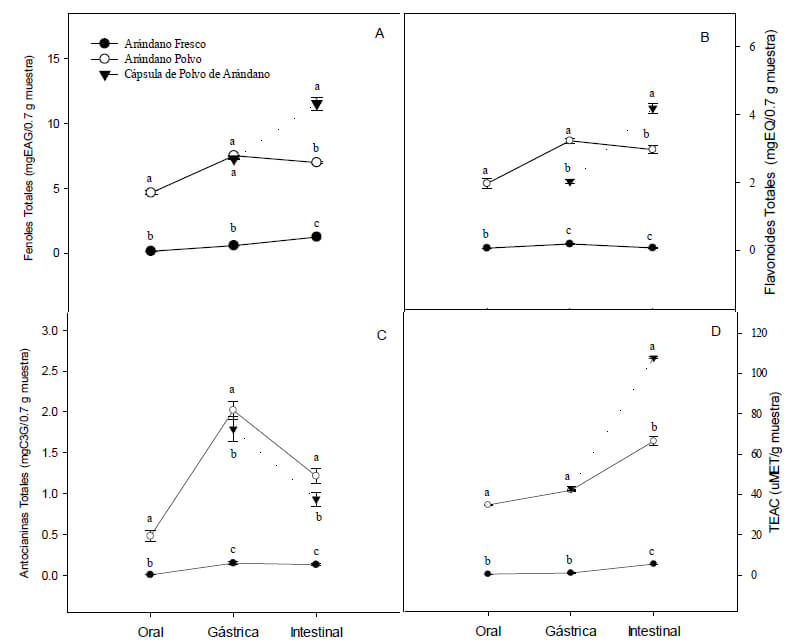
Flavonoides totales. El contenido de flavonoides totales en las muestras digeridas (Figura 1B) presentó un comportamiento similar al presentado para fenoles totales, en donde los valores más bajos correspondieron a las muestras de arándano fresco para las tres fases de la digestión. Haciendo una comparación entre arándano polvo y arándano en cápsula, se observa que la concentración de flavonoides totales de los digestos gástricos de arándano polvo fue aproximadamente un 62% más alta que su contraparte arándano en cápsula, sin embargo, cuando las muestras fueron sometidas a digestión intestinal, fueron las muestras de arándano en cápsula quienes superaron el contenido de flavonoides totales hasta en un 40%.
Antocianinas Totales. El contenido de antocianinas presentes en arándano fresco, polvo y cápsula mostraron un incremento de la fase oral a la fase gástrica sin cambios significativos para arándano fresco. Los valores en este componente disminuyeron notablemente cuando las muestras fueron sometidas a digestión intestinal para las tres muestras evaluadas. En términos de porcentaje esta disminución de la fase gástrica a la intestinal fue de 13%, 40% y 48% para arándano fresco, polvo y cápsula respectivamente (Figura 1C). En relación al comportamiento de la actividad antioxidante medida por el ensayo de TEAC, durante el proceso de digestión gastrointestinal, en la Figura 1D se muestran los valores para arándano fresco, polvo y cápsula. Se presentó una tendencia hacia un incremento en los valores conforme avanzó el proceso de digestión. Siendo en la fase de digestión intestinal donde la actividad antioxidante se incrementó considerablemente (5,44±0,025, 66,40±2,21 y 107,74 μMET/0,7 g para arándano fresco, polvo y arándano en cápsula respectivamente).
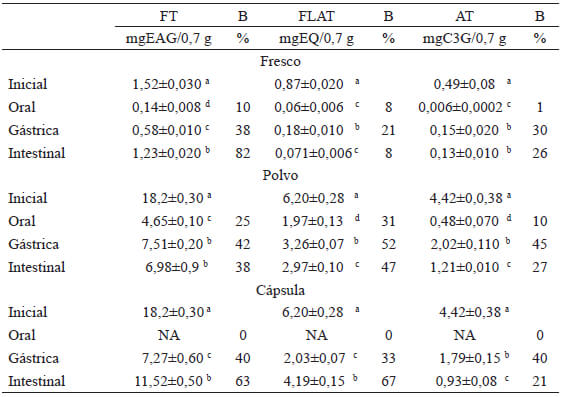
Bioaccesibilidad. En la Tabla 2, se presenta el contenido inicial de fenoles, flavonoides y antocianinas totales en arándano fresco, polvo y cápsula ajustado a 0,7 g de muestra. Cabe señalar que estos contenidos fueron considerados como el 100% de máxima extracción metanólica y tomado como referencia para el cálculo de bioaccesibilidad de estos componentes. Destaca primeramente que ninguno de los componentes evaluados durante el proceso de digestión gastrointestinal alcanzó 100% de bioaccesibilidad, esto puede significar que las condiciones de digestión no favorecieron una liberación que pudiera superar a lo encontrado en las muestras antes de la digestión. No obstante, es posible observar un comportamiento interesante en relación a la dependencia entre la concentración de componentes fenólicos presentes en las muestras antes de la digestión y su correspondiente porcentaje de bioaccesibilidad de la fase oral a la gástrica. De tal manera que a mayor contenido de FT, FLAT y AT en los digestos de arándano fresco y polvo, mayor fue su porcentaje de bioaccesibilidad. Refiriéndonos ahora a la bioaccesibilidad de los componentes presentes en las muestras de arándano posterior a la digestión intestinal, se puede observar que el contenido de FT, FLAT y AT disminuyó en muestras de arándano fresco y polvo (a excepción del contenido de FT en digestos intestinales de muestras de arándano fresco) esta disminución fue asociada a una reducción en el porcentaje de bioaccesibilidad. Para arándano en cápsula se presentó un efecto contrario, es decir, tanto el contenido como el porcentaje de bioaccesibilidad de FT como de FLAT se incrementaron significativamente en los digestos intestinales. No obstante la bioaccesibilidad de AT de las tres muestras evaluadas fue mayormente favorecida en la fase gástrica.
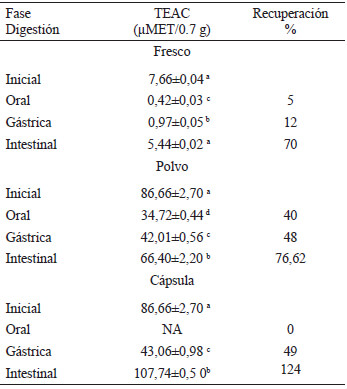
En la Tabla 3 se muestra la actividad antioxidante inicial medida por el ensayo de TEAC en muestras de arándano fresco, polvo y cápsula (inicial) y recuperación de actividad antioxidante en términos de porcentaje en cada una de las fases de digestión (oral, gástrica e intestinal). Para las tres muestras evaluadas se presentó una tendencia hacia un incremento en los porcentajes de recuperación a medida que se avanzó en el proceso de digestión gastrointestinal.
Los compuestos fenólicos particularmente las antocianinas son susceptibles a oxidación y descomposición química por temperaturas y humedad, luz ultravioleta, pH entre otros factores, por lo que se han estudiado diversas tecnologías para mejorar la estabilidad de estos compuestos tales como la pasteurización, ultrasonido de alta intensidad, microencapsulación y remoción de agua bajo condiciones controladas (13, 27). El proceso de liofilización ha sido uno de los procedimientos más utilizados para mejorar la estabilidad de compuestos bioactivos en arándano. Una consecuencia de este proceso es un aumento significativo de las concentraciones de los componentes fenólicos y actividad antioxidante en el fruto, tal como se presentó en nuestro estudio. Sin embargo, adicional a este efecto, es relevante mencionar que el proceso de liofilización no promueve pérdidas, pero sí modifica la estructura química de algunos componentes, y es que la sola remoción de agua puede incentivar interacciones entre los componentes químicos del fruto, favoreciéndose reacciones de oxidación, polimerización entre otros efectos, lo que pudo haber afectado de manera importante en los valores de fenoles totales en su conjunto. De aquí que las proporciones expresadas en referencia a los resultados mostrados en la Tabla 1 no sean similares para todos los componentes.
Por otra parte, es importante señalar que existe una amplia variabilidad en el contenido de compuestos fenólicos totales y por subgrupo en arándano fresco, atribuído a factores como el cultivar, zona geográfica de cultivo y prácticas de postcosecha en el fruto (28-30). El efecto del proceso de secado por liofilización sobre contenido de fenoles y actividad antioxidante ha sido ampliamente estudiado en arándano y los resultados han sido similares a los encontrados en el presente estudio (31, 27).
Para el caso del contenido de flavonoides totales, se sabe que estos pueden ser afectados por diferentes factores agronómicos y por lo tanto la variabilidad también puede ser muy alta. Bunea et al. (32) reportó valores de flavonoides totales en arándano de diferentes variedades en el orden de 1.03 mg EQ/ g, 0.92 mg EQ/g y 0.84 mg EQ/g para cultivares ‘Bluecrop’, ‘Elliot’ y ‘Duke’ respectivamente. Las variaciones en el contenido de compuestos flavonoides también pueden ser atribuidas al proceso de extracción química utilizado para su cuantificación (33). También se han reportado rangos muy amplios en el contenido de flavonoides totales dentro de cultivares de una misma especie como lo reportado por Saral et al. (34) que encontraron valores desde 0.74 - 5.65 mgEQ/g muestra. Para el caso de antocianinas, en un estudio de Rodrigues et al. (30), reportaron valores de arándano azul fresco similares a los obtenidos en nuestro estudio. En otros estudios se ha demostrado que el contenido de antocianinas puede variar de manera significativa conforme aumenta el estado de madurez del fruto con valores que pueden ir desde 0.019±0.002 mgAT/g para frutos inmaduros hasta 0.704±0.03 mgAT/g para frutos maduros (35)
Las antocianinas son flavonoides que contribuyen de manera significativa al contenido total de fenoles. Kalt et al. (36), demostraron que el porcentaje de contribución de antocianinas al contenido de fenoles totales se va incrementando a medida que el fruto va madurando, con porcentajes que van desde el 2% para frutos inmaduros hasta el 60% para frutos maduros (100% azules) esto para algunos cultivares de arándano azul; sin embargo, también en este estudio se observó que esta contribución disminuye significativamente una vez que el fruto ha sobremadurado. Para el caso de nuestro estudio la contribución de antocianinas al contenido de fenoles totales fue del 67% para muestras frescas y del 25% para muestras liofilizadas, este resultado puede sugerir que el proceso de liofilización afecta de manera importante el contenido de antocianinas.
En arándanos predominan las antocianinas monoméricas (glucosiladas) por encima de las no glucosiladas (antocianidinas) y prácticamente todas las antocianidinas precursoras (malvidina, petunidina, delfinidina, peonidina y cianidina) están presentes en este fruto (37), aunque dependiendo del estado de madurez del fruto los contenidos de estas antocianinas se pueden modificar, destacando la cianidin-3-glucósido en frutos (rojizo-púrpura) como la antocianina predominante, también es relevante mencionar que en fases inmaduras del fruto, la glicosilación de los monómeros no se presenta por lo que es muy probable encontrar antocianidinas (35). Olivas-Aguirre et al. (31) estudió la misma variedad comercial de arándano azul que estudiamos aquí, reportando varios ácidos fenólicos, flavonoides y antocianidinas.
Los compuestos fenólicos en su conjunto contribuyen a la actividad antioxidante del fruto. En diversos estudios se han reportado valores similares a los mostrados en el presente estudio (28, 30), aunque algunos autores han reportados valores de actividad antioxidante hasta 5 veces más altos (33). Sobre esto último, Baenas et al. (38) reportó valores de actividad antioxidante en un cultivar andino de arándano polvo, medida como TEAC (278.2±59 μMET/g), un valor que significa poco más del doble que lo obtenido en nuestro estudio.
Los beneficios del consumo de compuestos fenólicos dietarios van a depender de la accesibilidad en la que estos compuestos se presenten en los frutos (fenoles extraíbles ‘libres’), la diversidad molecular de los compuestos, las interacciones que estos tengan con otros componentes de la matriz alimentaria, la cantidad de fenoles consumida y particularmente de su estabilidad a lo largo del tracto gastrointestinal, todo lo anterior pudieran ser factores limitantes para su potencial absorción. En el estudio de Parada et al. (39), se menciona que la microestructura de la matriz alimentaria juega un papel importante en el proceso de biodisponibilidad de un compuesto bioactivo/nutriente, de tal manera que el autor indica que entre menos compleja sea la molécula más grande será su posibilidad de ser bioaccesible, absorbible y por tanto biodisponible.
En el presente estudio, resalta el hecho de que las condiciones de digestión gastrointestinal in vitro no favorecieron la estabilidad de los componentes fenólicos de las tres muestras evaluadas en el sentido de que ninguna de las muestras digeridas logró alcanzar los contenidos observados en las muestras originales (antes de la digestión). Lo anterior ya ha sido discutido por diversos autores que destacan la susceptibilidad a degradación de los compuestos fenólicos y particularmente de las antocianinas ante las condiciones de digestión gastrointestinal (40-41).
A pesar de lo anterior, cabe destacar la influencia significativa atribuida al proceso de liofilización ya que tanto arándano polvo como en cápsula mostraron los valores más altos en fenoles, flavonoides y antocianinas totales durante el proceso de digestión gastrointestinal in vitro comparado con arándano fresco. Específicamente, en la fase gástrica se encontró un mayor contenido de antocianinas totales, para todas las muestras estudiadas, lo anterior puede explicarse por un lado, considerando las condiciones ácidas presentes en la digestión gástrica que dieron lugar a la formación del catión flavilio una forma coloreada estabilizada de las antocianinas (42), por otra parte, diversos autores han mencionado que algunos ácidos fenólicos presentes y liberados de la matriz alimentaria pueden bajo las condiciones ácidas de la digestión gástrica llevar a cabo una función como co-pigmentos brindando estabilidad a las antocianinas (43-44). Un aspecto relevante que se deriva de lo anterior es que la presencia de estos compuestos fenólicos en la fase gástrica pudiera promover un ambiente antioxidante, que puede repercutir en la inactivación de radicales libres, cabe mencionar que la fase gástrica al igual que la intestinal son importantes fuentes productoras de radicales libres (45).
A nivel intestinal y comparando entre muestras de arándano polvo y en cápsula, esta última demostró tener una mayor capacidad para estabilizar a fenoles y flavonoides totales, lo que pudiera sugerir que el material del que está construida la cápsula (gelatina bovina) fungió como barrera de protección a las condiciones alcalinas del proceso de digestión intestinal. Butkeviciut et al. (46), modelaron cápsulas duras de gelatina con manzana liofilizada y estudiaron la cinética de liberación de los compuestos fenólicos en función del tiempo de disolución y de la cápsula y demostraron que la cápsula puede ser considerada de rápida disolución cuando se ha liberado el 85% del componente bioactivo en este caso correspondió al ácido clorogénico. Pudiera ser relevante realizar un estudio similar con el fin de valorar el posible uso de la cápsula dura como base para el desarrollo de suplementos nutracéuticos basados en polvo de arándano.
La importancia de conocer el contenido de compuestos fenólicos y actividad antioxidante en las diferentes fases de la digestión gastrointestinal radica en el hecho de que es posible asumir que las condiciones de digestión gastrointestinal están promoviendo un efecto que puede ser positivo o negativo, dependiendo de algunos factores como la constitución de la matriz alimenticia y las interacciones entre los componentes de la misma. Lo anterior brinda la posibilidad de inferir el potencial de absorción y bioactividad del componente. Sin embargo, estos resultados pueden no informar acerca de la bioaccesibilidad del componente fenólico es decir tomar en cuenta la proporción que se libera y que está potencialmente disponible para absorción en relación con el contenido original de la muestra antes de la digestión. Contar con esta información permite tomar decisiones en relación a posibles transformaciones de tipo tecnológicas o bioprocesamientos que puedan mejorar la bioaccesibilidad del material alimenticio a digerir.
Durante el proceso de digestión gastrointestinal, la fase gástrica es la que puede asumirse como la que favoreció la estabilidad de los componentes fenólicos evaluados, ya que es en esta fase en donde se encontraron los valores más altos de bioaccesibilidad para las tres muestras evaluadas y específicamente más alta la bioaccesibilidad en muestras liofilizadas y en cápsula.
Situaciones muy particulares se presentaron durante la fase de digestión intestinal, primero, el valor más alto de bioaccesibilidad de fenoles totales correspondió a digestos de arándano fresco, lo anterior puede tener su explicación en dos aspectos uno sería la presencia de agua que pudo promover reacciones de hidrólisis durante el proceso de digestión y liberar una mayor cantidad de compuestos fenólicos y por otra parte es importante mencionar la naturaleza del ensayo de Folin, que tiende a sobreestimar los resultados. A excepción del resultado anterior, tanto fenoles como flavonoides y antocianinas totales de digestos de arándano fresco y polvo mostraron una reducción en su bioaccesibilidad. Lo anterior puede significar que las condiciones de digestión intestinal no fueron favorables para este tipo de componentes por lo que pudieron presentarse procesos degradativos o de polimerización de estos compuestos.
Bajo las condiciones establecidas en el presente estudio las antocianinas contenidas en arándano fresco, polvo o encapsulado terminan degradándose en un rango de 73-79%. Sin embargo, la propuesta nutracéutica sigue siendo viable, ya que es importante destacar la alta bioaccesibilidad de fenoles y flavonoides totales en la fase gástrica, ya que además de brindar un ambiente antioxidante a nivel gástrico, también existe la posibilidad de absorción de estos componentes a nivel gástrico (47). Además, es importante mencionar que los componentes que no sean susceptibles de absorción pueden llegar a ser utilizados por el microbiota del colon (12). Hacer referencia a un ambiente antioxidante implica el conocimiento de la actividad antioxidante que puede ser atribuida a los componentes fenólicos presentes en las muestras de arándano estudiadas. Sin embargo, también cabe la posibilidad de la presencia de otros componentes de naturaleza no fenólica que pudieran estar contribuyendo al incremento de la actividad antioxidante.
Las condiciones de digestión gástrica in vitro promovieron una mayor estabilidad de fenoles, flavonoides y antocianinas en las muestras de arándano polvo y cápsula. Las condiciones de digestión intestinal favorecieron la bioaccesibilidad de fenoles y flavonoides totales, pero no la de antocianinas en donde independientemente de la constitución de la muestra los valores fueron similares.
Daniel Tánori Encinas recibió beca de CONACyT (Consejo Nacional de Ciencia y Tecnología) México.
Los autores declaran que no hay conflicto de interés.
Recibido: 13/06/2021
Aceptado: 15/12/2022